APRUEBA REGLAMENTO SANITARIO DE LOS ALIMENTOS
Núm. 977.- Santiago, 6 de agosto de 1996.- Visto:
estos antecedentes; la necesidad de actualizar la normativa
sobre productos alimenticios; lo establecido en los
artículos 2º y 9º letra c) y en el Libro IV del Código
Sanitario, aprobado por decreto con fuerza de ley Nº 725,
de 1967 y en el artículo 4º letra b) y 6º del decreto ley
Nº 2.763 de 1979 y teniendo presente las facultades que me
confiere el artículo 32 Nº 8 de la Constitución Política
del Estado
D e c r e t o:
Apruébase el siguiente Reglamento Sanitario de los
Alimentos:
|
|
TITULO PRELIMINAR
|
|
Artículo 1.- Este reglamento establece las
condiciones sanitarias a que deberá ceñirse la
producción, importación, elaboración, envase,
almacenamiento, distribución y venta de alimentos para uso
humano, así como las condiciones en que deberá efectuarse
la publicidad de los mismos, con el objeto de proteger la
salud y nutrición de la población y garantizar el
suministro de productos sanos e inocuos.
Este reglamento se aplica igualmente a todas las
personas, naturales o jurídicas, que se relacionen o
intervengan en los procesos aludidos anteriormente, así
como a los establecimientos, medios de transporte y
distribución destinados a dichos fines.
Para la aplicación del presente reglamento regirán
las definiciones y requisitos que su texto establece.
|
| Decreto 32, SALUD
Art. 1 N° 1
D.O. 28.11.2016 |
|
Artículo 2.- Alimento o producto alimenticio es
cualquier substancia o mezclas de substancias destinadas al
consumo humano, incluyendo las bebidas y todos los
ingredientes y aditivos de dichas substancias.
Materia prima alimentaria es toda sustancia que para
ser utilizada como alimento, precisa de algún tratamiento o
transformación de naturaleza química, física o
biológica.
|
|
Artículo 3.- Todos los alimentos y materias primas,
deberán responder en su composición química, condiciones
microbiológicas y caracteres organolépticos, a sus
nomenclaturas y denominaciones legales y reglamentarias
establecidas.
Los eventos biotecnológicos, que modifiquen determinados alimentos y/o materias
primas alimentarias para consumo humano, y los alimentos,
ingredientes y materias primas alimentarias nuevos, deberán
figurar en la nómina dictada
por el Ministerio de Salud para tales efectos, mediante la
correspondiente norma técnica basada en la evidencia
científica internacionalmente aceptada.
La autorización será otorgada mediante resolución
por el Servicio de Salud
competente.
| NOTA: El
artículo transitorio del DTO 115, Salud, publicado el
25.11.2003, dispone que la modificaciones a este artículo,
regirán 180 días después de su publicación.
|
|
| DTO
115, SALUD
Art. primero Nº 1
D.O. 25.11.2003 |
|
Artículo 4.- Corresponderá a los Servicios de Salud
el control sanitario de los alimentos y velar por el
cumplimiento de las disposiciones relativas a esta materia
del Código Sanitario y del presente reglamento, todo ello
de acuerdo con las normas e instrucciones generales que
imparta el Ministerio de Salud.
|
|
TITULO I
Principios Generales de Higiene de los Alimentos
|
|
Párrafo I
De los establecimientos de alimentos
|
|
Artículo 5.- Establecimientos de alimentos son los
recintos en los cuales se producen, elaboran, preservan,
envasan, almacenan, distribuyen, expenden y consumen
alimentos y aditivos alimentarios.
|
|
Artículo 6.- La instalación, modificación
estructural y funcionamiento de cualquier
establecimiento de alimentos deberá contar con
autorización del Servicio de Salud correspondiente.
|
| DTO 475, SALUD
Art. Unico, N° 3
D.O. 13.01.2000 |
|
Artículo 7.- Al solicitar la autorización para la
instalación de un establecimiento, el interesado deberá
presentar, según corresponda:
a) autorización municipal de acuerdo a plano regulador;
b) plano o croquis de planta e instalaciones sanitarias a
escala de la misma;
c) croquis de los sistemas de eliminación del calor, olor
o vapor y sistema de frío;
d) descripción general de los procesos de elaboración;
e) materias primas que empleará;
f) rubros a los que se destinará;
g) sistemas de control de calidad sanitaria con que
contará;
h) tipos de alimentos que elaborará;
i) sistema de eliminación de desechos.
|
|
Artículo 8.- La autorización será válida por un
plazo de tres años contado desde su
otorgamiento y se entenderá automáticamente prorrogada por
períodos iguales y sucesivos, a menos que el propietario o
representante legal comunique su voluntad de no continuar
sus actividades o que la autoridad sanitaria la deje sin
efecto por motivos fundados, tales como: cuando el
establecimiento de alimentos hubiere cesado sus actividades
o esté siendo utilizado para un fin distinto de aquel para
el que fue autorizado, de conformidad con el artículo 12
del presente reglamento.
|
| Decreto 40, SALUD
Art. 1° N° 1
D.O. 25.04.2024 |
|
Artículo 9.- La autorización sólo podrá emitirse
previa inspección del establecimiento y la solicitud de
autorización deberá ser resuelta por el Servicio de Salud
correspondiente dentro del plazo de treinta días hábiles
contados desde que el requirente complete los antecedentes
exigidos para ello. En dicho período deberán practicarse
todas las visitas, inspecciones, análisis y otras
actuaciones o diligencias necesarias para decidir sobre su
aceptación o rechazo.
|
|
Artículo 10.- Para aquellos establecimientos que el
Ministerio de Salud determine, la autorización podrá
emitirse sin practicar una inspección previa.
|
|
Artículo 11.- Desde el inicio de su funcionamiento, el
interesado deberá aplicar las prácticas generales de
higiene en la manipulación incluyendo el cultivo, la
recolección, la preparación, la elaboración, el envasado,
el almacenamiento, el transporte, la distribución y la
venta de alimentos, con objeto de garantizar un producto
inocuo y sano.
|
|
Artículo 12.- Los establecimientos de alimentos no
podrán utilizarse para un fin distinto de aquel para el que
fueron autorizados.
|
|
Artículo 13.- La autoridad sanitaria deberá enrolar
los establecimientos y para este efecto llevará un registro
en el que se indicará el rubro o giro, su ubicación y el
nombre del propietario.
|
|
Párrafo II
Definiciones
|
|
Artículo 14.- Para los fines de este reglamento se
entenderá por:
a) adecuado: suficiente para alcanzar el fin que persigue
este reglamento;
b) contaminación: la presencia de microorganismos, virus
y/o parásitos, sustancias extrañas o deletéreas de origen
mineral, orgánico o biológico, sustancias radioactivas y/o
sustancias tóxicas en cantidades superiores a las
permitidas por las normas vigentes, o que se presuman
nocivas para la salud.
La presencia de cualquier tipo de suciedad, restos o
excrementos.
Aditivos no autorizados por la reglamentación vigente
o en cantidades superiores a las permitidas;
c) desinfección: la reducción del número de
microorganismos a un nivel que no dé lugar a contaminación
nociva del alimento, sin menoscabo de la calidad de él,
mediante agentes químicos y/o métodos higiénicamente
satisfactorios;
d) higiene de los alimentos: todas las medidas necesarias
para garantizar la inocuidad y salubridad del alimento en
todas las fases, desde su cultivo, producción,
elaboración, envasado, transporte y almacenamiento hasta el
consumo final;
e) limpieza: la eliminación de tierra, residuos de
alimentos, polvo, grasa u otra materia objetable;
f) manipulación de alimentos: todas las operaciones del
cultivo y recolección, producción, preparación,
elaboración, envasado, almacenamiento, transporte,
distribución y venta de los alimentos;
g) manipulador de alimentos: corresponde a toda persona
que trabaje a cualquier título, aunque sea ocasionalmente,
en lugares donde se produzca, manipule, elabore, almacene,
distribuya o expenda alimentos;
h) material de envasado de alimentos: todos los
recipientes, como latas, botellas, cajas de cartón u otros
materiales, fundas y sacos, o material para envolver o
cubrir, tal como papel laminado, película, papel, papel
encerado, tela;
i) plagas: insectos, roedores, pájaros y otras especies
menores capaces de contaminar directa o indirectamente los
alimentos.
j) Estructura de una instalación de
alimentos: los elementos resistentes u orgánicos de una
construcción, tales como: cimientos, muros soportantes,
tabiques que separan salas o áreas, suelos, pilares,
techumbres, torres y otros análogos que la componen.
k) Modificación estructural: todo cambio en los elementos
resistentes u orgánicos de una construcción, detallados en
el literal anterior, que afecte el proceso de elaboración
del producto o el producto terminado, en atención a lo
dispuesto en los artículos 24 y 25 del presente reglamento.
No se considerará modificación estructural las operaciones
de mantención de la estructura de instalación de
alimentos.
|
| Decreto 40, SALUD
Art. 1° N° 2
D.O. 25.04.2024 |
|
Párrafo III
De los requisitos de higiene en la zona de
producción/recolección
|
|
Artículo 15.- No se permitirá cultivar, producir o
recolectar alimentos en zonas contaminadas con agentes
potencialmente nocivos o regadas con aguas sanitariamente
inadecuadas, que puedan dar lugar a concentraciones
inaceptables de agentes contaminantes en los alimentos.
|
|
Artículo 16.- Los alimentos se deberán proteger
contra la contaminación por desechos de origen humano,
animal, doméstico, industrial y agrícola cuya presencia
pueda alcanzar niveles susceptibles de constituir riesgo
para la salud.
|
|
Artículo 17.- Se deberán tomar precauciones adecuadas
para que los desechos no se utilicen ni evacuen de manera
que puedan constituir, a través de los alimentos, un riesgo
para la salud.
|
|
Artículo 18.- El equipo y los recipientes que se
utilicen en la recolección y la producción de alimentos
deberán construirse y conservarse de manera que no
constituyan un riesgo para la salud. Los envases que se
reutilicen deberán ser de material y construcción tales
que permitan una limpieza fácil y completa. Deberán
limpiarse y mantenerse limpios y, en caso necesario,
desinfectarse. Los recipientes usados para materias tóxicas
deberán ser identificados y no podrán utilizarse para
alimentos.
|
|
Artículo 19.- Los alimentos que no son aptos para el
consumo humano deberán separarse durante la recolección y
producción y eliminarse de tal forma que no puedan dar
lugar a la contaminación de la producción, del agua o de
otras materias alimentarias.
|
|
Artículo 20.- Los productos alimenticios y/o materias
primas recolectados, se deberán almacenar en condiciones
que confieran protección contra la contaminación y
reduzcan al mínimo los daños y deterioros.
|
|
Artículo 21.- Los medios de transporte de los
productos alimenticios recolectados deberán ser de
materiales y construcción tales que permitan una limpieza
fácil y completa. Deberán limpiarse y mantenerse limpios y
en caso necesario, ser desinfectados o desinsectados con
productos que no dejen residuos tóxicos.
|
|
Párrafo IV
Del proyecto y construcción de los establecimientos
|
|
Artículo 22.- Los establecimientos deberán estar
situados en zonas alejadas de focos de insalubridad, olores
objetables, humo, polvo y otros contaminantes y no expuestos
a inundaciones.
|
|
Artículo 23.- Las vías de acceso y zonas de
circulación que se encuentren dentro del recinto del
establecimiento o en sus inmediaciones, deberán tener una
superficie dura, pavimentada o tratada de manera tal que
controlen la presencia de polvo ambiental.
|
|
Artículo 24.- Los edificios e instalaciones
deberán proyectarse de tal manera que las
operaciones puedan realizarse en las debidas condiciones
higiénicas y se garantice la fluidez del proceso de
elaboración desde la llegada de la materia prima a los
locales hasta la obtención del producto terminado,
asegurando además condiciones de temperatura apropiadas
para el proceso de elaboración y para el producto.
Los establecimientos de alimentos en que se mantengan o
almacenen materias primas alimentarias, alimentos en
proceso, alimentos terminados y envases de alimentos
deberán diseñarse de tal forma que éstos estén
protegidos de la contaminación y/o alteración.
Los establecimientos destinados a la elaboración de
alimentos, según las características del proceso, deberán
contar con las siguientes áreas:
a) Recepción, selección, limpieza y preparación de
las materias primas.
b) Producción.
c) Almacenamiento de materias primas, envases,
etiquetas, alimentos en proceso y del producto terminado.
|
| Decreto 60,
SALUD
Art. 1, N° 1
D.O. 07.07.2018 |
|
Artículo 25.- En las zonas de preparación de
alimentos:
a) los pisos, se construirán de materiales impermeables,
no absorbentes, lavables, antideslizantes y atóxicos; no
tendrán grietas y serán fáciles de limpiar. Según el
caso, se les dará una pendiente suficiente para que los
líquidos escurran hacia las bocas de los desagües;
b) las paredes, se construirán de materiales
impermeables, no absorbentes, lavables y atóxicos y serán
de color claro. Hasta una altura apropiada para las
operaciones, como mínimo 1.80 m, deberán ser lisas y sin
grietas, fáciles de limpiar y desinfectar;
c) los cielos rasos deberán proyectarse, construirse y
acabarse de manera que se impida la acumulación de suciedad
y se reduzca al mínimo la condensación de vapor de agua y
la formación de mohos y deberán ser
fáciles de limpiar;
d) las ventanas y otras aberturas deberán construirse de
manera que se evite la acumulación de suciedad, y las que
se abran deberán estar provistas de protecciones contra
vectores. Las protecciones deberán ser removibles para
facilitar su limpieza y buena conservación. Los alféizares
de las ventanas deberán estar construidos con pendiente
para evitar que se usen como estantes;
e) las puertas deberán ser de superficie lisa y no
absorbente y, cuando así proceda, deberán tener cierre
automático;
f) las escaleras, montacargas y estructuras auxiliares,
como plataformas, escaleras de mano y rampas, deberán estar
situadas y construidas de manera que no sean causa de
contaminación de los alimentos. Las rampas deberán
construirse con rejillas de inspección y deberán ser
fácilmente desmontables para su limpieza y buena
conservación;
g) todas las estructuras y accesorios elevados deberán
instalarse de manera que se evite la contaminación directa
o indirecta de alimentos y de la materia prima por
condensación de vapor de agua y goteo y no se entorpezcan
las operaciones de limpieza;
h) Los materiales de revestimiento aplicados a
las superficies de trabajo y a los
equipos que puedan entrar en contacto directo con los
alimentos, no deberán ceder sustancias tóxicas o
contaminantes a los alimentos,
modificando los caracteres organolépticos y de inocuidad.
| NOTA: El Art. segundo
del DTO 68, Salud, publicado el 23.01.2006, dispuso que la
modificación introducida al presente artículo rige a
contar de 180 días después de su publicación.
|
|
| DTO 68, SALUD
Art. primero Nº 1
D.O. 23.01.2006 |
|
Artículo 26.- La zona de preparación de alimentos
deberá estar separada de los recintos destinados a
alojamientos, servicios higiénicos, vestuarios y acopio de
desechos.
|
|
Artículo 27.- Deberá disponerse de abundante
abastecimiento de agua potable que se ajustará a lo
dispuesto en la reglamentación vigente, a presión y
temperatura conveniente, así como de instalaciones
apropiadas para su almacenamiento, distribución y con
protección contra la contaminación.
|
|
Artículo 28.- El hielo, utilizado en contacto directo
con el alimento, deberá fabricarse con agua que se ajuste a
lo dispuesto en el presente reglamento, y habrá de
tratarse, manipularse, almacenarse y utilizarse de modo que
esté protegido contra la contaminación.
|
|
Artículo 29.- El vapor de agua utilizado en contacto
directo con alimentos no deberá contener ninguna sustancia
que pueda contaminar el alimento.
|
|
Artículo 30.- El agua no potable que se utilice para
la producción de vapor, refrigeración, lucha contra
incendios y otros propósitos similares no relacionados con
los alimentos, deberá trasportarse por tuberías
completamente separadas, identificadas por colores, sin que
haya ninguna conexión transversal ni sifonado de retroceso
con las tuberías que conducen el agua potable.
|
|
Artículo 31.- Los establecimientos deberán disponer
de un sistema eficaz de evacuación de aguas residuales, el
que deberá mantenerse en buen estado de funcionamiento.
Todos los conductos de evacuación (incluidos los sistemas
de alcantarillado) deberán ser diseñados para soportar
cargas máximas y deberán construirse de manera que se
evite la contaminación del abastecimiento de agua potable.
|
|
Artículo 32: Todos los establecimientos de
producción, elaboración y transformación de
alimentos deberán disponer de vestuarios y servicios
higiénicos convenientemente situados y en número conforme
a lo dispuesto por el Reglamento Sobre Condiciones
Sanitarias y Ambientales Básicas en los Lugares de Trabajo.
Los servicios higiénicos deberán estar bien
iluminados y ventilados y no tendrán comunicación directa
con la zona donde se manipulen los alimentos. Los lavamanos
contarán con grifos para el agua fría y caliente,
provistos de jabón para lavarse las manos y medios
higiénicos para secárselas, tales como toallas de papel,
aire caliente u otros. Deberá ponerse rótulos en los que
se indique al personal la obligación de lavarse las manos
después de usar los servicios.
Las ventanas y otras aberturas deberán estar provistas
de mallas protectoras contra vectores.
|
| DTO 475, SALUD
Art. Unico, N° 5
D.O. 13.01.2000 |
|
Artículo 33.- En las zonas de elaboración deberá
disponerse de lavamanos provistos de jabón y medios
higiénicos para secarse las manos, tales como, toallas de
un solo uso o aire caliente.
|
|
Artículo 34.- Todo el establecimiento deberá tener
una iluminación natural o artificial adecuada, que no
deberá alterar los colores, y que permita la apropiada
manipulación y control de los alimentos. La iluminación no
deberá ser menor a:
540 lux en todos los puntos de inspección, 220 lux en
las salas de trabajo, 110 lux en otras zonas.
Las lámparas que estén suspendidas sobre el material
alimentario en cualquiera de las fases de producción, deben
ser de fácil limpieza y estar protegidas para evitar la
contaminación de los alimentos en caso de rotura.
|
|
Artículo 35.- Deberá proveerse una ventilación
adecuada para evitar el calor excesivo, la condensación de
vapor de agua y acumulación de polvo y para eliminar el
aire contaminado. La dirección de la corriente de aire no
deberá desplazarse de una zona sucia a una zona limpia. Las
aberturas de ventilación deberán estar provistas de
rejillas u otras protecciones de material anticorrosivo y
que puedan retirarse fácilmente para su limpieza.
|
|
Artículo 36.- Deberá disponerse de instalaciones
separadas del lugar de elaboración para el almacenamiento
de los desechos y materiales no comestibles, donde
permanecerán hasta su eliminación.
INCISO SUPRIMIDO
| NOTA:
El Art. segundo del DTO 68, Salud, publicado el
23.01.2006, dispuso que la modificación introducida al
presente artículo rige a contar de 180 días después de su
publicación.
|
|
| DTO 68, SALUD
Art. primero Nº 2
D.O.
23.01.2006 |
|
Artículo 37.- Los establecimientos de alimentos en que
se mantengan, almacenen o exhiban alimentos o materias
primas, que precisen de frío para su conservación deberán
contar con refrigeradores, vitrinas refrigeradas o cámaras
frigoríficas según corresponda, además estos equipos
deberán estar provistos de un termómetro o de un
dispositivo para el registro de su temperatura.
|
|
Párrafo V
De los requisitos de higiene de los establecimientos
|
|
Artículo 38.- Los establecimientos, sus equipos,
utensilios y demás instalaciones, incluidos los desagües,
deberán mantenerse en buen estado, limpios y ordenados.
INCISO SUPRIMIDO
| NOTA: El Art. segundo
del DTO 68, Salud, publicado el 23.01.2006, dispuso que la
modificación introducida al presente artículo rige a
contar de 180 días después de su publicación.
|
|
| DTO 68, SALUD
Art. primero Nº 3
D.O. 23.01.2006 |
|
Artículo 39.-Los desechos deberán retirarse de las
zonas de manipulación y otras zonas de trabajo, cuantas
veces sea necesario y por lo menos una vez al día.
|
|
Artículo 40.- Se deberá impedir el acceso de las
plagas a los desechos. Inmediatamente después de su
evacuación, los receptáculos utilizados para el
almacenamiento y todo el equipo que haya entrado en contacto
con los desechos deberán limpiarse. La zona de
almacenamiento de desechos deberá, asimismo, mantenerse
limpia.
|
|
Artículo 41.- Todo establecimiento de
producción, elaboración y transformación de
alimentos deberá establecer un programa de limpieza y, de
ser necesario, de desinfección, a fin de asegurar que todas
las partes de la instalación presenten una adecuada
limpieza, de la forma como señala la letra a) del artículo
14 de este reglamento. Dicho programa deberá especificar
superficies, elementos del o los equipos y utensilios que
han de limpiarse; responsabilidad de tareas particulares;
métodos y frecuencia de la limpieza; medidas de vigilancia
de la misma y, de ser necesario, de la desinfección, para
asegurar su idoneidad y eficacia. La necesidad de
desinfección de superficies, elementos del equipo y
utensilios se deberá evaluar de acuerdo a las materias
primas, condición de éstas, procesos, productos y peligros
que estén asociados a los mismos o que, razonablemente, se
presuma que puedan estarlo.
Todo el personal de aseo deberá estar capacitado en
técnicas de limpieza y desinfección, según corresponda a
los procedimientos aplicados en la instalación. Se deberán
mantener registros de las capacitaciones realizadas
|
| Decreto 75, SALUD
Art. 1 N° 1
D.O. 12.11.2019 |
|
Artículo 42.- Para impedir la contaminación de los
alimentos, todo el equipo y utensilios deberán mantenerse
debidamente protegidos en estantes, vitrinas, u otros,
después de limpiarse y desinfectarse.
|
|
Artículo 43.- Deberán tomarse precauciones adecuadas
para impedir que el alimento se contamine cuando las salas,
el equipo y los utensilios se limpien o desinfecten con agua
y detergentes o con desinfectantes o soluciones de éstos.
Los desinfectantes deberán ser apropiados al fin
perseguido, debiendo eliminarse cualquier residuo de modo
que no haya posibilidad de contaminación de los alimentos.
|
|
Artículo 44.- Inmediatamente después de terminar el
trabajo de la jornada o cuantas veces sea necesario,
deberán limpiarse minuciosamente los pisos, incluidos los
desagües, las estructuras auxiliares y las paredes de la
zona de manipulación de alimentos.
|
|
Artículo 45.- Las salas de vestuario, servicios
higiénicos, vías de acceso y los patios situados en las
inmediaciones de los locales y que sean partes de éstos,
deberán mantenerse limpios.
|
|
Artículo 46.- Se prohíbe la entrada a las salas
y áreas de elaboración de los
establecimientos de alimentos de toda especie animal,
excepto en los mataderos, de aquellas destinadas al
faenamiento.
| NOTA: El Art. segundo
del DTO 68, Salud, publicado el 23.01.2006, dispuso que la
modificación introducida al presente artículo rige a
contar de 180 días después de su publicación.
|
|
| DTO 68, SALUD
Art. primero Nº 4
D.O. 23.01.2006 |
|
Artículo 47.- Deberá aplicarse un programa
preventivo eficaz y continuo de lucha contra las
plagas. Los establecimientos y las zonas circundantes
deberán inspeccionarse periódicamente para cerciorarse de
que no exista infestación.
|
| DTO 475, SALUD
Art. Unico, N° 7
D.O. 13.01.2000 |
|
Artículo 48.- En caso que alguna plaga invada los
establecimientos deberán adoptarse medidas de
erradicación. El tratamiento con agentes químicos,
físicos o biológicos sólo deberá aplicarse de acuerdo a
la reglamentación vigente, por empresas autorizadas para
tales efectos por la autoridad sanitaria correspondiente.
|
|
Artículo 49.- Sólo deberá emplearse plaguicidas si
no pueden aplicarse con eficacia otras medidas de
prevención. Antes de aplicar plaguicidas se deberá tener
cuidado de proteger todos los alimentos, equipos y
utensilios contra la contaminación. Después de aplicar los
plaguicidas y a fin de eliminar los residuos, estos equipos
y utensilios se deberán limpiar minuciosamente antes de
volverlos a usar.
|
|
Artículo 50.- Se prohíbe la mantención de
plaguicidas u otras sustancias tóxicas que puedan
representar un riesgo para la salud, en las zonas de
producción, elaboración, transformación, envase y
almacenamiento de alimentos.
|
|
Artículo 51.- En las zonas de manipulación
de alimentos se prohíbe almacenar
sustancias que puedan contaminar los alimentos ni depositar
o guardar en ellas ropa u otros objetos personales.
|
| Decreto 60,
SALUD
Art. 1, N° 2
D.O. 07.07.2018 |
|
Párrafo VI
De los requisitos de higiene del personal
|
|
Artículo 52.- La dirección del establecimiento
será responsable de que todas las personas
que manipulen alimentos reciban una instrucción adecuada y
continua en materia de manipulación higiénica de los
mismos e higiene personal. Se deberán mantener registros de
tales instrucciones, su calendarización, programas, listas
de asistencia y evaluaciones, si corresponde.
|
| Decreto 75, SALUD
Art. 1 N° 2
D.O. 12.11.2019 |
|
Artículo 53.- La empresa tomará las medidas
necesarias para evitar que el personal que padece o es
portador de una enfermedad susceptible de transmitirse por
los alimentos, o tenga heridas infectadas, infecciones
cutáneas, llagas o diarrea, trabaje en las zonas de
manipulación de alimentos en las que haya probabilidad que
pueda contaminar directa o indirectamente a éstos con
microorganismos patógenos. Toda persona que se encuentre en
esas condiciones debe comunicar inmediatamente al supervisor
su estado de salud.
|
|
Artículo 54.- INCISO ELIMINADO El personal que manipule
alimentos no deberá atender pagos del público, sea
recibiendo o entregando dinero, no deberá realizar tareas
que puedan contaminar sus manos y ropas de trabajo.
|
| DTO 79, SALUD
Nº 1
D.O. 24.06.2003 |
|
Artículo 55.- El personal que manipula
alimentos deberá lavarse siempre las manos
cuando su nivel de limpieza pueda afectar la inocuidad de
los alimentos, antes de iniciar el trabajo, inmediatamente
después de haber hecho uso de los servicios higiénicos,
después de manipular material contaminado y todas las veces
que sea necesario.
|
| Decreto 31, SALUD
Art. 1 N° 1
D.O. 28.10.2017 |
|
Artículo 56.- Los manipuladores deberán mantener una
esmerada limpieza personal mientras estén en funciones
debiendo llevar ropa protectora, tal como: cofia o gorro que
cubra la totalidad del cabello, y delantal. Estos artículos
deben ser lavables, a menos que sean desechables y
mantenerse limpios. Este personal no debe usar objetos de
adorno en las manos cuando manipule alimentos y deberá mantener
las uñas de las manos cortas, limpias y sin barniz.
|
| DTO 475, SALUD
Art. Unico, N° 8
D.O. 13.01.2000 |
|
Artículo 57.- En las zonas en que se manipulen
alimentos deberá prohibirse todo acto que pueda contaminar
los alimentos, como: comer, fumar, masticar chicle, o
realizar otras prácticas antihigiénicas, tales como
escupir.
|
|
Artículo 58.- Si para manipular los alimentos se
emplean guantes, éstos se mantendrán en perfectas
condiciones de limpieza e higiene. El uso de guantes no
eximirá al operario de la obligación de lavarse las manos
cuidadosamente.
|
|
Artículo 59.- Se deberá evitar la presencia de
personas extrañas en las salas donde se manipulen
alimentos. En la eventualidad que esto suceda se tomarán
las precauciones para impedir que éstas contaminen los
alimentos. Las precauciones deben incluir el uso de ropas
protectoras.
|
|
Artículo 60.- La responsabilidad del cumplimiento por
parte del personal de todos los requisitos señalados en
este párrafo, deberá asignarse al personal supervisor
competente, sin que ello implique exclusión de esta
responsabilidad a los propietarios del establecimiento.
|
|
Párrafo VII
De los requisitos de higiene en la elaboración de los
alimentos
|
|
Artículo 61.- En la elaboración sólo deberán
utilizarse materias primas e ingredientes en buen estado de
conservación, debidamente identificados, exentos de
microorganismos o sustancias tóxicas en cantidades
superiores a las aceptadas en este reglamento u otras
materias extrañas.
|
|
Artículo 62.- Las materias primas,
ingredientes, alimentos en proceso y envases
almacenados en los locales del establecimiento deberán
mantenerse en condiciones que eviten su deterioro y
contaminación, considerando aspectos tales como: naturaleza
del producto, infraestructura, características de los
envases, tratamientos térmicos o de preservación a que
serán sometidos.
|
| Decreto 60,
SALUD
Art. 1, N° 3
D.O. 07.07.2018 |
|
Artículo 63.- El flujo del personal, vehículos y de
materias primas en las distintas etapas del proceso, debe
ser ordenado y conocido por todos los que participen en la
elaboración, para evitar contaminación cruzada.
|
|
Artículo 64.- Todo el equipo que haya entrado en
contacto con materias primas o con material contaminado
deberá limpiarse, desinfectarse y verificarse el grado de
limpieza antes de entrar en contacto con productos
terminados.
|
|
Artículo 65.- En la manipulación de los alimentos
sólo deberá utilizarse agua de calidad potable.
|
|
Artículo 66.- Deberán existir registros de
producción, distribución y control de los
alimentos y materias primas y conservarse, como mínimo,
durante 90 días posteriores a la fecha de vencimiento o
plazo de duración del producto. Los alimentos de duración
indefinida deberán mantener el registro, al menos, durante
tres años.
En el registro deberá identificarse la procedencia del
alimento y/o materia prima, como etapa anterior, y el
destino del producto, como etapa posterior.
|
| Decreto 4,
SALUD
Art. 1 Nº 1
D.O. 09.01.2013 |
|
Artículo 67.- Los productos terminados deberán
almacenarse y transportarse en condiciones adecuadas de
temperatura y humedad que garantice su aptitud para el
consumo humano.
|
|
Artículo 68.- El transporte de alimentos
perecibles que requieren frío para su
conservación en estado fresco, enfriado y/o congelado,
sólo podrá realizarse en vehículos o medios de transporte
con carrocera cerrada, con
equipos capaces de mantener la temperatura requerida según
el tipo de producto y lo establecido en este reglamento,
provistos de termómetros que permitan su lectura desde el
exterior y deberán mantenerse en todo momento en perfectas
condiciones de higiene y limpieza.
Además, deberán contar con autorización sanitaria
otorgada por la autoridad sanitaria en cuyo territoro de
competencia registre el domicilio el propietario o su
representante legal. Esta autorización será válida por un
plazo de tres años contados desde la fecha de su
otorgamiento.
| NOTA: El artículo
transitorio del DTO 45, Salud, publicado el 12.07.2006,
dispone que la sustitución de la presente norma, rige 12
meses después de su publicación.
|
|
| DTO 45, SALUD
Art. único Nº 1
D.O. 12.07.2006 |
|
Artículo 69.- Los establecimientos de
producción, elaboración, preservación y envase
de alimentos deberán cumplir con las Buenas Prácticas de
Fabricación (BPF) mencionadas en este reglamento, en forma
sistematizada y auditable.
Además, aquellos que la autoridad sanitaria determine
dentro de su correspondiente área de competencia, según
los criterios establecidos por resolución del Ministerio de
Salud, deberán implementar las metodologías de Análisis
de Peligros y Puntos Críticos de Control (HACCP), en toda
su línea de producción, conforme lo establecido en la
Norma Técnica que, para tales efectos, dicte ese mismo
Ministerio.
|
| DTO 45, SALUD
Art. único Nº 2
D.O. 12.07.2006 |
| Decreto 126, SALUD
Art. 1
D.O. 20.11.2014 |
|
Artículo 70.- Los procedimientos de laboratorio
utilizados en el control de calidad, deberán ajustarse a
métodos normalizados y reconocidos por organismos oficiales
nacionales e internacionales, con el fin de que los
resultados puedan ser comparables y reproducibles.
|
|
Párrafo VIII
De los requisitos de higiene en el expendio
|
|
Artículo 71.- En los establecimientos donde se
expendan alimentos que necesitan conservarse a baja
temperatura, se deberá contar con sistemas de frío que
aseguren las características propias del producto, los que
deberán mantenerse de acuerdo a las recomendaciones
técnicas de los fabricantes.
Asimismo, los establecimientos donde se
expendan alimentos a granel de alto riesgo de
contaminación, tales como productos lácteos, productos
cárnicos, productos congelados y encurtidos, entre otros,
deberán contar con vitrinas que permitan conservar este
tipo de alimentos, de acuerdo a sus características y a las
recomendaciones del fabricante y su diseño será tal que
impida el autoservicio por parte del público.
El fraccionamiento y expendio de los alimentos
señalados en el inciso anterior, deberá ser realizado por
un manipulador de alimentos, especificamente destacado para
tales efectos.
Los productos alimenticios de venta a granel expuestos
en vitrina deberán exhibir la identificación del
fabricante o productor.
En los establecimientos deberán mantenerse los
antecedentes de origen y fechas de elaboración y
vencimiento de los productos sujetos a este tipo de
comercialización, de manera tal que, estén disponibles
para la autoridad sanitaria cuando ésta lo requiera.
El almacenamiento de alimentos en
establecimientos destinados al expendio deberá realizarse
de modo de mantener los productos protegidos de la
contaminación y/o alteración conforme a las
características de los alimentos que se expenden.
|
| DTO 475, SALUD
Art. Unico, N° 10
D.O. 13.01.2000 |
| Decreto 60,
SALUD
Art. 1, N° 4
D.O. 07.07.2018 |
|
Artículo 72.- Tanto el local como los equipos,
superficies de trabajo y utensilios deberán mantenerse en
perfectas condiciones de limpieza. La vajilla, cubiertos y
cristalería, después de lavados con agua corriente y
jabón u otro detergente, deben ser tratados con agua
caliente y/o vapor de agua por dos minutos y sumergidos por
veinte segundos, por lo menos, en una solución que contenga
sesenta partes por millón de cloro libre, con posterior
enjuague con agua corriente. Donde no se desinfecten los
vasos, copas y tazas, será obligatorio el empleo de
utensilios de único uso y de material autorizado. No se
permite el uso de vajilla, platos, vasos, copas y tazas que
presenten trizaduras o bordes rotos.
|
|
Artículo 73.- Los locales donde se expenden alimentos
para su consumo en el mismo establecimiento deberán contar
además de lo dispuesto en el artículo 32 de este
reglamento, con servicios higiénicos gratuitos para uso del público, separados para
cada sexo, los que deberán mantenerse en todo momento en
perfectas condiciones de higiene, limpieza y ventilación.
Deberán estar dotados de papel
higiénico en cantidad necesaria para el uso de los
excusados, dispositivos de jabón líquido para el lavado de
manos y de medios higiénicos para secárselas, tales como
toallas de papel o aire caliente.
Se exceptúa de esta obligación a los locales "al
paso", los cuales sólo expenderán comida lista para llevar
y/o atenderán público en la barra.
| NOTA: El Art.
transitorio del DTO 214, Salud, publicado el 04.02.2006,
dispuso que la modificación introducida al presente
artículo rige a contar de 180 días desde su publicación.
|
|
| DTO
214, SALUD
Art. primero I Nº1
D.O. 04.02.2006 |
|
Artículo 74.- Los puestos emplazados en ferias
libres, como también los quioscos, casetas y
carros que carezcan de conexiones a las redes de agua
potable, alcantarillado y los vendedores ambulantes, sólo
podrán expender:
a) alimentos y bebidas envasados que provengan de
fábricas autorizadas, que no requieran de protección del
frío o del calor. Las bebidas serán vendidas en su envase
original o de máquinas expendedoras que utilicen bases de
premezclas;
b) frutas enteras, verduras, semillas y otros alimentos
similares. Estos alimentos deberán almacenarse en buenas
condiciones sanitarias;
c) algodón de azúcar, infusiones de té o café, en
vasos desechables desde depósitos térmicos sellados, que
provengan de establecimientos autorizados, y helados
envasados que provengan, asimismo, de establecimientos
autorizados;
d) pescados, mariscos y productos del mar, y
carnes de especies de abasto, de aves y los
subproductos comestibles de todas estas especies, siempre y
cuando dichos establecimientos reúnan los siguientes
requisitos:
- disponer de un sistema de agua corriente con un
estanque que deberá abastecerse con al menos 150 litros de
agua potable, al inicio de cada jornada y cada vez que sea
necesario;
- disponer de un estanque hermético de
recepción de las aguas utilizadas, cuya
capacidad sea igual o mayor a la del estanque de agua
limpia;
- disponer de un sistema de frío, que
permita mantener a temperatura
de refrigeración (0° C -
5° C), los productos alimenticios antes señalados,
durante toda la jornada de trabajo de la feria.
e) Hielo granizado saborizado con jarabes naturales
o artificiales, en la medida que se cumplan los siguientes
requisitos:
- Ser elaborado en máquinas granizadoras especialmente
diseñadas para tales efectos y que, por sus
características de funcionamiento, el alimento no sea
objeto de manipulación directa.
- Utilizar hielo y jarabes que provengan de
establecimientos autorizados.
- Utilizar cucharas o bombillas y vasos desechables.
- Disponer de un sistema o material de almacenamiento,
transporte y expendio que permita mantener una temperatura,
para la conservación del hielo, de 0 ºC o menos durante la
jornada de trabajo.
- Preservar los insumos en condiciones que impidan su
contaminación
f) Quesos y cecinas provenientes de fábricas
autorizadas, fraccionados y envasados en las mismas
fábricas, siempre y cuando dichos puestos de venta
dispongan de un sistema de frío que permita mantener a
temperatura de refrigeración (máximo 5º C) los productos
alimenticios antes señalados. En el caso de cecinas crudas
maduradas, éstas podrán mantenerse sin refrigeración,
pero en lugar seco y fresco (máximo 12º C). Queda
prohibido el fraccionamiento de los alimentos anteriormente
mencionados en tales puestos
g) Frutas y verduras frescas lavadas, trozadas o
peladas y envasadas provenientes de establecimientos
autorizados para dichos fines, siempre que dichos puestos de
venta dispongan de un sistema de frío que permita mantener
a temperatura de refrigeración (máximo 5° C) los
productos alimenticios antes señalados. Los envases
deberán cubrir totalmente los alimentos y constituir una
barrera eficaz contra la contaminación.
Las implementaciones exigidas precedentemente para la
comercialización de los productos alimenticios señalados en la letra d)
deberán mantenerse en perfectas condiciones, en forma
permanente.
| NOTA: El Art.
transitorio del DTO 214, Salud, publicado el 04.02.2006,
dispuso que las modificaciones introducidas al presente
artículo rigen a contar de 180 días desde su publicación.
|
|
| DTO 214, SALUD
Art. primero I Nº2
D.O. 04.02.2006 |
| DTO 37, SALUD
Art. 1º Nº 1
D.O. 05.05.2004 |
| DTO 214, SALUD
Art. primero I Nº2
D.O. 04.02.2006 |
| Decreto 24, SALUD
Art. 1 Nº 1
D.O. 19.11.2013 |
| Decreto 118, SALUD
Art. 1 N° 1
D.O. 07.10.2014 |
| Decreto 11, SALUD
Art. 1 N° 1
D.O. 06.06.2016 |
| DTO 37, SALUD
Art. 1º Nº 1
D.O. 05.05.2004 |
|
Artículo 74 a.- Los quioscos, casetas y carros
podrán elaborar y expender fruta fresca
confitada, frutos secos confitados, palomitas de maíz y
algodón de azúcar, bajo las siguientes
condiciones:
a) Instalación de material sólido, lavable, de tamaño
suficiente y con toldo o techo para protegerse de las
condiciones climáticas.
b) Disponer de un depósito o contenedor, lavable y con
tapa, que asegure la protección de las materias primas.
c) Los cilindros de gas deberán estar instalados y ser
utilizados cumpliendo con las medidas de seguridad que
garanticen la salud del trabajador y la comunidad, conforme
a las disposiciones de la autoridad competente.
| NOTA: El Art.
transitorio del DTO 214, Salud, publicado el 04.02.2006,
dispuso que la modificación introducida al presente
artículo rige a contar de 180 días desde su publicación.
|
|
| DTO 214, SALUD
Art. primero I Nº3
D.O. 04.02.2006 |
|
Artículo 74 b.- Los quioscos, casetas y carros
podrán freír, hornear y expender: masas sin
relleno, empanadas de queso y productos vegetales. Asimismo,
podrán expender frutas y verduras frescas lavadas, trozadas
o peladas y demás vegetales procesados y envasados
provenientes de establecimientos autorizados para dichos
fines. Además, de elaborar y expender infusiones de té,
café y demás estimulantes y fruitivos, emparedados fríos
y calientes a base de cecinas cocidas, cumpliendo los
siguientes requisitos:
a) Carro o soporte físico de la instalación de material
sólido, lavable, de tamaño suficiente. y deberá contar
con una estructura protegida que delimite el espacio de
manipulación de alimentos.
b) Disponer de un sistema de agua potable corriente
mediante un estanque con capacidad de provisión mínima de
100 litros, que permita su reabastecimiento cada vez que sea
necesario, y que asegure el correcto lavado de manos y
utensilios que se utilicen. Para el lavado de manos deberá
contarse con lavamanos, jabón y toallas de papel
desechables como único sistema de secado.
c) Disponer de un estanque hermético de recepción de las
aguas utilizadas, cuya capacidad sea mayor a las del
estanque de agua limpia.
d) Disponer de un sistema de frío que permita mantener la
temperatura de refrigeración, de las masas, vegetales
procesados y cecinas, entre 0° y 5° C y de un dispositivo
para el control permanente de la temperatura.
e) Disponer de un depósito o contenedor para las materias
primas que no requieran refrigeración que asegure
mantenerlas protegidas y aisladas del medio ambiente
f) Los aceites o mantecas utilizados en frituras deberán
cumplir lo establecido en el Título X, párrafo V del
presente Reglamento.
g) Disponer de un depósito lavable con tapa para la
acumulación de desperdicios, los que deberán ser retirados
y eliminados cuantas veces sea necesario y por lo menos una
vez al día.
h) Los cilindros de gas deberán estar instalados y ser
utilizados cumpliendo con las medidas de seguridad que
garanticen la salud del trabajador y la comunidad, conforme
a las disposiciones de la autoridad competente.
i) Contar con acceso a servicios higiénicos a 75 metros
de distancia como máximo.
j) Los carros, quioscos y casetas que no cuenten con
estructura protegida deberán poseer un toldo y sólo
podrán expender emparedados a base de cecinas cocidas, las
cuales se deberán mantener debidamente refrigeradas y para
su expendio sólo se podrán calentar a través de un
sistema aislado del medio ambiente.
Todas las materias primas utilizadas deberán provenir
de establecimientos autorizados. Los aderezos y salsas,
además, deberán expenderse en envases unitarios sellados y
rotulados para asegurar su inocuidad y evitar la
contaminación cruzada. Sólo se permitirá la elaboración
y expendio de aderezos a base de vegetales (tomate, palta)
en aquellos quioscos o carros que cuenten estructura
cerrada, estos aderezos deberán mantenerse en
refrigeración y en recipientes cerrados y no podrán ser de
acceso directo de los consumidores.
Los manipuladores de alimentos deberán dar
cumplimiento a las medidas estipuladas en el Título I
Párrafo VI. "De los requisitos de higiene del personal",
del presente reglamento.
Para otorgar la autorización la autoridad sanitaria
deberá disponer de los antecedentes que acrediten que el
lugar en que se ubicará el quiosco, carro o caseta está
determinado para tales efectos por la autoridad comunal
correspondiente.
|
| Decreto 11, SALUD
Art. 1 N° 2
D.O. 06.06.2016 |
|
Artículo 75.- Se permite la venta de la bebida
tradicional "Mote con Huesillos" provenientes de establecimientos autorizados en
carros móviles especialmente diseñados para tales efectos,
los cuales tendrán una vitrina para el mote y dispondrán
de un doble estanque para el jugo y además de cucharas y
vasos desechables. Deberán contar con depósitos con tapa
para la acumulación y posterior eliminación de
desperdicios.
Se permite la venta de jugos de frutas cítricas
en carros móviles especialmente diseñados para tales
efectos, los cuales tendrán, formando parte de su
estructura, un estanque para el agua potable con capacidad
mínima de 30 litros, un lavamanos, un receptáculo para el
agua utilizada con una capacidad igual o superior a la del
estanque de agua potable, una vitrina para la fruta, un
depósito con tapa para la acumulación y posterior
eliminación de los desperdicios, un sistema de extracción
del jugo de frutas por prensado, un dispensador de vasos y
bombillas desechables. Para el lavado de las superficies, se
deberá disponer de un sistema de aplicación de agua y
detergente por aspersión y de secado con toallas
desechables. La materia prima deberá estar lavada y
almacenada en buenas condiciones sanitarias. La elaboración
del jugo deberá hacerse a pedido y en presencia del
comprador. No se permite la adición de agua, hielo u otro
ingrediente al producto final. Además, deberán cumplir con
lo dispuesto en la letra i) del artículo 74b.
|
| DTO
475, SALUD
Art. Unico, N° 12
D.O. 13.01.2000 |
| Decreto 118, SALUD
Art. 1 N° 2
D.O. 07.10.2014 |
|
Párrafo IX
De los requisitos de higiene de los mataderos
|
|
Artículo 76.- Los mataderos de aves y otras especies
distintas del ganado, deberán estar ubicados en un sector
permitido por el respectivo plano regulador y estar
emplazados en un terreno normalmente no inundable y alejado
de cualquier foco de insalubridad ambiental.
|
|
Artículo 77.- Los mataderos de ganado se rigen por
lo establecido en el Reglamento sobre
estructura y funcionamiento de mataderos, establecimientos
frigoríficos, cámaras frigoríficas y plantas de desposte
y fija equipamiento mínimo de tales establecimientos,
aprobado por decreto supremo Nº 94, de 2008, de los
Ministerios de Agricultura y de Salud.
|
| Decreto 83, SALUD
Art. 1 N° 1
D.O. 25.06.2010 |
|
Artículo 78.- Mataderos son aquellos establecimientos
donde se sacrifican y faenan reses, aves y otras especies
animales destinadas a la alimentación humana. Deberán
estar habilitados de tal forma que aseguren el faenamiento y
preservación higiénica de las carnes.
|
|
Artículo 79.- Los mataderos de aves y otras especies
distintas del ganado, deberán contar al menos con las
siguientes dependencias: área destinada al lavado y
desinfección del transporte de especies vivas, área de
descarga, área de sacrificio, área de escaldado y
desplumado cuando corresponda, área de eviscerado, área de
enfriado y empaque, área de producto trozado, cámaras
frigoríficas, área de lavado y desinfección de transporte
de especies faenadas y área de despacho.
|
|
Artículo 80.- Los mataderos, a que se refiere el
artículo 76 cuando corresponda, deberán disponer de
secciones para el procesamiento de subproductos, aisladas de
la línea de faena.
Además deberán disponer de un área para el sistema
de tratamiento o destrucción de decomisos la que deberá
estar separada del área de faenamiento.
|
|
Artículo 81.- Se prohíbe el sacrificio y el faenamiento de animales destinados a
la alimentación humana en locales o recintos no autorizados
por la autoridad sanitaria.
No se permitirá la presencia dentro de la sala de
faenamiento de personas ajenas a las tareas propias del
matadero, la mantención de otros animales que no estén
destinados al sacrificio, ni la salida o retiro de animales
vivos del recinto, salvo circunstancias excepcionales,
debidamente calificadas por la autoridad sanitaria.
|
| DTO
475, SALUD
Art. Unico, N° 13
D.O. 13.01.2000 |
| Decreto 83, SALUD
Art. 1 N° 2
D.O. 25.06.2010 |
|
Párrafo X
De los requisitos de la inspección de los animales y sus
carnes
|
|
Artículo 82.- La encierra de las reses
deberá efectuarse por un período de tiempo
de antelación al sacrificio, con el fin de permitir el
reposo y el examen ante-mortem.
|
| Decreto 83, SALUD
Art. 1 N° 3
D.O. 25.06.2010 |
|
Artículo 83.- Todas las especies de reses, aves y
otras especies animales destinadas al sacrificio serán
sometidas a inspección médico-veterinaria por la autoridad
de salud o por terceros en quienes ésta delegue sus
funciones.
La inspección médico-veterinaria comprenderá, la
inspección de las especies vivas (examen ante-mortem), la
inspección de la canal, cabeza y vísceras (inspección
post-mortem) y la supervisión de la disposición final de
los animales o partes declarados no aptos para el consumo
humano.
La supervisión de la higiene de la carne, con
inclusión de la inspección de la carne, estará bajo la
responsabilidad de un médico veterinario inspector oficial.
Las técnicas de inspección y el dictamen final
respecto de la aptitud para el consumo de las carnes y
subproductos, se efectuarán de acuerdo a las normas que
para tales efectos dicte el Ministerio de Salud.
Los mataderos deberán contar además, con los
instrumentos necesarios para la detección de triquina y
otros parásitos.
|
|
Artículo 84.- La sangría, faenamiento y movilización
interna de aves y de otras especies distintas de ganado, se
hará en suspensión y los ganchos que soportan directamente
la canal deben ser de acero inoxidable. Estas carnes en
suspensión no deberán contactar con el piso o las paredes
de las dependencias.
|
|
Artículo 85.- Todos los animales enfermos que se
detecten en el examen ante-mortem, serán enviados a un
corral especialmente habilitado para ello, el que se
encontrará aislado de los otros corrales. El destino final
de estos animales se realizará de acuerdo a la normativa
vigente.
|
|
Artículo 86.- Los órganos, partes o especies
enteras no aptas para el consumo humano, de
las especies de abasto deberán ser destruidos o sometidos a
tratamientos aprobados por la autoridad sanitaria, con el
fin exclusivo de destinarlos al uso industrial no
alimentario humano. Estas operaciones deberán realizarse en
el recinto especialmente habilitado para ello, bajo la
vigilancia y responsabilidad directa del médico
veterinario, inspector de carnes.
Excepcionalmente la autoridad sanitaria podrá autorizar el retiro de estos
productos de los establecimientos donde se faenen animales,
con el fin exclusivo de su utilización en prácticas
docentes o de investigación científica, a cuyo efecto
requerirá los antecedentes que den cuenta de su identidad,
condiciones de bioseguridad, de transporte, conservación,
manejo y destino final y eventual destrucción posterior.
|
| DTO 475, SALUD
Art. Unico, N° 14
D.O. 13.01.2000 |
| DTO
214, SALUD
Art. primero I Nº 4
D.O. 04.02.2006 |
|
Artículo 87.- Los establecimientos señalados en
el artículo 76 y los mataderos de reses
deberán mantener un registro diario de la procedencia de
los animales y de las canales, partes y órganos declarados
no aptos para el consumo humano, indicando las causas de
inaptitud.
|
| DTO 475, SALUD
Art. Unico, N° 15
D.O. 13.01.2000 |
|
Párrafo XI
De los requisitos de higiene de las salas de desosado de
aves y otras especies distintas del ganado
|
|
Artículo 88.- Establecimiento o sala de desosado es
aquel recinto donde se desosan y/o trozan aves y otras
especies distintas del ganado, destinadas a la alimentación
humana.
Deberán contar con una sala para realizar el desosado,
la preparación de cortes y preempaque y una sala para
operaciones de empaque.
|
|
Artículo 89.- Las salas destinadas a las labores de
desosado, trozado, empaque y pesaje deberán disponer de un
dispositivo de enfriamiento que permita mantener
una temperatura no superior a 12ºC y un
sistema de registro permanente de
temperatura.
| NOTA:
El Art. segundo del DTO 68, Salud, publicado el
23.01.2006, dispuso que la modificación introducida al
presente artículo rige a contar de 180 días después de su
publicación.
|
|
| DTO 68, SALUD
Art. primero Nº 5
D.O. 23.01.2006 |
|
Artículo 90.- El traslado del producto obtenido en las
salas de desosado debe realizarse exclusivamente en cajas o
contenedores que garanticen la calidad higiénica del
producto y que impidan su contaminación por agentes
externos o del propio envase.
|
|
Artículo 91.- Empacadora de carne de ave u otras
especies es el establecimiento destinado al envasado de
carnes. Incluirá recepción, cámara frigorífica, cámara
de trozado, sección de almacenamiento de cajas y sección
para despuntes y huesos.
INCISO DEROGADO
| NOTA: El artículo
transitorio del DTO 115, Salud, publicado el 25.11.2003,
dispone que la modificaciones a este artículo, regirán 180
días después de su publicación.
|
|
| DTO 115, SALUD
Art. primero Nº 2
D.O. 25.11.2003 |
|
Párrafo XII
De los requisitos de higiene del transporte y
expendio de leches crudas
|
| DTO 214, SALUD
Art. primero II
Nos. 1 y 2
D.O. 04.02.2006 |
|
Artículo 92.- El transporte de leches crudas deberá
realizarse en envases destinados exclusivamente a este fin.
Deberán ser de material inerte que permita su fácil lavado
y desinfección antes y después de su uso. Sus tapas
estarán ajustadas, sin accesorios destinados a corregir
deficiencias del ajuste.
| NOTA: El Art.
transitorio del DTO 214, Salud, publicado el 04.02.2006,
dispuso que las modificaciones introducidas al presente
artículo rigen a contar de 180 días desde su publicación.
|
|
|
Artículo 93.- Se prohíbe el transporte de leches o
sus envases vacíos junto a animales,
detergentes, desinfectantes, pesticidas, combustibles u
otras sustancias químicas que signifiquen riesgo
sanitario.
| NOTA: El Art.
transitorio del DTO 214, Salud, publicado el 04.02.2006,
dispuso que la modificación introducida al presente
artículo rige a contar de 180 días desde su publicación.
|
|
| DTO 214, SALUD
Art. primero II Nº3
D.O. 04.02.2006 |
|
Artículo 94.- Cuando los productores expendan
leche directamente al público, deben
cumplir los siguientes requisitos:
a) contar con un local de ventas autorizado;
b) mantener las leches enfriadas a temperaturas inferiores a 4°C; c) expender las
leches dentro de las ocho horas siguientes a la
ordeña.
| NOTA: El Art.
transitorio del DTO 214, Salud, publicado el 04.02.2006,
dispuso que las modificaciones introducidas al presente
artículo rigen a contar de 180 días desde su publicación.
|
|
| Decreto 71, SALUD
Art. 1 N° 1
D.O. 06.03.2019 |
| DTO
214, SALUD
Art. primero II Nº4
D.O. 04.02.2006 |
|
TITULO II
De los alimentos
|
|
Párrafo I
Disposiciones generales
|
|
Artículo 95.- Para los efectos de la aplicación del
presente Reglamento, la responsabilidad derivada de las
actividades de producción, importación, envase y
comercialización de alimentos corresponderá individual o
conjuntamente, según determine el Servicio de Salud
competente, al productor, importador, envasador,
distribuidor, vendedor o tenedor del producto.
|
|
Artículo 96.- Se prohíbe la fabricación, tenencia,
distribución, comercialización o transferencia de
alimentos elaborados o envasados en el país que, aun siendo
destinados a la exportación, provengan de establecimientos
que no hayan sido autorizados por la autoridad de salud
competente.
|
|
Artículo 97.- Los alimentos de exportación que no
cumplan con las normas establecidas en el presente
Reglamento deberán llevar impreso en su envase y en forma
destacada e indeleble, la clave "Z". Estos alimentos no
podrán ser comercializados en el país.
|
|
Artículo 98.- Alimento alterado es aquel que por
causas naturales de índole física, química o biológica,
o por causas derivadas de tratamientos tecnológicos,
aisladas o combinadas, ha sufrido modificación o deterioro
en sus características organolépticas, en composición y/o
su valor nutritivo.
|
|
Artículo 99.- Alimento adulterado es aquel que
ha experimentado por intervención del
hombre, cambios que le modifican sus características o
cualidades propias sin que se declaren expresamente en el
rótulo, tales como:
a) la extracción parcial o total de cualquiera de los
componentes del producto original;
b) la sustitución parcial o total de cualquiera de los
componentes del producto original por otros inertes o
extraños, incluida la adición de agua u otro material de
relleno;
c) la mezcla, coloración, pulverización o encubrimiento,
en tal forma que se oculte su inferioridad o disminuya su
pureza.
|
| DTO 475, SLAUD
Art. Unico, N° 16
D.O. 13.01.2000 |
|
Artículo 100.- Alimento falsificado es aquel que:
a) se designe, rotule o expenda con nombre o calificativo
que no corresponda a su origen, identidad, valor nutritivo o
estimulante; y
b) cuyo envase, rótulo o anuncio, contenga cualquier
diseño o declaración ambigua, falsa o que pueda inducir a
error, respecto a los ingredientes que componen el alimento.
|
|
Artículo 101.- Alimento contaminado es aquel que
contenga:
a) microorganismos, virus y/o parásitos, sustancias
extrañas o deletéreas de origen mineral, orgánico o
biológico, sustancias radioactivas y/o sustancias tóxicas
en cantidades superiores a las permitidas por las normas
vigentes, o que se presuman nocivas para la salud;
b) cualquier tipo de suciedad, restos o excrementos;
c) aditivos no autorizados por las normas vigentes o en
cantidades superiores a las permitidas.
|
|
Artículo 102.- Se prohíbe la fabricación,
importación, tenencia, distribución,
comercialización o transferencia a cualquier título, de
alimentos alterados, contaminados, adulterados o
falsificados.
|
| DTO 475, SALUD
Art. Unico, N° 17
D.O. 13.01.2000 |
|
Artículo 103.- No podrá llevarse a efecto
enajenación alguna de alimentos, materias primas
procedentes de rezagos de aduanas, de empresas de transporte
o de salvataje de incendios, catástrofes, y desastres sin
la aprobación de la autoridad sanitaria.
|
|
Artículo 104.- El interesado o el martillero encargado
de la subasta en su caso, deberá solicitar con a lo menos
veinte días de anticipación a la enajenación, una visita
de inspección para comprobar el estado sanitario de los
productos, acompañando para el efecto el inventario de los
mismos.
|
|
Artículo 105.- Los alimentos que impliquen un
riesgo para la salud deberán ser
decomisados por la autoridad sanitaria, pudiendo quedar
retenidos bajo custodia de su dueño o tenedor con
prohibición de efectuar su
traslado, consumo, expendio o distribución a cualquier
título. Para estos efectos los establecimientos de
alimentos deberán definir un espacio físico suficiente y
adecuado para el almacenamiento de productos alimenticios no
aptos para el consumo humano, productos que deberán constar
con una marca clara, inequívoca e indeleble, como por
ejemplo, una X de color rojo u otro signo similar en
términos de prohibición.
Estos productos podrán ser destinados a uso industrial
no alimentario o alimentación animal, siempre que su
desnaturalización sea autorizada por la autoridad sanitaria
competente y, en caso que ello no sea posible, o no sea de
interés de su propietario, deberán ser destruidos,
incluyendo su disposición final en recinto adecuado para
ello.
La autorización sanitaria para la desnaturalización
deberá concederse expresamente previo pago del arancel
correspondiente, siendo el costo de la operación de cargo
del interesado, o de su propietario o tenedor, según el
caso.
| NOTA: El Art. segundo
del DTO 68, Salud, publicado el 23.01.2006, dispuso que la
modificación introducida al presente artículo rige a
contar de 180 días después de su publicación.
|
|
| DTO 68, SALUD
Art. primero Nº 6
D.O. 23.01.2006 |
|
Párrafo II
De la rotulación y publicidad
|
|
Artículo 106.- "Para los efectos de este reglamento
se entiende por:
1) Alimento sucedáneo: Aquel alimento destinado a
parecerse a un alimento usual, por su textura, aroma, sabor
u olor, y que se utiliza como
un sustituto completo o parcial
del alimento al que se parece;
2) Alimentos desecados: Corresponden a frutas, verduras,
hortalizas o leguminosas deshidratadas, aun cuando adopten
presentaciones farmacéuticas por vía oral;
3) Adición: Agregado de uno o más nutrientes o factores
alimentarios, por ejemplo fibra dietética a un alimento,
para fines nutricionales, en una concentración menor a un
10% de la Dosis Diaria de Referencia (DDR), por porción de
consumo habitual para un nutriente particular;
4) Alimento, ingrediente y materia alimentaria nuevos:
Aquel alimento, ingrediente y materia alimentaria obtenido a
través de procesos de síntesis físico químicos o a
través de procesos que ocurren en la naturaleza que no
corresponden a moléculas o compuestos propios de la
alimentación humana conocida;
5) Suplementación: Es la adición de nutrientes a la
alimentación, con el fin de producir un efecto nutricional
saludable o fisiológico característico;
6) Complementación: La adición de nutrientes a un
alimento que carece de ellos o que los contiene sólo en
cantidades mínimas con el propósito de producir un efecto
nutricional; la complementación comprende los conceptos de
adición, enriquecimiento o fortificación y
suplementación, según el porcentaje del nutriente
agregado, basado en las Dosis Diarias de Referencia y por
porción de consumo habitual;
7) Declaración de nutrientes: Relación o enumeración
normalizada del contenido de nutrientes de un alimento;
8) Declaración de propiedades nutricionales: Cualquier
representación que afirme, sugiera o implique que un
producto alimenticio posee propiedades nutricionales
particulares, especialmente, pero no sólo en cuanto a su
valor energético, contenido de proteínas, grasas y
carbohidratos disponibles, sino también por su contenido de
vitaminas, minerales y otros factores alimentarios, como por
ejemplo colesterol y fibra dietética;
9) Declaración de propiedades saludables: Cualquier
representación que afirme, sugiera o implique que existe
una relación entre un alimento, un nutriente u otra
sustancia contenida en un alimento y una condición
relacionada con la salud;
10) Descriptor: El término o palabra con que se define o
describe determinada característica que se le atribuye a un
alimento;
11) Factor alimentario: Sustancias nutrientes y sustancias
no nutrientes que cumplen un rol en nuestro organismo, tales
como colesterol, fibra dietética y otros;
12) Enriquecimiento o fortificación: La adición de uno o
más nutrientes o fibra dietética a un alimento, en una
concentración de un 10% o más de la Dosis Diaria de
Referencia (DDR) por porción de consumo habitual para un
nutriente en particular;
13) envase: cualquier recipiente que
contenga alimentos, que los cubra total o parcialmente.
14) Evento biotecnológico: Asociación o combinación de
genes, provenientes de distintas especies, producto de la
ingeniería genética, distinta o en distinto orden,
respecto a la que se da en la naturaleza en forma
espontánea;
15) Fecha o plazo de duración mínimo: Aquella fecha o
aquel plazo en que expira el período en que el fabricante
garantiza que el producto, conservado bajo determinadas
condiciones de almacenamiento, si las hubiera, mantiene
todas las cualidades significativas que se le atribuyen,
tácita o explícitamente, sin que esto signifique que el
producto no puede ser comercializado más allá de esta
fecha o plazo. El uso de fecha o plazo de duración mínimo
es optativo;
Esta fecha o plazo de duración mínimo podrá
indicarse en forma de recomendación pudiendo utilizarse la
expresión "consumir preferentemente antes de" u otras
equivalentes;
16) Fecha de elaboración: Aquélla en que el alimento se
convierte en el producto descrito en el envase;
17) Fecha de envasado: Aquélla en la que el alimento se
coloca en el envase en que se venderá finalmente;
18) Fecha de vencimiento o plazo de duración: Aquella
fecha o aquel plazo en que el fabricante establece que, bajo
determinadas condiciones de almacenamiento termina el
período durante el cual el producto conserva los atributos
de calidad esperados. Después de esa fecha o cumplido este
plazo el producto no puede ser comercializado.
Para los efectos de utilizar el plazo de duración, se
entenderá que éste empieza a regir a partir de la fecha de
elaboración.
La fecha de vencimiento o el plazo de duración
deberán ser claramente definidos, no aceptándose en estos
casos expresiones tales como "consumir preferentemente antes
de", u otras equivalentes, que resten precisión o
relativicen la fecha de vencimiento o el plazo de duración;
19) Ingrediente: Cualquier sustancia, incluidos los
aditivos, que se emplee en la fabricación o preparación de
un alimento y esté presente en el producto final, aunque
sea en forma modificada;
20) Ingrediente caracterizante: Aquel ingrediente que le da
al alimento atributos peculiares de modo de distinguirlo
claramente de los demás alimentos de su mismo tipo;
21) Lote: Cantidad determinada de un alimento producido en
condiciones esencialmente iguales;
22) Normalización o estandarización: La adición o
extracción de nutrientes a un alimento con el fin de
compensar las variaciones naturales en el contenido de
nutrientes;
23) Nutriente: Cualquier sustancia normalmente consumida
como un constituyente de un alimento, y que es necesaria
para el crecimiento, desarrollo y mantenimiento normal del
organismo o cuya deficiencia hace que se produzcan cambios
bioquímicos o fisiológicos característicos;
24) Nutriente esencial: Toda sustancia consumida como
constituyente de un alimento necesario para el crecimiento,
desarrollo y mantenimiento de las funciones vitales y que no
puede ser sintetizado en cantidades suficientes por el organismo humano;
25) porción de consumo habitual: cantidad de alimento
generalmente consumida por una persona en una oportunidad,
definida en función de la parte comestible del producto y
referida al producto tal como éste se comercializa.
Para productos alimenticios deshidratados, que se
consuman reconstituidos, la porción de consumo habitual se
informar de acuerdo a las instrucciones de reconstitución.
26) Restitución: La adición a un alimento, de uno o más
nutrientes, que se han perdido en el curso del proceso de
fabricación, de almacenamiento y manipulación, en
cantidades tales que dan lugar a la recuperación de tales
pérdidas;
27) Rotulación: Conjunto de inscripciones, leyendas o
ilustraciones contenidas en el rótulo que informan acerca
de las características de un producto alimenticio;
28) Rotulación o etiquetado nutricional: Toda descripción
destinada a informar al consumidor sobre las propiedades
nutricionales de un producto alimenticio. Comprende la
declaración de nutrientes y la información nutricional
complementaria;
29) Rótulo: Marbete, etiqueta, marca, imagen u otra
materia descriptiva o gráfica, que se haya escrito,
impreso, estarcido, marcado en relieve o hueco grabado o
adherido al envase de un alimento;30) Carbohidratos disponibles: El
total de carbohidratos con exclusión de la fibra
dietética.
31) Alimentos listos para consumo (LPC): alimentos
destinados por el productor o el fabricante o envasador al
consumo humano directo sin necesidad de cocinado u otro tipo
de transformación eficaz para eliminar o reducir a un nivel
aceptable los microorganismos peligrosos.
32) Hipersensibilidad alimentaria: reacciones adversas a los
alimentos de origen no tóxico. Se dividen en
Alergia alimentaria e Hipersensibilidad no alérgica a los
alimentos.
33) Alimento de referencia: aquel alimento homólogo que
sirve como patrón de comparación para realizar y destacar
una modificación nutricional, restringido al descriptor
reducido y sus sinónimos. Este alimento de referencia
deberá estar presente en el mercado y ser de propia
fabricación y, sólo en su defecto, se podrán considerar
otros alimentos homólogos, también presentes en el
mercado.
34) Publicidad: Toda forma de promoción,
comunicación, recomendación, propaganda, información o
acción destinada a promover el consumo de un determinado
producto.
36) Vegetales pre-elaborados: frutas u hortalizas,
combinadas o no, procesadas para su consumo de manera de
mantenerlos organolépticamente frescos a través de
operaciones como: remoción de partes no comestibles,
picado, laminación,
trituración, cubeteado, centrifugación, sanitización y
envasado, a los que se les puede prolongar su vida útil a
través de la disminución y control de la carga
microbiológica y de las condiciones de envasado u otros
procesos tecnológicos.
| NOTA: El artículo
transitorio del DTO 57, Salud, publicado el 06.05.2005,
dispone que las modificaciones a la presente norma entrarán
en vigencia dieciocho meses después de su publicación.
|
| NOTA 1 El
numeral 1 del artículo 1 del Decreto 15, Salud, publicado
el 02.08.2017, modifica el presente artículo en el sentido
de incluir el numeral 36, sin embargo, no se encuentra en
dicho texto el numeral 35, razón por la cual se ingresa a
continuación del 34. |
|
| DTO 57, SALUD
Art. único Nº 1
D.O. 06.05.2005 |
| DTO 58, SALUD
Art. 1 N 1
D.O. 16.06.2007 |
| DTO 58, SALUD
Art. 1º Nº 1
D.O. 16.06.2007 |
| Decreto 63, SALUD
Art. 1 Nº 1
D.O. 11.12.2009 |
| Decreto 88, SALUD
Art. 1 Nº 1
D.O. 06.01.2011 |
| Decreto 13, SALUD
Art. 1 N° 1
D.O. 26.06.2015 |
| Decreto 15, SALUD
Art. 1 N° 1
D.O. 02.08.2017 |
|
Artículo 107.- Todos los productos alimenticios que
se almacenen, transporten o expendan
envasados deberán llevar un rótulo o etiqueta que contenga
la información siguiente:
a) nombre del alimento. El nombre deberá indicar la
verdadera naturaleza del alimento en forma específica. Sin
perjuicio del nombre podrá indicarse su marca comercial. En los
productos sucedáneos deberá indicarse claramente esta
condición. Junto al nombre o muy cerca del
mismo, deberán aparecer las
palabras o frases adicionales necesarias para evitar que se
induzca a error o engaño respecto a la naturaleza y
condición física auténtica del alimento, que incluyen
pero que no se limitan al tipo o medio de cobertura, a la
forma de presentación o al tipo de tratamiento al que haya sido sometido.
INCISO ELIMINADO.
b) contenido neto expresado en unidades del sistema
métrico decimal o del sistema internacional, mediante el
símbolo de la unidad o con palabra completa. No deberá
acompañar a los valores del contenido neto ningún término
de significado ambiguo.
Además de la declaración del contenido neto, en los
alimentos envasados en un medio líquido deberá indicarse
en unidades del sistema métrico decimal o del sistema
internacional, el peso drenado del alimento;
c) En el caso de los alimentos nacionales, el nombre o razón social y
domicilio del fabricante, elaborador, procesador, envasador
o distribuidor, según sea el caso;
d) país de origen, debe indicarse en forma clara, tanto en los productos
nacionales como en los importados, conforme a las normas de
rotulación establecidas, respecto a esta información, en el decreto Nº 297, de 1992,
del Ministerio de Economía, Fomento y Reconstrucción, o en
el que lo reemplace;
e) Número y fecha de la resolución y el nombre
de la Secretaría Regional Ministerial de Salud que autoriza
el establecimiento que elabora o envasa el producto;
f) fecha de elaboración o fecha de envasado del producto.
Esta deberá ser legible, se ubicará en un lugar del envase
de fácil localización y se indicará en la forma y orden
siguiente :
- el día, mediante dos dígitos
- el mes, mediante dos dígitos o las tres primeras
letras del mes, y
- el año, mediante los dos últimos dígitos.
En aquellos productos cuya duración mínima sea
menor o igual a 90 días, podrá omitirse
el año. En aquellos productos cuya duración mínima sea
igual o mayor a tres meses, podrá omitirse el día.
ELIMINADO
La industria podrá identificar la fecha de
elaboración con la clave correspondiente al lote de
producción. En este caso los registros de esta última
deberán estar disponible en todo momento a la autoridad
sanitaria;
g) fecha de vencimiento o plazo de duración del producto.
Esta información se ubicará en el envase en un lugar
fácil de localizar y con una leyenda destacada.
La fecha de vencimiento se
indicará en la forma y orden establecido para la fecha de
elaboración. El plazo de duración se indicará en
términos de días o de meses o de años, según
corresponda, utilizando siempre unidades enteras, a menos
que se trate de "duración indefinida", caso en el cual
deberá consignarse dicha expresión.
Los productos que identifiquen la fecha de elaboración
con la clave del lote de producción, deberán rotular la
duración en términos de fecha de vencimiento, mientras que
los que indiquen expresamente la fecha de elaboración
podrán utilizar la fecha de vencimiento o plazo de
duración.
Los productos que rotulen "duración indefinida"
deberán necesariamente indicar la fecha de elaboración.
Se exceptúan de esta rotulación, las
frutas y hortalizas frescas, incluidos los tubérculos, que
no han sufrido modificaciones en sus caracteres o
composición, esto es, que no hayan sido peladas, cortadas o
tratadas de otra forma análoga, salvo las que fueren
necesarias para la separación de las partes no comestibles.
h) ingredientes, en el rótulo deberá figurar la lista de todos los
ingredientes y aditivos que componen el producto, con sus
nombres específicos, en orden decreciente de proporciones,
con la excepción correspondiente a los
saborizantes/aromatizantes, de acuerdo a lo
establecido en el artículo
136 del presente reglamento.
Cuando el alimento, ingrediente o derivado sea o
contenga alguno de los causantes de hipersensibilidad
(alergenos alimentarios) reconocidos oficialmente por resolución del
Ministerio de Salud, publicada en el Diario Oficial, el o
los alergenos deberán señalarse en la misma lista de
ingredientes, con letra de tamaño igual o mayor a las
letras de los ingredientes generales, o bajo el título
"Contiene..." u otro similar. Si el ingrediente es un
derivado de cualquiera de los alergenos reconocidos por la
citada resolución, deberá rotularse el ingrediente y
además el alergeno, como el ejemplo siguiente: caseína
(leche) o caseína de leche.
Si el producto alimenticio tiene riesgo de
contaminarse, desde la producción o elaboración hasta la
comercialización, con los citados alergenos, se deberá
incluir a continuación de la lista de ingredientes,
cualquiera de las siguientes frases: "Puede contener...",
"Contiene pequeñas cantidades de ...", "Contiene trazas de
..." o "Elaborado en líneas que también procesan....";
indicando el alergeno de que se trate;
i) aditivos, se debe indicar en el rótulo la
incorporación de aditivos, en orden decreciente de
concentraciones, con sus nombres específicos, con las
excepciones indicadas en el título correspondiente. Se debe incluir en la
lista de ingredientes todo aditivo alimentario que haya sido
empleado en las materias primas y otros
ingredientes de un alimento,
y que se transfiera a éste en cantidad suficiente para
desempeñar en él una función tecnológica
j) información nutricional de acuerdo a
lo establecido en el artículo 115 del presente reglamento;
k) instrucciones para el
almacenamiento, además de la fecha de duración mínima se
debe indicar en la etiqueta las condiciones especiales que
se requieran para la conservación del alimento, si de su
cumplimiento depende la validez de la fecha de duración
mínima. En caso de que, una vez abierto el envase, el
producto necesite de refrigeración u otro ambiente
especial, deberá también señalarse en la rotulación;
l) instrucciones para su uso, el rótulo debe contener las
instrucciones que sean necesarias sobre el modo de empleo,
incluida la reconstitución, si es el caso, para asegurar la
correcta utilización del alimento;
m) En el caso de los productos importados, el nombre y
domicilio del importador.
El importador estará obligado a mantener un registro
de todas las partidas internadas al país, por un plazo
mínimo de 90 días posteriores a la fecha de vencimiento o
del plazo de duración del producto, según corresponda. Los
alimentos de duración indefinida deberán mantener el
registro, al menos, durante tres años.
Este registro deberá incluir los antecedentes de la
destinación aduanera, los antecedentes sanitarios del
producto, la autorización de uso y consumo, las claves de
los lotes de producción o fechas de elaboración, la fecha
de vencimiento, el país de origen, tipo de producto, la
marca comercial, el nombre del proveedor extranjero y
estará, en todo momento, a disposición de la Autoridad
Sanitaria.
La clave del lote de producción o la fecha de
elaboración deberá, además, estar estampada en el envase,
permitiendo distinguir, inequívocamente, las distintas
partidas o lotes de producción.
Los alimentos importados deberán cumplir con todas las
demás normas de etiquetado vigentes en aquello no
expresamente regulado en este literal. La autorización de
internación y consumo se efectuará partida por partida,
quedando, por lo tanto, sujetos a todos los controles que la
Autoridad Sanitaria deba realizar conforme a lo dispuesto en
el presente reglamento; n) el alimento y/o materia prima
para consumo humano, modificados por medio de eventos biotecnológicos, que presenten
características nutricionales distintas a las del alimento
y/o materia prima convencional, deberá hacer mención de
ellas en el rótulo, de acuerdo a lo establecido en los
artículos 113 y 115 al 120 de este reglamento.
| NOTA: El artículo
transitorio del DTO 475, Salud, publicado el 13.01.2000,
establece un plazo de seis meses, a partir de la
publicación en el D.O. de dicho decreto, para dar
cumplimiento a lo señalado en el artículo 107, letra g) de
este decreto, respecto a la rotulación de la fecha de
vencimiento o plazo de duración. En el caso de bebidas
comercializadas en envases retornables, cuya rotulación sea
impresa directamente en el envase, el plazo será de dos
años.
|
| NOTA: 1 El
artículo transitorio del DTO 115, Salud, publicado el
25.11.2003, dispone que la modificaciones a este artículo,
regirán 180 días después de su publicación.
|
| NOTA: 2 El
artículo transitorio del DTO 57, Salud, publicado el
06.05.2005, dispone que las modificaciones a la presente
norma entrarán en vigencia dieciocho meses después de su
publicación.
|
|
| DTO 475, SALUD
Art. Unico, N° 20
D.O. 13.01.2000 |
| DTO 115, SALUD
Art. primero Nº 4
D.O. 25.11.2003 |
| Decreto 88,
SALUD
Art. 1 Nº 2
D.O. 06.01.2011 |
| Decreto 4,
SALUD
Art. 1 Nº 2
D.O. 09.01.2013 |
| DTO 115,
SALUD
Art. primero Nº 4
D.O. 25.11.2003 |
| Decreto 38, SALUD
Art. 1 N° 1
D.O. 02.02.2021 |
| DTO 475, SALUD
Art. Unico, N° 20
D.O. 13.01.2000 |
| DTO 475,
SALUD
Art. Unico, N° 20
D.O. 13.01.2000 |
| DTO 475, SALUD
Art. Unico, N° 20
D.O. 13.01.2000 |
| Decreto 38, SALUD
Art. 1 N° 2
D.O. 02.02.2021 |
| DTO 807, SALUD
N° 1
D.O. 03.02.1998
DTO 115, SALUD
Art. primero Nº 4
D.O. 25.11.2003 |
| Decreto 88,
SALUD
Art. 1 Nº 2
D.O. 06.01.2011 |
| DTO 57, SALUD
Art. único Nº 2 a)
D.O. 06.05.2005 |
| DTO 57, SALUD
Art. único Nº 2 b)
D.O. 06.05.2005 |
| Decreto 4,
SALUD
Art. 1 Nº 3
D.O. 09.01.2013 |
|
Artículo 108.- Además los productos importados
deberán cumplir con todas las disposiciones de rotulación
estipuladas en el presente Reglamento. Cualquier información
especificada en este Reglamento y que no haya sido
considerada en la rotulación original, que no esté en
castellano o no esté indicada de acuerdo a lo establecido
en este Reglamento, se deberá colocar en una etiqueta
adherida permanentemente al envase, de un tamaño y
ubicación adecuados.
|
| Decreto 88, SALUD
Art. 1 Nº 3
D.O. 06.01.2011 |
|
Artículo 109.- La información en el rótulo deberá
estar en idioma castellano, pudiendo repetirse eventualmente en otro
idioma. Los datos deberán señalarse con caracteres
visibles, indelebles y fáciles de leer en circunstancias
normales de compra y uso. En el caso de envases
transparentes, se prohíbe la colocación de información
obligatoria en el reverso de la etiqueta adherida al envase.
No se permitirá sobreimpresión o cualquier modificación
de la información contenida en el rótulo original, salvo
autorización por escrito de la autoridad sanitaria, con las
siguientes excepciones:
1) Los productos importados cuya rotulación esté en
otro idioma o no cumpla con las exigencias del presente
reglamento en lo que a rotulación se refiere.
2) Los productos que utilicen la sobreimpresión o
modificación de la información en el rótulo en
conformidad a las disposiciones del artículo 120 bis del
presente reglamento, incluyendo el ajuste de la información
nutricional que debe declararse o eliminando información
incompatible con dicho descriptor, cuando corresponda
|
| Decreto 31, SALUD
Art. 1 N° 1
D.O. 13.12.2016 |
|
Artículo 110.- La rotulación y publicidad de
cualquier tipo no deberá contener palabras, ilustraciones
y/u otras representaciones gráficas que puedan inducir a equívocos, engaños
o falsedades, o que de alguna forma sean susceptibles de
crear una impresión errónea respecto a la naturaleza,
composición o calidad del
producto. Asimismo, no deberán sugerirse ni indicarse
efectos terapéuticos, curativos ni posologías.
En aquellos alimentos o productos alimenticios
que contengan saborizantes/aromatizantes
(saborizante/aromatizante natural, saborizante/aromatizante
idéntico a natural y/o
saborizante/aromatizante artificial), se admitirá la
representación gráfica del alimento o sustancia cuyo sabor
caracteriza al producto, aunque éste no lo contenga,
debiendo acompañar el nombre del alimento con las
expresiones: "Sabor a ..." o "Sabor ..." llenando el espacio
en blanco con el nombre del sabor o sabores caracterizantes,
con letras en idéntico color, realce y visibilidad.
Para destacar la ausencia de nutrientes, factores alimentarios o ingredientes,
natural o normalmente ausentes en un alimento, deberá
hacerse en términos genéricos y no como una
característica exclusiva del alimento que lo declara.
| NOTA: El artículo
transitorio del DTO 115, Salud, publicado el 25.11.2003,
dispone que la modificaciones a este artículo, regirán 180
días después de su publicación.
|
|
| DTO 115, SALUD
Art. primero Nº 5
D.O. 25.11.2003 |
| DTO 115, SALUD
Art. primero Nº 5
D.O. 25.11.2003 |
| Decreto
88, SALUD
Art. 1 Nº 4
D.O. 06.01.2011 |
|
Artículo 110 bis: Tratándose de
cualquier alimento o producto alimenticio que, en su
composición nutricional, contenga energía, sodio,
azúcares o grasa saturada en cantidades superiores a las
establecidas en la Tabla Nº1 del artículo 120 bis de este
reglamento, no se podrá realizar publicidad dirigida a
menores de 14 años, cualquiera sea el lugar donde ésta se
realice.
Para estos efectos, se podrá considerar que la
publicidad está dirigida a este grupo etario si emplea,
entre otros elementos, personajes y figuras infantiles,
animaciones, dibujos animados, juguetes, música infantil,
si contempla la presencia de personas o animales que
atraigan el interés de menores de 14 años, o si contiene
declaraciones o argumentos fantásticos acerca del producto
o sus efectos, voces infantiles, lenguaje o expresiones
propias de niños, o situaciones que representen su vida
cotidiana, como son la escuela, el recreo o los juegos
infantiles. Esta calificación deberá ser fundada.
De igual manera, en la publicidad de estos alimentos no
se podrán utilizar aplicaciones interactivas, juegos,
concursos u otros elementos similares, dirigidos a menores
de 14 años.
Del mismo modo, también se entiende que la publicidad
de tales alimentos o productos alimenticios está dirigida a
menores de 14 años, cuando se realiza en programas o sitios
web dirigidos a ese público objetivo; o cuando estos
programas o sitios web capten una audiencia de menores de 14
años, mayor al 20%. Tampoco podrán publicitarse dichos
alimentos o productos alimenticios en espacios publicitarios
durante, entre o inmediatamente antes o después de la
difusión de dichos programas o sitios web.
Los alimentos o productos alimenticios que, en su
composición nutricional, contengan energía, sodio,
azúcares o grasa saturada en cantidades superiores a las
establecidas en la Tabla Nº1 del artículo 120 bis de este
reglamento, no podrán ofrecerse o entregarse gratuitamente
a los menores de 14 años, ni utilizar ganchos comerciales
dirigidos a éstos, no relacionados con la promoción propia
del producto, tales como: juguetes, accesorios, adhesivos,
incentivos u otros similares.
Estos alimentos o productos alimenticios no se podrán
expender, comercializar, promocionar ni publicitar dentro de
los establecimientos de educación parvularia, básica o
media.
La publicidad de estos alimentos que se efectúe por
medios de comunicación masivos, deberá llevar un mensaje
que promueva hábitos de vida saludable, cuyas
características serán determinadas por decreto supremo del
Ministerio de Salud dictado "por orden del Presidente de la
República".
Se exceptuarán de las disposiciones de este artículo,
los alimentos o las mezclas de éstos, a los que no se les
haya añadido azúcares, miel, jarabes, sodio o grasas
saturadas.
|
| Decreto 13, SALUD
Art. 1 N° 3
D.O. 26.06.2015 |
|
Artículo 110 ter.- Cuando a un alimento o producto
alimenticio se le haya adicionado sodio, azúcares o grasas
saturadas, y su contenido supere el valor establecido para
estos nutrientes en la Tabla N° 1 del artículo 120 bis de
este reglamento, o bien, cuando se le haya adicionado
azúcares, miel, jarabes o grasas saturadas, y su contenido
de energía supere el valor de energía establecido en esa
misma tabla, no se podrá realizar ningún tipo de
publicidad destinada a promover el consumo de ellos en todas
las transmisiones de cine y televisión entre las 06:00 y
las 22:00 horas.
Se exceptúa de la medida señalada en el inciso
anterior, la publicidad en todos los servicios de
televisión y cine realizada durante la transmisión de
eventos o espectáculos deportivos, culturales, artísticos
o de beneficencia social, cuando cumplan los siguientes
requisitos copulativos:
a) Que la publicidad se encuentre acotada a la
exhibición del nombre del producto o su marca.
b) Que la publicidad no esté destinada o dirigida,
directa o indirectamente a menores de 14 años.
c) Que, el evento o espectáculo no sea organizado o
financiado, exclusivamente, por la empresa interesada en la
publicidad del producto o por sus coligadas o relacionadas.
d) Que la publicidad no muestre situaciones de consumo
que induzcan a este ni al producto promocionado, tales como:
personas o personajes ingiriendo el producto o situaciones
que enuncien o hagan inferir su ingesta.
No se aplicarán las disposiciones de este artículo a
los alimentos o mezclas de éstos a los que no se les haya
añadido azúcares, miel, jarabes, sodio o grasas saturadas.
|
| Decreto 24
Art. 1 N° 1
D.O. 28.11.2017 |
|
Artículo 111.- La información debe colocarse en el
envase de manera que no se separe del mismo. Cuando el
envase esté cubierto por una envoltura no transparente, en
ésta deberá figurar toda la información necesaria.
|
|
Artículo 112.- Cuando en el etiquetado de un alimento
se destaque la presencia o el contenido de uno o más
ingredientes caracterizantes, o cuando la descripción del
alimento produzca el mismo efecto, deberá declararse el
porcentaje de él o los ingredientes masa/masa, en el
producto final. Se
excluyen de la aplicación de este artículo, aquellos ingredientes que son objeto
de condiciones o criterios específicos de rotulación, en
otros artículos del presente Reglamento o en sus
resoluciones complementarias.
| NOTA: El artículo
transitorio del DTO 57, Salud, publicado el 06.05.2005,
dispone que las modificaciones a la presente norma entrarán
en vigencia dieciocho meses después de su publicación.
|
|
| DTO 57, SALUD
Art. único Nº 3
D.O. 06.05.2005 |
| Decreto
88, SALUD
Art. 1 Nº 5
D.O. 06.01.2011 |
|
Artículo 113.- En el etiquetado nutricional se
podrá facultativamente, incorporar
información nutricional complementaria y cuando
corresponda, deberán rotular junto al nombre principal del
alimento o formando parte del
mismo o junto a la información nutricional, en caracteres
destacados, el descriptor nutricional correspondiente de
acuerdo a lo establecido en el artículo 120 de este
reglamento.
| NOTA: El artículo
transitorio del DTO 57, Salud, publicado el 06.05.2005,
dispone que las modificaciones a la presente norma entrarán
en vigencia dieciocho meses después de su publicación.
|
|
| DTO 57, SALUD
Art. único Nº 4
D.O. 06.05.2005 |
|
Artículo 114.- Todos los alimentos que en su rotulación o publicidad declaren
propiedades saludables o, cuando su descripción produzca el
mismo efecto, quedarán afectos a la declaración de
nutrientes tal como lo establece el presente reglamento. Las
declaraciones de propiedades saludables deberán ser
científicamente reconocidas o consensuadas
internacionalmente y deberán estar enmarcadas dentro de las
normas técnicas sobre directrices nutricionales aprobadas
por resolución del Ministerio de Salud, la que se
publicará en el Diario Oficial.
Tanto la declaración de propiedades saludables como la
declaración de propiedades nutricionales de un alimento o
cuando su descripción produzca ese mismo efecto, en su
rotulación y/o publicidad, no podrán hacer asociaciones
falsas, inducir el consumo innecesario de un alimento ni
otorgar sensación de protección respecto de una enfermedad
o condición de deterioro de la salud.
Será responsabilidad del fabricante, importador y/o
envasador final, que toda la información en el rótulo sea
fidedigna y dé cumplimiento a lo establecido en el presente
reglamento.
|
| DTO
58, SALUD
Art. 1º Nº 2
D.O. 16.06.2007 |
|
Artículo 115.- Todos los alimentos envasados
listos para su entrega al consumidor final
deberán obligatoriamente incorporar en su rotulación la
siguiente información nutricional:
a) Valor energético o
energía expresado en calorías (unidad de expresión kcal),
las cantidades de proteínas, grasas totales,
hidratos de carbono disponibles o carbohidratos disponibles
y azúcares totales, en gramos (unidad de expresión g) y el
sodio en miligramos (unidad de expresión mg).
En aquellos productos cuyo contenido total de grasa sea
igual o mayor a 3 gramos por porción de consumo habitual,
deberán declararse además de la grasa total, las
cantidades de ácidos grasos saturados, monoinsaturados,
poliinsaturados y ácidos grasos trans, en gramos y el
colesterol en miligramos.
En el caso de aquellos alimentos que contengan una
cantidad igual o menor a 0,5 gramos de ácidos grasos trans
por porción de consumo habitual, se aceptará como
alternativa la declaración que el alimento no contiene más
de 0,5 gramos de ácidos grasos trans por porción.
En el caso de aquellos alimentos que contengan una
cantidad igual o menor a 35 miligramos de sodio por porción
de consumo habitual, se aceptará como alternativa la
declaración que el alimento no contiene más de 35
miligramos de sodio por porción.
En el caso de aquellos alimentos que contengan una
cantidad igual o menor a 0,5 gramos de azúcares por
porción de consumo habitual, se aceptará como alternativa
la declaración que el alimento no contiene más de 0,5
gramos de azúcares por porción.
b) La cantidad de cualquier otro nutriente o factor
alimentario, como fibra dietética y colesterol, acerca del
que se haga una declaración de propiedades nutricionales
y/o saludables.
Todos estos valores deben expresarse por 100 g o 100 ml
y por porción de consumo habitual del alimento. Deberá
señalarse el número de porciones que contiene el envase y
el tamaño de la porción en gramos o mililitros y en
medidas caseras.
Los valores que figuren en la declaración de
nutrientes deberán ser valores medios ponderados derivados
de datos específicamente obtenidos de análisis de
alimentos realizados en laboratorios o de tablas de
composición de alimentos debidamente reconocidas por
organismos nacionales o internacionales, que sean
representativos del alimento sujeto a la declaración.
Los límites de tolerancia para los valores de los
nutrientes declarados en el rótulo, serán los siguientes:
Para aquellos alimentos que en su
rotulación declaren mensajes nutricionales o saludables y
para aquellos que utilicen descriptores nutricionales, con
excepción de aquellos que rotulen el descriptor del
artículo 120 bis del presente reglamento, los límites de
tolerancia para el valor declarado del nutriente en
cuestión, serán los siguientes:
i) cuando los nutrientes y factores alimentarios
sean expresados como proteínas, vitaminas,
minerales, fibra dietaria y/o grasas
monoinsaturadas y poliinsaturadas, deberán
estar presentes en una cantidad mayor o igual
al valor declarado en el rótulo;
ii) cuando los nutrientes y factores alimentarios
sean expresados como energía, hidratos de
carbono, azúcares, grasa total, colesterol,
grasa saturada, grasa trans y/o sodio,
deberán estar presentes en una cantidad
menor o igual al valor declarado en
el rótulo. La tolerancia anteriormente
descrita, aplicará también para los
descriptores nutricionales referidos
en el artículo 120 bis del presente
reglamento.
Para aquellos alimentos que en su rotulación no
destaquen mensajes nutricionales o saludables, ni utilicen
descriptores nutricionales, los límites de tolerancia para
el etiquetado nutricional serán los siguientes:
i) cuando los nutrientes y factores alimentarios
sean expresados como proteínas, vitaminas,
minerales, fibra dietaria y/o grasas
monoinsaturadas y poliinsaturadas, deberán
estar presentes en una cantidad mayor o
igual al 80% del valor declarado en el
rótulo;
ii) cuando los nutrientes y factores alimentarios
sean expresados como energía, hidratos de
carbono, azúcares, grasa total, colesterol,
grasa saturada, grasa trans y/o sodio, podrán
exceder sólo hasta un 20% del valor declarado
en el rótulo.
En cualquier caso, los límites de vitaminas, minerales
y fibra dietaria no deberán sobrepasar los valores
establecidos en la resolución Nº 393/02 y sus
modificaciones, que fija Directrices Nutricionales sobre Uso
de Vitaminas, Minerales y Fibras Dietéticas en Alimentos y
la resolución 394/02 y sus modificaciones, que fija
Directrices Nutricionales sobre Suplementos Alimentarios y
sus contenidos en Vitaminas y Minerales, todas del
Ministerio de Salud.
Para aquellos nutrientes cuyo porcentaje de
variabilidad, en función de la especie y del tipo de
manejo, sea superior a la tolerancia permitida, la empresa
deberá mantener a disposición de la autoridad sanitaria
los antecedentes técnicos que lo justifiquen.
Se exceptuarán del cumplimiento de lo anteriormente
dispuesto en este artículo:
i) Los alimentos predefinidos, fraccionados y
envasados con antelación al momento de la
venta en el lugar de expendio, incluidos los
platos preparados, los que deberán cumplir
con lo establecido en el artículo 468 de
este reglamento;
ii) Los estimulantes o fruitivos sin agregado de
otros ingredientes, los aditivos, los
coadyuvantes de elaboración, las especias
solas o en mezclas sin otros ingredientes y
las frutas y hortalizas en su estado natural;
iii) Los alimentos que se comercialicen a granel,
los porcionados o fraccionados y los
preparados a solicitud del público, aunque
éstos se envasen al momento de la venta.
Facultativamente, se podrá hacer declaración de
nutrientes en la etiqueta de los alimentos que no tengan
obligatoriedad de hacerlo, la que en todo caso, deberá
estar de acuerdo con lo establecido en el presente
reglamento.
La expresión numérica de los nutrientes y factores
alimentarios; la aproximación para expresar los valores de
nutrientes y factores alimentarios y la expresión de los
valores de las porciones de consumo habitual y de las
medidas caseras, se realizarán de acuerdo a los siguientes
criterios:
Expresión numérica de nutrientes y factores
alimentarios:
Valores iguales o mayores a 100 Se declararán en
números enteros
Valores menores a 100 y Se declararán en
números enteros o con
mayores o iguales a 10 un decimal
Valores menores a 10 y Se declararán en
números enteros o
mayores o iguales a 1 hasta con dos decimales
Valores menores a 1 Se declararán hasta con
dos decimales
Criterios de aproximación para valores de nutrientes y
factores alimentarios en cifras con decimales.
i) Si el dígito que se va a descartar es igual
o mayor que 5, se aumenta en una unidad el
dígito anterior.
ii) Si el dígito que se va a descartar es menor
que 5 se deja el dígito anterior.
La expresión numérica del número de porciones de consumo habitual
deberá ser en números enteros y la expresión del tamaño
de la porción en medidas caseras puede ser en unidades,
rebanadas, trozos, tazas, cucharadas u otras similares o sus
partes, como por ejemplo media cucharada o 1/4 taza. Cuando
el resultado de dividir el contenido del envase por el
tamaño de la porción definida, no sea número entero, o
cuando no sea fácilmente definible, las porciones se
aproximarán con los criterios de aproximación matemática
de los valores de nutrientes y factores alimentarios,
anteriormente descritos. Cuando la aproximación matemática
corresponda que sea al entero superior, será obligatorio el
uso de la expresión "alrededor de" o la expresión
"aprox.", acompañando al número entero obtenido. Cuando la
aproximación matemática corresponda que sea al entero
inferior, será facultativo el uso de la expresión
"alrededor de" o la expresión "aprox.", acompañando al
número entero obtenido.
c) La declaración de nutrientes deberá cumplir con las siguientes
características:
1) Las familias tipográficas que se utilizarán serán
las Arial, Dax, Futura, Helvética, Myriad, Swiss y Univers,
u otras familias equivalentes que posean igual peso y
consistencia visual, de cortes y perfiles rectos, sin serif,
y que incluyan versiones bold (negrita) y condensadas
estandarizadas.
2) La altura mínima de las letras y números será de
1,2 milímetros medidos en la altura de una letra H
mayúscula en las familias tipográficas previamente
definidas o sus equivalentes, lo que equivale
aproximadamente a 5 puntos tipográficos definidos en los
softwares (programas) de diseño gráfico.
3) Los colores utilizados en la combinación del fondo
con las letras y números con los que se entrega la
información nutricional, deberán tener entre sí el
máximo contraste posible, usándose para este fin colores
planos o llenos, sin gradaciones de color o tramas.
4) La información deberá ordenarse de preferencia en
forma vertical, usando dos columnas, una para la
información por 100 g ó 100 ml (según corresponda) y otra
para la información por porción de consumo habitual. Se
aceptará un ordenamiento horizontal o división de la
información en dos cuerpos o a renglón seguido.
| NOTA: El Art. 2º del
DTO 58, Salud, publicado el 16.06.2007, dispuso que las
modificaciones introducidas en el presente artículo
referidas a la expresión numérica de nutrientes y factores
alimentarios, la referida a los criterios de aproximación
para valores de nutrientes y factores alimentarios y la
referida a la expresión del número de porciones de consumo
habitual y medidas caseras, entrarán en vigencia en el
plazo de 12 meses desde su publicación.
|
|
| DTO 58, SALUD
Art. 1º Nº 3
D.O. 16.06.2007 |
| Decreto 14, SALUD
Art. 1 N° 1
D.O. 18.10.2011 |
| Decreto 13, SALUD
Art. 1 N° 4
D.O. 26.06.2015 |
| Decreto 13. SALUD
Art. 1 N° 5
D.O. 26.06.2015 |
| Decreto 88, SALUD
Art. 1 Nº 6
D.O. 06.01.2011 |
| Decreto 14,
SALUD
Art. 1 N° 2
D.O. 18.10.2011 |
|
Artículo 116.- Cuando se haga una declaración de
propiedades nutricionales o saludables con
respecto a la cantidad o el tipo de carbohidratos
disponibles o hidratos de carbono disponibles deberá
incluirse, además de lo prescrito en el artículo 115, la
cantidad total de cualquier carbohidrato disponible o
hidratos de carbono disponibles involucrada en la
declaración o mensaje.
Cuando se haga declaración de propiedades
nutricionales o saludables respecto a la fibra dietética,
además de lo establecido en el artículo 115, deberá
indicarse la cantidad de fibra dietética total, de fibra
soluble, de fibra insoluble y de la(s) fibra(s)
dietética(s) involucrada(s) en la declaración o mensaje.
Asimismo, cuando se declaren propiedades nutricionales
o saludables respecto a la cantidad o tipo de ácidos grasos
deberá indicarse inmediatamente a continuación de la
declaración del contenido total de grasa, las cantidades de
ácidos grasos saturados, ácidos grasos monoinsaturados,
poliinsaturados, ácidos grasos trans y colesterol. Se
exceptúan de esta obligatoriedad aunque hagan una
declaración de propiedad, usen un descriptor nutricional o
un mensaje saludable, a los alimentos que cumplen con los
parámetros establecidos en el artículo 120 para el
descriptor nutricional "libre de grasas total".
|
| Decreto 14, SALUD
Art. 1 N° 3
D.O. 18.10.2011 |
|
Artículo 117.- La declaración de propiedades nutricionales, la declaración de
propiedades saludables, la declaración de nutrientes y la
información nutricional complementaria, deberán ceñirse a
las normas técnicas que imparta al respecto el Ministerio
de Salud por resolución que se publicará en el Diario
Oficial.
|
| DTO
238, SALUD
Art. 1°, N° 2
D.O. 26.05.2000 |
|
Artículo 118.- Cuando se haga declaración de nutrientes podrán enumerarse,
además, las vitaminas y minerales que se hallen presentes
en cantidades significativas, 5% o más de la ingesta
recomendada para la población pertinente. Para la
población mayor de cuatro años se usará la Dosis Diaria
de Referencia (DDR), en energía, proteínas, vitaminas y
minerales propuesta por el Codex Alimentarius, en el caso de
la vitamina E, biotina, ácido pantoténico, cobre y
selenio, que no están especificadas en el Codex
Alimentarius, se utilizarán los valores propuestos por la
Food and Drug Administration (FDA), References Daily Intakes
(RDI).
Para lactantes y niños menores de cuatro años,
embarazadas y nodrizas se utilizarán como Dosis Diaria de
Referencia las respectivas RDI. En el caso del hierro y
vitamina A se aceptará, como Dosis Diaria de Referencia
durante el embarazo el valor de 30 mg/día para hierro y 800
mcg/día para vitamina A, establecidas en las Directrices
Nutricionales del Ministerio de Salud.
La información numérica sobre vitaminas y minerales
se expresará en unidades métricas, sistema internacional
para 100 g o 100 ml, para una porción de consumo habitual
expresada como porcentaje de la Dosis Diaria Recomendada de
referencia y por envase si éste contiene sólo una
porción. Además, esta información deberá especificarse
por porción de consumo habitual en la etiqueta si se indica
el número de porciones que contiene el envase.
|
| DTO
475, SALUD
Art. Unico, N° 26
D.O. 13.01.2000 |
|
Artículo 119.- La información nutricional
complementaria, que facultativamente se podrá añadir a la
declaración de nutrientes, tendrá por objeto facilitar la
comprensión del consumidor del valor nutritivo del alimento
y ayudarle a interpretar la declaración sobre él o los
nutrientes. INCISO DEROGADO
|
| DTO 238, SALUD
Art. 1°, N° 3
D.O. 26.05.2000 |
|
Artículo 120.- Para destacar las cualidades de
cualquier tipo de alimento o
producto alimenticio en cuanto a contenido energético (energía o
calorías), grasa total, grasa saturada, grasa trans,
colesterol, azúcar, azúcares, sodio, vitaminas, minerales,
proteínas, ácido docosahexaenoico (DHA), ácido
eicosapentaenoico (EPA), otros nutrientes y fibra
dietética, sólo se permitirá el uso de los descriptores
que se indican en el presente Reglamento.
El uso de un descriptor deberá ser seguido del nombre
del respectivo nutriente, factor alimentario o de la palabra
calorías o energía, según corresponda.
Se permite el uso de palabras en otro idioma o palabras
de fantasía, que se asocien inequívocamente con
características nutricionales, tales como light, diet,
high, lite, low, delgadíssimo, flakin y soft, entre otras,
siempre que cumplan con los parámetros de alguno de los
descriptores autorizados en el presente Reglamento.
Cuando se usen palabras en otro idioma o palabras de
fantasía asociadas con alguna característica nutricional,
la superficie ocupada por el descriptor en la rotulación,
deberá corresponder como mínimo al 33% de la superficie
ocupada por la palabra en otro idioma o de fantasía de
mayor tamaño y deberá ubicarse, al menos una vez, en la
cara principal del envase, junto a la palabra en otro idioma
o palabra de fantasía. Si la relación de superficie es
mayor o igual a 50%, entonces el descriptor podrá ubicarse
en cualquier cara.
A los efectos de aplicación de este artículo, para el
cálculo de los respectivos porcentajes, deberá
considerarse como superficie de referencia, la palabra en
otro idioma y/o palabra de fantasía, de mayor tamaño, y
deberá mantenerse siempre la condición de legibilidad de
todos los descriptores presentes en el etiquetado del
producto.
El descriptor reducido y sus sinónimos, no podrán
usarse si el alimento cumple el requisito para ser descrito
como bajo aporte. El descriptor bajo aporte no podrá
utilizarse para destacar el contenido de azúcar o azúcares
de un alimento.
En la declaración de propiedades nutricionales de los
alimentos no se podrán usar dos descriptores
simultáneamente para describir una misma propiedad.
Los descriptores: libre, bajo aporte, reducido y
liviano en colesterol sólo podrán aplicarse a alimentos
que sean libres de grasa trans (máximo 0,2 g de ácidos
grasos trans por porción de consumo habitual) y que
contengan por porción de consumo habitual máximo 2 g de
grasa saturada.
Los alimentos que usen los descriptores que a
continuación se indican, deberán ceñirse a lo establecido
en el artículo 113 de este reglamento:
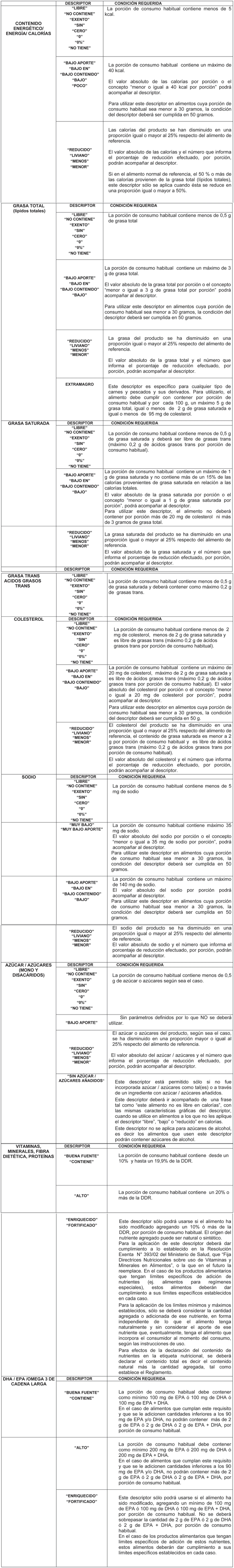
|
| NOTA El artículo 1
del Decreto 1, Salud, publicado el 13.07.2018 dispone
reemplazar en el cuadro inserto en el presente artículo las
secciones que establecen los descriptores nutricionales para
"Vitaminas, Minerales, Fibra Dietética, Proteínas" y para
"DHA / EPA / Omega 3 de Cadena Larga", junto con las
condiciones requeridas para declarar tales descriptores, de
la manera que la citada norma indica. |
|
| Decreto 88, SALUD
Art. 1 Nº 7
D.O. 06.01.2011 |
|
"Artículo 120 bis: Cuando a un
alimento o producto alimenticio se le haya adicionado sodio,
azúcares o grasas saturadas, y su contenido supere el valor
establecido en la Tabla Nº 1 del presente artículo,
deberá rotular la o las características nutricionales
relativas al nutriente adicionado. En el caso de la
energía, se deberá rotular su contenido cuando se le haya
adicionado azúcares, miel, jarabes, o grasas saturadas, y
se supere el valor establecido en la referida tabla.
Tabla Nº1: Límites de contenido de energía, sodio,
azúcares totales y grasas saturadas en alimentos.
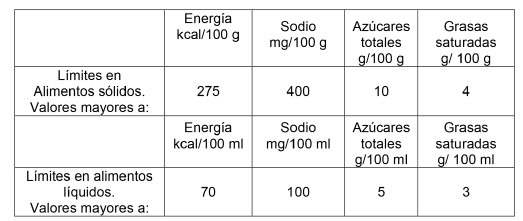
|
.
Se exceptuarán de la obligación de rotulación,
indicada en el inciso primero del presente artículo, los
siguientes alimentos o productos alimenticios:
A. Los alimentos o las mezclas de éstos, a los que no
se les haya añadido azúcares, miel, jarabes, sodio o
grasas saturadas.
B. Los alimentos que se comercialicen a granel, los
porcionados, los fraccionados y los preparados a solicitud
del público, aunque éstos se envasen al momento de la
venta.
C. Los siguientes alimentos del Título XXVIII, "De los
Alimentos para Regímenes Especiales":
c.1 Párrafo II de las fórmulas para lactantes.
c.2 Párrafo III de las preparaciones comerciales de
alimentos infantiles
(colados y picados), salvo aquellas que tengan
adición de azúcares.
c.3 Párrafo IV de los alimentos para uso infantil
procesados a base de
cereales, salvo aquellos que tengan adición de
azúcares.
c.4 Párrafo V de los alimentos para uso médico o
medicinal.
c.5 Párrafo VII de los alimentos para regímenes de
control de peso.
D. Los siguientes alimentos del Título XXIX, "De los
Suplementos Alimentarios y de los Alimentos para
Deportistas":
d.1 Párrafo I, de los suplementos alimentarios.
d.2 En el Párrafo II, de los alimentos para
deportistas, aquellos que
cumplan con los requisitos descritos en las
letras a), b), c) y d)
del artículo 540.
E. Los edulcorantes de mesa libres de azúcar y
calorías, regulados en el artículo 146 del presente
reglamento.
Para los efectos de este artículo, se entenderá que
un alimento es sólido o líquido según la unidad de medida
utilizada en la declaración del contenido neto del
alimento, es decir, será sólido si su contenido neto está
expresado en gramos u otra medida equivalente, o líquido si
su contenido neto está expresado en mililitros u otra
medida equivalente. En el caso de los productos alimenticios
que se consuman reconstituidos, se entenderá como sólido o
líquido, según como sea el producto listo para consumir,
de acuerdo a las instrucciones de reconstitución.
La forma de destacar las características nutricionales
indicadas en el inciso primero de este artículo será
rotulando un símbolo octagonal de fondo color negro y borde
blanco, y en su interior el texto "ALTO EN", seguido de:
"GRASAS SATURADAS", "SODIO", "AZÚCARES" o "CALORÍAS", en
uno o más símbolos independientes, según corresponda. Las
letras del texto deberán ser mayúsculas y de color blanco.
Además, en el mismo símbolo, deberá inscribirse en letras
blancas, la frase "Ministerio de Salud", según el diagrama
Nº 1 del presente artículo.
El o los símbolos referidos se ubicarán en la cara
principal de la etiqueta de los productos.
Las dimensiones del o los símbolos referidos estarán
determinadas de acuerdo al área de la cara principal de la
etiqueta, según el cuadro siguiente:
Cuadro Nº1: Dimensiones de símbolo.
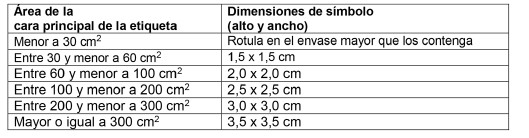
|
.
En el caso de los envases cuya área de la cara
principal de la etiqueta sea entre 30 cm² y menor a 60
cm², podrán rotularse el o los símbolos en otra cara
visible del envase.
Cuando corresponda rotular más de un símbolo con el
descriptor "ALTO EN", éstos deberán estar dispuestos uno
junto al otro. El o los símbolos deberán rotularse de modo
visible, indeleble y fácil de leer en circunstancias
normales de compra y uso. En ningún caso, podrán ser
cubiertos total o parcialmente.
Se exceptuarán de rotular el o los símbolos con el
descriptor "ALTO EN" los alimentos envasados cuya área de
la cara principal de la etiqueta sea menor a 30 cm², en
cuyo caso este o estos símbolos deberán rotularse en el
envase mayor que los contenga.
Cuando un alimento rotule el descriptor "ALTO EN", no
podrá declarar, en su rótulo o en su publicidad, las
propiedades nutricionales descritas en el artículo 120 del
presente reglamento, cuando se trate del mismo nutriente o
energía.
Cuando la información especificada en este artículo
no haya sido considerada en el diseño de la gráfica
original de la rotulación, se permitirá adherirla en la
etiqueta o envase, de modo indeleble, y de acuerdo al
tamaño, ubicación y demás características establecidas
en este reglamento.

|
.
|
| Decreto 13, SALUD
Art. 1 N° 6
D.O. 26.06.2015 |
|
Artículo 121.- En envases cuya superficie mayor sea
inferior a 10 cm2, podrá omitirse el número de lote,
lista de ingredientes e instrucciones para el uso, datos que deberán colocarse en
el envase mayor que los contenga.
Se exceptuarán de dar cumplimiento a lo establecido en
el artículo 115 del presente reglamento, los alimentos
envasados cuya superficie mayor (cara principal) sea
inferior a 40 cm2, en cuyo caso la información deberá
colocarse en el envase mayor que los contenga.
|
| DTO 58,
SALUD
Art. 1º Nº 4 a)
D.O. 16.06.2007
DTO 58, SALUD
Art. 1º Nº 4 b)
D.O. 16.06.2007 |
|
Párrafo III
De los envases y utensilios
|
|
Artículo 122.- Para los efectos de este reglamento se
entiende por:
a) aparatos: los elementos mecánicos o equipos
utilizables en la laboración, envasado, conservación y
distribución de los alimentos;
b) embalajes: los materiales y estructuras que protegen a
los alimentos, envasados o no, contra golpes o cualquier
otro daño físico durante su almacenamiento y transporte;
c) envase: cualquier recipiente que contenga alimentos, que los cubra total o
parcialmente; d) envolturas: los materiales que protegen a
los alimentos en su empaquetado permanente o en el momento
de venta al público;
e) equipo: al conjunto de maquinarias e instalaciones que
se precisen en la producción, elaboración ,
fraccionamiento, envasado y expendio de alimentos;
f) recipientes: a los receptáculos destinados a contener
por lapsos variables, materias primas, productos intermedios
o alimentos en la industria y establecimientos de alimentos;
g) revestimiento: las cubiertas que íntimamente unidas a
los utensilios, recipientes, envases, embalajes, envolturas
y aparatos referidos en este artículo, los protegen y
conservan durante su vida útil.
h) utensilios: a los elementos de uso manual y corriente
en la industria alimentaria y establecimientos de alimentos
así como los enseres de cocina y la vajilla, cubiertos y
cristalería de uso doméstico;
|
| DTO 58,
SALUD
Art. 1º Nº 5
D.O. 16.06.2007 |
|
Artículo 123.- Los utensilios, recipientes, envases,
embalajes, envoltorios y aparatos destinados a la
elaboración, conservación, fraccionamiento y distribución
de los alimentos, deberán estar construidos o revestidos
con materiales resistentes al producto y no cederán
sustancias tóxicas, contaminantes o modificadoras de los
caracteres organolépticos o nutricionales de dichos
productos.
|
|
Artículo 124.- El equipo y los utensilios empleados
para materias no comestibles o desechos deberán
identificarse, respecto a su utilización y no deberán
emplearse para productos comestibles.
|
|
Artículo 125.- Los metales en contacto con los
alimentos y sus materias primas no deberán contener más de
uno por ciento de impurezas constituidas por plomo,
antimonio, zinc, cobre, cromo, hierro, estaño considerados
en conjunto, ni más de 0,01 por ciento de arsénico, ni
otros contaminantes constituidos por metales o metaloides
que puedan considerarse nocivos. Asimismo, los utensilios,
recipientes, envases y aparatos fabricados con metales, no
deberán ceder las sustancias antes señaladas en cantidades
superiores a las indicadas.
|
|
Artículo 126.- Todos los utensilios, recipientes,
envases, embalajes, envolturas, laminados, películas,
barnices, partes de aparatos, cañerías y accesorios de
material plástico que se hallen en contacto con alimentos y
sus materias primas, no deben contener como monómeros
residuales más de 0,25 % de estireno, 1 ppm de cloruro de
vinilo y 11 ppm de acrilonitrilo. Asimismo todos los objetos
de materias plásticas no deben ceder a los alimentos más
de 0,05 ppm de cloruro de vinilo o de acrilonitrilo, y
ninguna otra sustancia utilizada en la fabricación de
materias plásticas que puedan ser nocivas para la salud.
|
|
Artículo 127.- El aire de los envases se podrá
reemplazar por un gas inerte tal como nitrógeno, bióxido
de carbono u otros permitidos por la autoridad sanitaria.
|
|
Artículo 128.- Se permite el empleo de envases de
retorno siempre que sea posible efectuar una correcta
higienización de los mismos antes de usarlos nuevamente. La
limpieza de dichos envases debe ser completa, debiendo
éstos desecharse cuando, debido a su uso o por cualquier
otra causa, se hallen alterados.
En el caso de los alimentos que se
comercializan en envases retornables, la
información sanitaria y nutricional que vaya escrita,
impresa, estarcida, marcada en relieve o hueco grabada,
cuando el rótulo o etiqueta
forme parte del envase, se hará exigible a partir de la
fecha de fabricación del envase sólo cuando esta fecha sea
posterior a la fecha de entrada en vigencia del decreto
modificatorio correspondiente.
En los envases retornables se deberá registrar de
manera indeleble la fecha de fabricación del envase. El mes
de fabricación se indicará, según corresponda mediantes
letras de la A a la L y el año mediante los dos últimos
dígitos.
| NOTA: El Art. 2º del
DTO 47, Salud, publicado el 15.05.2008, dispuso que la
modificación que introduce al presente artículo rige a
contar del 06 de mayo de 2008.
|
|
| DTO 47, SALUD
Art. 1º Nº 1
D.O. 15.05.2008 |
|
Artículo 129.- Se prohíbe utilizar para contener
sustancias alimenticias y sus correspondientes materias
primas, recipientes que en su origen o en alguna oportunidad
hayan estado en contacto con productos no alimenticios o
incompatibles con los mismos. Asimismo, se prohíbe envasar
productos industriales en recipientes de productos
alimenticios.
|
|
TITULO III
De los aditivos alimentarios
|
|
Párrafo I
Disposiciones generales
|
|
Artículo 130.- Se considera aditivo
alimentario cualquier sustancia que no se consume
normalmente como alimento por sí misma ni se usa como
ingrediente típico del alimento, tenga o no valor
nutritivo, cuya adición intencional al alimento para un fin
tecnológico (inclusive organoléptico) en la fabricación,
elaboración, tratamiento, envasado, empaquetado, transporte
o almacenamiento provoque o pueda esperarse razonablemente
que provoque (directa o indirectamente), el que ella misma o
sus subproductos lleguen a ser un complemento del alimento o
afecten a sus características.
|
| DTO 475, SALUD
Art. Unico, N° 29
D.O 13.01.2000 |
|
Artículo 131.- Se considera coadyuvante toda
sustancia o materia, excluidos aparatos y
utensilios, que no se consume como ingrediente alimenticio
por sí misma y que se emplea intencionalmente en la
elaboración de materias primas, alimentos o sus
ingredientes, para lograr alguna finalidad tecnológica
durante el tratamiento o la elaboración pudiendo dar lugar
a la presencia no intencionada, pero inevitable, de residuos
o derivados inocuos en el producto final.
|
| DTO 475, SALUD
Art. Unico, N° 30
D.O. 13.01.2000 |
|
Artículo 132.- Para los efectos del presente
reglamento se consideran aditivos alimentarios permitidos,
aquellos cuyo carácter inocuo ha sido evaluado
toxicológicamente, considerando especialmente los efectos
carcinogénicos, mutagénicos y teratogénicos, en
diferentes especies de animales como asimismo en estudios
bioquímicos y metabólicos.
Se prohíbe la adición a alimentos de sustancias con
principios terapéuticamente activos o sustancias
calificadas como productos farmacéuticos.
|
|
Artículo 133.- Sólo se permite la incorporación de
un aditivo a un alimento si:
a) cumple con un fin tecnológico, tanto en la
producción, elaboración, preparación, acondicionamiento,
envasado, transporte o almacenamiento de un alimento;
b) contribuye a mantener la calidad nutritiva del
alimento, previniendo la destrucción de componentes
valiosos del mismo;
c) permite mejorar sus características organolépticas.
|
|
Artículo 134.- Se prohíbe el uso de un aditivo, en
caso que:
a) disminuya sensiblemente el valor nutritivo del alimento
al substituir un ingrediente importante o al posibilitar
pérdidas de componentes nutritivos valiosos, salvo cuando
se trate de alimentos para regímenes especiales;
b) permita disimular una calidad defectuosa o la
aplicación de técnicas de elaboración o manipulación no
permitidas;
c) induzca a engaño al consumidor sobre la cantidad o
naturaleza del alimento, o al contralor, por contribuir a
falsear los resultados del análisis.
|
|
Artículo 135.- Todos los aditivos deberán cumplir las
normas de identidad, de pureza y de evaluación de su
toxicidad de acuerdo a las indicaciones del Codex
Alimentarius de FAO/OMS. Debe ser factible su evaluación
cualitativa y cuantitativa y su metodología analítica debe
ser suministrada por el fabricante, importador o
distribuidor.
|
|
Artículo 136.- Los aditivos deberán
declararse obligatoriamente en la rotulación,
en orden decreciente de proporciones, y en cualquiera de
estas formas: a) con su nombre específico según el Codex
Alimentarius; b) con el sinónimo correspondiente consignado
en el presente reglamento, o c) con el nombre genérico de
la familia a la cual pertenecen expresado en este Párrafo
de los aditivos alimentarios, en singular o plural, según
sea el caso. Se exceptúa de esta obligación a los
saborizantes/aromatizantes, los que pueden declararse en
forma genérica sin detallar sus componentes, según la
clasificación que les corresponda de acuerdo con el
Artículo 155 de este reglamento.
Aquellos aditivos que requieran ser colocados bajo
rotulación destacada, deben hacerlo con su nombre
específico, letras en negrilla y de un tamaño mayor al
resto de la lista de ingredientes y aditivos.
|
| Decreto 106, SALUD
Art. 1 Nº 1
D.O. 23.04.2009 |
|
Artículo 137.- Los aditivos sólo pueden ser agregados
dentro de los límites establecidos en el Párrafo II de
este Título y de los límites específicos que para cada alimento se establecen
expresamente en este reglamento o de acuerdo a las Buenas
Prácticas de Fabricación, (B.P.F.), que en dicho párrafo
se señalan.
| NOTA: El Art. segundo
del DTO 68, Salud, publicado el 23.01.2006, dispuso que la
modificación introducida al presente artículo rige a
contar de 180 días después de su publicación.
|
|
| DTO 68,
SALUD
Art. primero Nº 8
D.O. 23.01.2006 |
|
Artículo 138.- En los casos en que se incorporen en un
alimento dos o más aditivos con una misma función, a los
cuales se les haya asignado concentraciones máximas, la
suma de las concentraciones empleadas, no podrá ser
superior a la concentración máxima autorizada para aquel
aditivo al cual se le ha fijado la concentración
más alta, respetando las máximas
individuales de cada uno de los aditivos empleados.
|
| DTO 475, SALUD
Art. Unico, N° 32
D.O. 13.01.2000 |
|
Artículo 139.- Si un aditivo alimentario cumple más
de una función tecnológica y aparece clasificado sólo en
una de ellas, se entiende como autorizado para las otras
funciones dentro de los límites indicados en el artículo
correspondiente.
|
|
Párrafo II
Del uso de los Aditivos
|
|
Artículo 140.- Se permite usar como reguladores
de acidez, sólo aquellos que se indican
en este artículo, de acuerdo con las Buenas Prácticas de
Fabricación:
|
| DTO 475, SALUD
Art. Unico, N° 33
D.O. 13.01.2000 |
| Decreto 106, SALUD
Art. 1 Nº 2
D.O. 23.04.2009 |
|
Artículo 141.- Se permite usar como sustancias
antiaglomerantes y antihumectantes sólo aquellas que se
indican en este artículo y en concentraciones no mayores,
en producto terminado listo para el
consumo, que las que se señalan en forma específica para
cada aditivo:
|
| Decreto 106, SALUD
Art. 1 Nº 3
D.O. 23.04.2009 |
|
Artículo 142.- Se permite usar como sustancias
antiespumantes y espumantes sólo aquellas que se indican en
este artículo y en concentraciones no mayores, en producto
terminado listo para el consumo, que las que se señalan en
forma específica para cada aditivo:
a) antiespumantes
b) espumantes
|
| Decreto 106, SALUD
Art. 1 Nº 4
D.O. 23.04.2009 |
| Decreto 106, SALUD
Art. 1 Nº 4
D.O. 23.04.2009 |
|
Artículo 143.- Se permite usar como
sustancias antioxidantes sólo aquellas que se
indican en este artículo y en concentraciones no mayores a
las que se señalan en forma específica para cada aditivo.
Los límites de los antioxidantes señalados en la letra a)
del presente artículo están expresados en base a materia
grasa pura y en la letra b) se listan los antioxidantes para
otros productos.
a) Antioxidantes para materias
grasas
b) Antioxidantes para otros productos
| NOTA El Nº 2 del Art.
1º del Decreto 71, Salud, publicado el 23.08.2010, con
vigencia a contar de 24 meses después de su publicación,
modificó el cuadro de la letra a) en el sentido de agregar
los siguientes aditivos, Nºs. 304 y 305:
N° NOMBRE LIMITE
SIN CODEX SINONIMOS MAXIMO
304 Palmitato Vitamina C
de ascorbilo palmitato 500 mg/kg
305 Estearato Vitamina C
de ascorbilo estearato 500 mg/kg |
|
| Decreto 71, SALUD
Art. 1º Nº 1
D.O. 23.08.2010 |
| Decreto 106, SALUD
Art. 1 Nº 5
D.O. 23.04.2009 |
| Decreto 106, SALUD
Art. 1 Nº 5
D.O. 23.04.2009 |
|
Artículo 144.- Se permite usar como sustancias
secuestrantes y sinergistas de antioxidantes sólo aquellas
que se indican en este artículo y en concentraciones no
mayores, a las que se señalan en forma especifica para cada
aditivo:
a) Sinergistas de antioxidantes
b) Secuestrantes
|
| Decreto 106, SALUD
Art. 1 Nº 6
D.O. 23.04.2009 |
| Decreto 106, SALUD
Art. 1 Nº 6
D.O. 23.04.2009 |
|
Artículo 145.- Se permite usar como
sustancias colorantes sólo las que se señalan
en el presente artículo.
Para los efectos de rotulación se deberá emplear el
nombre, según el Codex Alimentarius, señalado
en la siguiente lista:
(1) Sólo en conservas de cerezas, macedonia de frutas y
marrasquino
(2) Sólo para decoraciones
(3) Rotular en forma destacada de acuerdo al Art. 136
|
| DTO 475, SALUD
Art. Unico, N° 34
D.O. 13.01.2000 |
| Decreto 106, SALUD
Art. 1 Nº 7
D.O. 23.04.2009 |
|
Artículo 146.- Sólo se permite usar los
edulcorantes no nutritivos en uno o más de los
siguientes alimentos:
a) Alimentos para regímenes de control de peso.
b) Alimentos libres, bajos o reducidos en azúcar o
azúcares (mono y disacáridos).
c) Alimentos libres, bajos o reducidos en calorías.
d) Alimentos libres, bajos o reducidos en grasas.
Los descriptores anteriormente señalados en las letras
b), c) y d) se rigen por lo dispuesto en el artículo 120
del presente reglamento.
Los edulcorantes no nutritivos que se pueden utilizar
en uno o más de los alimentos antes descritos, son los que
se indican a continuación:
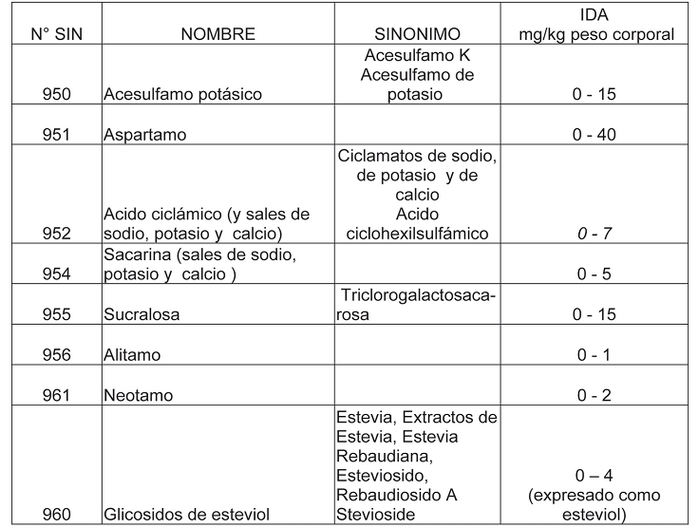
|
En la rotulación de los alimentos que contienen estos
productos deberá indicarse en forma
destacada su agregado como
aditivo y la cantidad de edulcorante por porción de consumo
habitual servida y por cada 100 g o 100 ml del producto
listo para el consumo, señalando, además, para cada
edulcorante utilizado los valores de ingesta diaria
admisible (I.D.A.), en mg/kg de peso corporal, según
recomendaciones de FAO/OMS.
Los edulcorantes de mesa, cualquiera sea su forma de
presentación, deberán cumplir con la rotulación general y
nutricional que establece este reglamento, indicando,
además, la concentración por porción de consumo habitual
y por cada 100 g o 100 ml y la I.D.A. correspondiente.
Adicionalmente, en caso de empleo de Aspartamo, se
deberá indicar en forma destacada en la rotulación:
"Fenilcetonúricos; contiene fenilalanina".
Ninguna forma de bebidas o refrescos,
tanto líquidos como en polvo para preparación, podrán
contener más de 250 mg/litro de ácido ciclámico o de sus
sales.
| NOTA 6 El artículo
transitorio del DTO 115, Salud, publicado el 25.11.2003,
dispone que la modificaciones a este artículo, regirán 180
días después de su publicación. |
|
| Decreto 71, SALUD
Art. 1º Nº 3
D.O. 23.08.2010 |
| Decreto 106, SALUD
Art. 1 Nº 8
D.O. 23.04.2009 |
| DTO 115, SALUD
Art. primero Nº 12
D.O. 25.11.2003 |
| Decreto 106, SALUD
Art. 1 Nº 9
D.O. 23.04.2009 |
|
Artículo 147.- Se permite usar como sustancias
emulsionantes sólo aquellas que se indican en este
artículo y en concentraciones no mayores, en producto
terminado listo para el consumo, que las que se señalan en
forma específica para cada aditivo :
Los emulsionantes en base a las sales de fósforo señaladas precedentemente se podrán
rotular como fosfato, polifosfatos o mezcla de ambos, según
sea el caso.
| NOTA El Nº 1 del
Art�culo 1º del Decreto 11, Salud, publicado el 06.08.2013,
modificó la presente norma en el sentido de agregar entre
los números SIN 436 Y 444 el SIN Nº 442 la sustancia
emulsionante Sales de amonio del ácido fosfatídico, de la
manera indicada en la citada norma |
|
| Decreto 106, SALUD
Art. 1 Nº 10
D.O. 23.04.2009 |
| DTO
475, SALUD
Art. Unico, N° 36
D.O. 13.01.2000 |
|
Artículo 148.- Sólo podrán usarse como
sales emulsionantes aquellas que se indican
en este artículo y sus concentraciones no podrán ser
mayores, en producto terminado listo para el consumo, que
las que se señalan en forma específica para cada aditivo
en la siguiente tabla:
Los emulsionantes fabricados en base a las sales de
fósforo señaladas precedentemente se podrán rotular como
fosfatos, polifosfatos o mezcla de ambos, según sea el
caso.
El límite máximo de fósforo expresado como P2O5,
corresponde sólo al agregado como
aditivo, sin considerar el propio de las materias primas
utilizadas en la elaboración del alimento.
Para su cálculo se debe restar del fósforo total, el
aportado por el alimento.
|
| Decreto 106, SALUD
Art. 1 Nº 11
D.O. 23.04.2009 |
|
Artículo 149.- Sólo podrán usarse como
aditivos enturbiantes los que se indican en la
presente tabla, en concentraciones no mayores a las
señaladas:
|
| Decreto 106, SALUD
Art. 1 Nº 12
D.O. 23.04.2009 |
|
Artículo 150.- Sólo se podrán usar como
sustancias espesantes o estabilizadores,
aquellas que se indican en este artículo, de acuerdo con
Buenas Prácticas de Fabricación:
Los almidones indicados en este artículo se podrán
rotular en forma genérica como almidones modificados.
| NOTA El numeral 10 del
Decreto 68, Salud, publicado el 23.01.2006, modifico los
listados de la presente norma, de la manera que la citada
norma indica. |
|
| Decreto 106, SALUD
Art. 1 Nº 13
D.O. 23.04.2009 |
|
Artículo 151.- Sólo podrán usarse como
sustancias estabilizadoras de humedad, agentes
de relleno y/o edulcorantes aquellas que se indican en este
artículo, de acuerdo con las Buenas Prácticas de
Fabricación:
|
| Decreto 106, SALUD
Art. 1 Nº 14
D.O. 23.04.2009 |
|
Artículo 152.- Sólo podrán usarse como
aditivos impermeabilizantes o sustancias de
recubrimiento aquellas que se indican en este artículo y en
concentración no mayor que la señalada en forma
específica:
|
| Decreto 106, SALUD
Art. 1 Nº 15
D.O. 23.04.2009 |
|
Artículo 153.- Se permite usar como sustancias
leudantes, blanqueadoras y mejoradoras de la panificación,
sólo aquellas que se indican en este artículo y en
concentraciones no mayores que las que se señalan en forma
específica para cada aditivo:
a) leudantes
b) Blanqueadores o mejoradores de
panificación
|
| Decreto 106, SALUD
Art. 1 Nº 16
D.O. 23.04.2009 |
| Decreto 106, SALUD
Art. 1 Nº 17
D.O. 23.04.2009 |
|
Artículo 154.- Se permite utilizar como preservantes
químicos sólo los que se indican en este artículo y en
concentraciones no mayores, en productos terminando, que las
que se señalan en forma específica para cada aditivo:
| NOTA El Nº 4 del Art.
1º del Decreto 71, Salud, publicado el 23.08.2010, con
vigencia a contar de 24 meses después de su publicación,
modificó el Nº 234 del cuadro contenido en el presente
artículo, el que queda de la siguiente forma:
N° SIN NOMBRE CODEX SINONIMOS LIMITE MAXIMO
234 Nísina 12,5 mg/kg en quesos
10 mg/kg en crema
natural o nata
cuajada
|
| NOTA 1 El
Nº 2 del Art�culo 1º del Decreto 11, Salud, publicado el
06.08.2013, modificó la presente norma en el sentido de
agregar entre los números SIN 242 Y 249 el SIN Nº 243
preservante quimico Etil - lauroil arginato, de la manera
indicada en la citada norma. |
|
| Decreto 106, SALUD
Art. 1 Nº 18
D.O. 23.04.2009 |
|
Artículo 155.- Se permite usar como
saborizantes/aroma- tizantes aquellas sustancias aromáticas
o mezclas de ellas obtenidas por procesos físicos o
químicos de aislamiento o síntesis de tipo natural,
idéntico a natural y artificial aceptados por FAO/OMS,
Unión Europea, Food and Drug Administration y
F.E.M.A.(Flavor and Extractive Manufacturing Assoc.).
Se entenderá por:
saborizante/aromatizante natural: al producto puro de
estructura química definida o al preparado saborizante de
estructura química no definida, concentrado o no, que tiene
características saporíferas y son obtenidos por un proceso
físico, microbiológico o enzimático a partir de productos
de origen vegetal o animal.
saborizante/aromatizante idéntico a natural: es aquel
producto obtenido por procesos físicos, microbiológicos,
enzimáticos, de síntesis química o de aislamiento por
procesos químicos, cuya formulación incluye componentes
idénticos a los existentes en la naturaleza.
saborizante/aromatizante artificial: es aquel producto
que en su formulación incluye, en una proporción
cualquiera, componentes que no se encuentran naturalmente en
productos animales o vegetales y son obtenidos por síntesis
química.
|
|
Artículo 156.- Podrán usarse disolventes portadores
o diluyentes de sustancias
saborizantes/aromatizantes y de antioxidantes, siempre que
cumplan con las normas establecidas por el Codex
Alimentarius FAO/OMS y su concentración esté de acuerdo
con las buenas prácticas de fabricación.
|
| Decreto 106, SALUD
Art. 1 Nº 19
D.O. 23.04.2009 |
|
Artículo 157.- Se permite usar como acentuantes del
sabor sólo los que se indican en este artículo y en
concentraciones no mayores, en producto terminado listo para
el consumo, que las que se señalan en forma específica
para cada aditivo:
|
| Decreto 106, SALUD
Art. 1 Nº 20
D.O. 23.04.2009 |
|
Artículo 158.- Se permite el uso de preparaciones
enzimáticas y coadyuvantes de elaboración siempre que
cumplan con las normas establecidas por el Codex
Alimentarius FAO/OMS y su concentración estará de acuerdo
con las buenas prácticas de fabricación.
|
| DTO 475,
SALUD
Art. Unico, N° 1
D.O. 13.01.2000 |
|
Artículo 159.- En el caso que antecedentes sanitarios
y técnicos hagan conveniente introducir modificaciones a
las listas establecidas en los artículos precedentes de
este Título, el Ministerio de Salud propondrá el
correspondiente decreto supremo modificatorio al Presidente
de la República.
|
|
TITULO IV
De los Contaminantes y Residuos
|
| Decreto 64, SALUD
Art. 1 Nº 1
D.O. 11.12.2009 |
|
Párrafo I
De los metales pesados
|
|
Artículo 160.- Los elementos que se indican a
continuación no podrán sobrepasar, en los alimentos
señalados, los límites máximos siguientes:
Límite
máximo
mg/kg de
producto
final
AESENICO
Aceites y grasas 0,1
comestibles
Nota:
No incluye la
mantequilla
Grasas y mezclas 0,1
de grasas para untar
Nota:
No incluye la
mantequilla
Sal 0,5
comestible
Nota:
Ver Párrafo II del
Título XXIII
Aguas minerales y aguas 0,01
envasadas para bebida Nota:
expresado en mg/l
Arroz pulido 0,2
Notas:
Límite para arsénico
Inorgánico
Solo será necesario determinar
Arsénico inorgánico, si la
medición de Arsénico Total
superara este límite.
CADMIO
Sal comestible 0,5
Agua mineral de mesa 0,01
COBRE
Caseína ácida comestible y caseinatos
comestibles 5,0
Aceites y grasas comestibles 0,1 no virgen
0,4 virgen
Margarina 0,1
Mayonesa 2,0
Azúcar blanca 1,0
Azúcar en polvo, dextrosa (anhidra,
monohidrato, en polvo), lactosa, fructosa 2,0
Jarabe de glucosa 5,0
Jugos de frutas y hortalizas 5,0 (1)
Jugos concentrados de fruta 5,0 (1) en el
producto
reconsti-
tuido
Néctares de fruta 5,0 (1)
Mantecas de cacao 0,4
Chocolates, dulce de manteca de cacao 15,0
Chocolate no edulcorado 30,0
Chocolate compuesto y relleno 20,0
Cacao en polvo y mezclas secas de
cacao y azúcar; torta de prensado
de cacao 50,0
Cacao sin cáscara ni germen;
cacao en pasta 30,0
Emulsiones lácteas para untar,
pobres en grasa 0,1
Suero dulce en polvo y suero
ácido en polvo, de calidad alimentaria 5,0
Caseína de cuajo comestible 2,0
Grasa de mantequilla 0,05
Sal comestible 2,0
Agua mineral de mesa 1,0
Otros productos 10,0
ESTAÑO
Frutas y hortalizas en conserva 250
Aceitunas de mesa 250
Conservas de pescados y mariscos 250
Jugos de frutas y hortalizas,
excepto manzana, uva y grosella negra 200
Jugos de manzana, uva y grosella
negra 150
Jugos concentrados de frutas,
excepto manzana, uva y grosella
negra 250 en el producto
reconstituido.
Jugos concentrados de manzana,
uva y grosella negra 150 en el producto
reconstituido
Néctares de fruta:
damasco, durazno, pera, guayaba
y cítricos 250
grosella negra y frutas pequeñas 150
Carne enlatada, jamón curado cocido,
espaldilla de cerdo curada cocida, carne
picada curada cocida,
en recipientes estañados 200
en otros recipientes 50
HIERRO
Caseína ácida comestible 0,0
Caseinatos comestibles 20,0 en productos
por
deshidra-
tados
pulverización
50,0 en
productos
deshidratados
por
cilindros
secadores
Aceites y grasas comestibles 5,0 virgen
1,5 no virgen
Jugos de frutas y hortalizas 15,0 (1)
Jugos concentrados de fruta 15,0 (1) en el
producto
reconsti
tuido
Néctares de fruta 15,0 (1)
Mantecas de cacao 2,0
Grasa de mantequilla 0,2
Emulsiones lácteas para untar,
pobres en grasa 1,5
Suero dulce en polvo y suero ácido
en polvo, de calidad alimentaria 20,0 en productos
deshidratados
por
pulveriza-
ción.
50,0 en
productos
deshidrata-
dos por
cilindros
secadores
Caseína de cuajo comestible 5,0
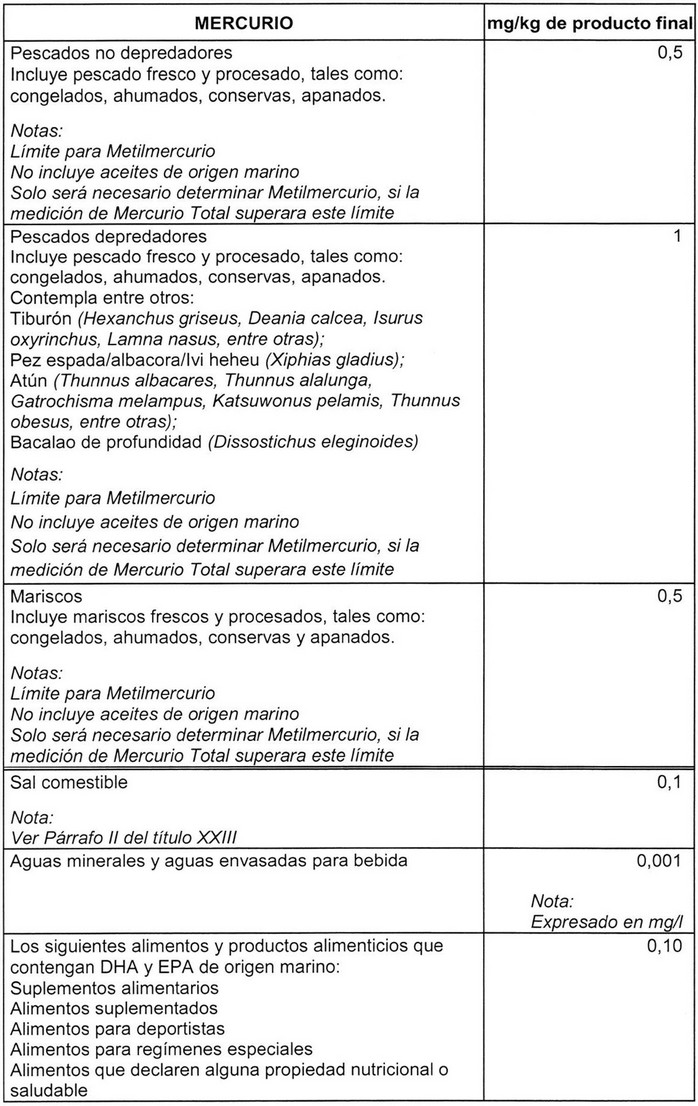
|
.
PLOMO
Caseína ácida comestible y
caseinatos comestibles 2,0
Conservas de frutas y hortalizas,
excepto concentrado de tomate 1,0
Concentrado de tomate 1,5
Aceitunas de mesa 1,0
Mantecas de cacao 0,5
Chocolate, chocolate compuesto y relleno 1,0
Chocolate no edulcorado 2,0
Aceites y grasas comestibles 0,1
Mayonesa 0,3
Azúcar blanca 1,0
Azúcar en polvo dextrosa (anhidra,
monohidrato, deshidratada),
jarabe de glucosa, lactosa 2,0
Fructosa 0,5
Caldos y sopas 1,0 en producto
seco
0,5 en producto
enlatado
Cacao en polvo y mezclas secas
de cacao y azúcar; cacao sin
cáscara ni germen; cacao en pasta;
torta de prensado de cacao,
polvillo de cacao (finos de cacao) 2,0
Dulce de manteca de cacao 1,0
Jugos de frutas y hortalizas,
excepto limón 0,3
Jugo de limón 1,0
Jugos concentrados de fruta 0,3 en el
producto
reconsti-
tuido
Néctares de fruta, excepto damasco,
durazno, pera y guayaba 0,2
Néctares de damasco, durazno, pera
y guayaba 0,3
Emulsiones lácteas para untar,
pobres en grasa 0,1
Suero dulce en polvo y suero
ácido en polvo, de calidad alimentaria 2,0
Caseína de cuajo comestible 2,0
Carne enlatada, jamón curado cocido, 0,5
espaldilla de cerdo curada cocida, carne
picada curada cocida
Cereales, legumbres y leguminosas 0,5
Conservas de pescados y mariscos, 2,0
pescados y mariscos frescos, enfriados
y congelados
Sal comestible 2,0
Agua mineral de mesa 0,05
Otros productos 2,0
SELENIO
En productos líquidos 0,05
En productos sólidos 0,30
Agua mineral de mesa 0,01
ZINC
Jugos de frutas y hortalizas 5,0 (1)
Jugos concentrados de fruta 5,0 (1) en el
producto
reconsti-
tuido
Néctares de fruta 5,0 (1)
Agua mineral de mesa 5,0
Otros productos 100,0
(1) Total Zn, Fe y Cu: máximo 20 mg/kg
*Arsénico inorgánico
|
| Decreto 7, SALUD
Art. 1 N° 1
D.O. 13.07.2018 |
| DTO 475, SALUD
Art. Unico, N° 41
D.O 13.01.2000 |
| DTO
475, SALUD
Art. Unico, Nº 41
D.O. 13.01.2000 |
| Decreto
7, SALUD
Art. 1 N° 2
D.O. 13.07.2018 |
| DTO
475, SALUD
Art. Unico, Nº 41
D.O. 13.01.2000 |
| DTO
475, SALUD
Art. Unico, Nº 41
D.O. 13.01.2000 |
| DTO
475, SALUD
Art. Unico, Nº 41
D.O. 13.01.2000 |
| DTO 475, SALUD
Art. Unico, Nº 41
D.O. 13.01.2000 |
|
Artículo 161.- En el caso de que antecedentes
sanitarios y técnicos hagan conveniente introducir
modificaciones a las listas establecidas en el artículo
precedente, el Ministerio de Salud propondrá el
correspondiente decreto supremo modificatorio al Presidente
de la República.
|
|
Párrafo II
De los residuos de plaguicidas
|
| Decreto 64, SALUD
Art. 1 Nº 2
D.O. 11.12.2009 |
|
Artículo 162.- El Ministerio de Salud mediante
la dictación de la correspondiente
norma técnica determinará las tolerancias de residuos de
plaguicidas permitidos en los alimentos.
|
| Decreto 64, SALUD
Art. 1
D.O. 11.12.2009 |
| DTO 475, SALUD
Art. Unico, Nº 42
D.O. 13.01.2000 |
|
Párrafo III
De los radionucleidos
|
| Decreto 64, SALUD
Art. 1
D.O. 11.12.2009 |
|
Artículo 163.- Para los fines de este Reglamento se
entenderá por:
Becquerel (Bq): unidad de actividad, equivale a una
desintegración por segundo de cualquier radionucleido.
Sievert (Sv): unidad de dosis equivalente. Es la dosis
absorbida ponderada que equivale a la energía entregada por
la radiación por gramo de sustancia irradiada.
Nivel de referencia de dosis (NRD): dosis equivalente
anual.
Corresponde a 1mSv/año.
Factor de conversión de dosis (FCD): factor que
relaciona la dosis equivalente por unidad de actividad
ingerida. Se expresa en Sv/Bq.
Tasa de consumo de alimento (TCA): masa promedio de
alimento que se consume anualmente per cápita en el país.
Se expresa en kg/año.
Nivel de intervención derivado (NID): concentración
de un radionucleido en un alimento dado. Se calcula
dividiendo el nivel de referencia de dosis por el factor de
conversión de dosis y por la tasa de consumo de alimentos.
Se expresa en Bq/kg.
|
|
Artículo 164.- El control de los niveles de
intervención derivados (NID) deberá efectuarse en aquellos
alimentos contaminados por radionucleidos liberados en un
accidente nuclear o radiológico y no, a los que se
encuentran naturalmente presentes formando parte del fondo
radiológico ambiental.
|
|
Artículo 165.- Los radionucleidos de interés se
clasifican en tres grupos de acuerdo a su radioactividad,
cuyos valores de conversión de dosis (FCD) son los
siguientes:
FCD FCD
leches y
otros
fórmulas alimentos
lácteos
I.- ( a ) Americio (241Am) 10-5 10-6
Plutonio (239Pu)
Otros actínidos
II.- ( ß ) Estroncio (90Sr) 10-7 10-7
Estroncio (89Sr)
Otros emisores beta
III.-( Y ) Yodo (131I) 10-8
10-8
Cesio (134Cs)
Cesio (137Cs)
| NOTA: El Art.
transitorio del DTO 214, Salud, publicado el 04.02.2006,
dispuso que la modificación introducida al presente
artículo rige a contar de 180 días desde su publicación.
|
|
| DTO 214, SALUD
Art. primero II Nº3
D.O. 04.02.2006 |
| DTO 475, SALUD
Art. Unico, Nº 44
D.O. 13.01.2000 |
|
Artículo 166.- La contaminación por radionucleidos no
sobrepasará los niveles de intervención derivados (NID)
por grupos de alimentos que se indican:
Grupo I( ) Grupo II( ß) Grupo III( )
(Bq/kg) (Bq/kg) (Bq/kg)
Grupos de
alimentos
Cereales 6 60 600
Raíces y
tubérculos 20 200 2000
Vegetales 15 150 1500
Frutas 15 150 1500
Carne 30 300 3000
Pescado 35 350 3500
Productos lácteos 10 100 1000
Leches 10 Bq/L 100 Bq/L 1000
Bq/L
Fórmulas para
lactantes 1 Bq/L 10 Bq/L 100
Bq/L
| NOTA: El Art.
transitorio del DTO 214, Salud, publicado el 04.02.2006,
dispuso que la modificación introducida al presente
artículo rige a contar de 180 días desde su publicación.
|
|
| DTO 214, SALUD
Art. primero II Nº5
D.O. 04.02.2006 |
|
Artículo 167.- Para efectos de cálculo de la
contaminación de las leches y fórmulas para lactantes el
131I se considera como perteneciente al grupo II. Los
valores de NID tanto para las leches fluidas, leches
en polvo como para las fórmulas para
lactantes se expresan en Bq/L del producto listo para el
consumo.
| NOTA: El Art.
transitorio del DTO 214, Salud, publicado el 04.02.2006,
dispuso que las modificaciones introducidas al presente
artículo rigen a contar de 180 días desde su publicación.
|
|
| DTO 214, SALUD
Art. primero II Nº6
D.O. 04.02.2006 |
|
Artículo 168.- Los niveles de intervención derivados
señalados en el artículo 166 se han calculado sobre la
base de un alimento contaminado con sólo un radionucleido.
Si más de una categoría de alimento está contaminada y/o
si hay varios radionucleidos presentes, la autoridad
competente establecerá nuevos NID, de acuerdo a la
metodología recomendada internacionalmente.
|
|
Párrafo IV
De las micotoxinas
|
| Decreto 64, SALUD
Art. 1 Nº 4
D.O. 11.12.2009 |
|
Artículo 169.- Las micotoxinas que se indican
a continuación no podrán sobrepasar
los siguientes límites:
.
.
| NOTA El artículo 2º
del Decreto 22, Salud, publicado el 05.10.2013, indica que
el presente decreto entrará en vigencia en el plazo de doce
meses, contado desde su publicación, con excepción de lo
establecido para aflatoxinas totales, aflatoxinas M1 y
Zearalenona que entrarán en vigencia desde su
publicación. |
|
| Decreto 22, SALUD
Art. 1 Nº1
D.O. 05.10.2013 |
|
Párrafo V De otros contaminantes y residuos
|
| Decreto 64, SALUD
Art. 1 Nº 5
D.O. 11.12.2009 |
|
Artículo 170.- Los contenidos máximos de Dioxinas
y Bifenilos Policlorados Coplanares
(PCBs) en los alimentos que a continuación se indican son
los siguientes:
Contenido Máximo de
Alimento Dioxinas y PCBs Unidad
coplanares
Carne de cerdo y 2,0 (pg EQT/OMS/g
productos derivados de grasa)
Carne de ave y 3,5 (pg EQT/OMS/g
productos derivados de grasa)
Carne de bovino y ovino 6,0 (pg EQT/OMS/g
y productos derivados de grasa)
Pescados y productos 2,0 (pg EQT/OMS/g de
derivados peso fresco)
Huevos y productos 3,0 (pg EQT/OMS/g de
derivados grasa)
Leche y productos 6,0 (pg EQT/OMS/g de
derivados grasa)
Para los efectos de este reglamento se entiende por:
- Dioxinas: Familia de compuestos clorados relacionados
entre sí desde el punto de vista estructural y químico,
constituida por Dibenzo-para-dioxinas policloradas (PCDD) y
Dibenzofuranos policlorados (PCDF).
- Bifenilos Policlorados Coplanares: Algunos PCBs que
poseen propiedades tóxicas similares a las dioxinas.
- Equivalencia Tóxica (EQT): valor relativo calculado
multiplicando la concentración de un compuesto análogo a
las dioxinas por el factor de equivalencia tóxica (FET).
- EQT/OMS: Equivalencia Tóxica de la Organización
Mundial de Salud para Dioxinas y PCBs coplanares, basada en
factores de equivalencia tóxica (FET).
- Factor de Equivalencia Tóxica (FET): estimaciones de
la toxicidad de compuestos análogos a las dioxinas en
relación con la toxicidad de
2,3,7,8-Tetraclorodibenzo-p-dioxina (TCDD), a la que se
asigna un FET de 1.
Tabla de Factores de Equivalencia Tóxica
Compuesto (congénere) Abreviatura FET
Dibenzodioxinas Policloradas
2,3,7,8-Tetraclorodibenzodioxina TCDD 1
1,2,3,7,8-Pentaclorodibenzodioxina 1,2,3,7,8-PeCDD 1
1,2,3,4,7,8-Hexaclorodibenzodioxina 1,2,3,4,7,8-HxCDD0 . 1
1,2,3,6,7,8-Hexaclorodibenzodioxina 1,2,3,6,7,8-HxCD D0. 1
1,2,3,6,7,9-Hexaclorodibenzodioxina 1,2,3,6,7,9-HxCDD 0.1
1,2,3,4,6,7,8
Heptaclorodibenzodioxina 1,2,3,4,6,7,8-HxCDD0.01
Octaclorodibenzodioxin OCDD 0.0001
Dibenzofuranos Policlorados
2,3,7,8-Tetraclorodibenzofurano 2,3,7,8-TCDF 0.1
1,2,3,7,8-Pentaclorodibenzofurano 1,2,3,7,8-PeCDF 0.05
2,3,4,7,8-Pentaclorodibenzofurano 2,3,4,7,8-PeCDF 0.5
1,2,3,4,7,8-Hexaclorodibenzofurano 1,2,3,4,7,8-HxCDF 0.1
1,2,3,6,7,8-Hexaclorodibenzofurano 1,2,3,6,7,8-HxCDF 0.1
1,2,3,7,8,9-Hexaclorodibenzofurano 1,2,3,7,8,9-HxCDF 0.1
2,3,4,6,7,8-Hexaclorodibenzofurano 2,3,4,6,7,8-HxCDF 0.1
1,2,3,4,6,7,8-Heptaclorodibenzofurano
1,2,3,4,6,7,8-HpCDF 0.01
1,2,3,4,7,8,9-Heptaclorodibenzofurano
1,2,3,4,7,8,9-HpCDF 0.01
Octaclorodibenzofurano OCDF 0.0001
Bifenilos policlorados "no-orto"
3,3',4',4'-Tetraclorobifenilo 3,3',4,4'-TCB 0.0001
3,4,4',5,-Tetraclorobifenilo 3,4,4',5-TCB 0.0001
3,3',4,4',5-Pentaclorobifenilo 3,3',4,4',5-PeCB 0.1
3,3',4,4',5,5'-Hexaclorobifenilo 3,3',4,4',5,5'-HxCB 0.01
Bifenilos policlorados "mono-orto"
2,3,3',4,4'-Pentaclorobifenilo 2,3,3',4,4'-PeCB 0.0001
2,3,4,4',5-Pentaclorobifenilo 2,3,4,4',5-PeCB 0.0005
2,3',4,4',5-Pentaclorobifenilo 2,3',4,4',5-PeCB 0.0001
2,3',4,4',5'-Pentaclorobifenilo 2,3',4,4',5'-PeCB 0.0001
2,3,3',4,4',5-Hexaclorobifenilo 2,3,3',4,4',5-HxCB 0.0005
2,3,3',4,4',5'-Hexaclorobifenilo 2,3,3',4,4',5'-HxCB0.0005
2,3',4,4',5,5'-Hexaclorobifenilo
2,3',4,4',5,5'-HxCB0. 00001
2,3,3',4,4',5,5'-Heptaclorobifenilo
2,3,3',4,4',5,5'-HpCB 0.00001
|
| Decreto 64, SALUD
Art. 1 Nº 6
D.O. 11.12.2009 |
|
Artículo 170 bis.- El contenido de Tetrahidrocannabinol (THC) en la
semilla de cáñamo utilizada para la alimentación humana y
los alimentos en base a cáñamo no deberá ser superior a:
a) Aceite de cáñamo 10,0 mg/Kg
b) Semilla de cáñamo entera 5,0 mg/Kg
c) Semilla de cáñamo sin cáscara 2,5 mg/Kg
d) Harina o proteína de cáñamo 3,5 mg/Kg
|
| Decreto 80,
SALUD
Art. 1° Nº 1)
D.O. 25.09.2023 |
|
TITULO V
De los criterios microbiológicos
|
|
Párrafo I
Definiciones
|
|
Artículo 171.- Para los fines del presente reglamento
se entenderá por:
a) criterio microbiológico: el valor o la gama de valores
microbiológicos, establecidos mediante el empleo de
procedimientos definidos, para determinar la aceptación o
rechazo del alimento muestreado;
b) parámetro microbiológico: los análisis
microbiológicos específicos practicados a cada alimento,
tales como, microorganismos indicadores, microorganismos
patógenos, toxinas, etc.;
c) indicador microbiológico: a los microorganismos no
patógenos pero frecuentemente asociados a éstos,
utilizados para reflejar el riesgo de la presencia de
agentes productores de enfermedades;
d) severidad del muestreo: el rigor que se aplicará al
muestreo. Depende del grado de riesgo para la salud y
condiciones de uso posterior del alimento. Determina los
planes de muestreo con respecto al número de unidades de
muestras a ser examinadas (n), a la cantidad máxima de
unidades defectuosas que puede contener la muestra (c) y al
tipo de plan, 2 o 3 clases;
e) plan de muestreo: el procedimiento en que se estipula
el tamaño de la muestra (n), y el criterio de aceptación o
rechazo (c), de forma que pueda tomarse una decisión
respecto a si se debe aceptar o rechazar el alimento
inspeccionado, basándose en los resultados del
análisis;
f) plan de 2 clases: un plan de muestreo, por atributos,
donde la calidad de un producto de acuerdo con los criterios
microbiológicos puede dividirse en dos grados de calidad,
"aceptable" y "rechazable", basado en comprobar la presencia
o ausencia de microorganismos, o si la tasa microbiológica
es superior o inferior a un nivel crítico establecido (c).
Un plan de 2 clases queda descrito por n y c;
g) plan de 3 clases: un plan de muestreo, por atributos,
donde la calidad de un producto, de acuerdo con los
criterios microbiológicos puede dividirse en tres grados de
calidad, "aceptable", "medianamente aceptable" y
"rechazable". La clase aceptable tiene como límites 0 y m;
la clase medianamente aceptable tiene como límites m y M, y
la rechazable aquellos valores superiores a M. Un plan de
tres clases queda descrito por n, m, M y c;
h) n = número de unidades de muestras a ser examinadas;
i) m = valor del parámetro microbiológico para el cual o
por debajo del cual el alimento no representa un riesgo para
la salud;
j) c = número máximo de unidades de muestra que
puede contener un número de
microorganismos comprendidos entre ''m'' y ''M'' para que el
alimento sea aceptable;
k) M = valor del parámetro microbiológico por encima del
cual el alimento representa un riesgo para la salud.
l) categoría de riesgo: la relación entre el grado
de peligrosidad que representa el
alimento para la salud en relación con las condiciones
posteriores de manipulación.
|
| DTO 475, SALUD
Art. Unico, Nº 45
D.O.13.01.2000 |
| DTO 475, SALUD
Art. Unico, Nº 45
D.O. 13.01.2000 |
| DTO 475, SALUD
Art. Unico, Nº 45
D.O.13.01.2000 |
|
Párrafo II
Disposiciones generales
|
|
Artículo 172.- Para los fines del presente reglamento,
se definen los criterios microbiológicos tomando como base
la clasificación, los parámetros de control y planes de
muestreo de la ICMSF ( International Commission on
Microbiological Specification for Foods ), adaptados a la
realidad nacional. De este modo:
a) se establecen los parámetros microbiológicos que se
controlarán en los distintos grupos de alimentos:
microorganismos indicadores, microorganismos patógenos,
toxinas, etc.;
b) se clasifican los alimentos, según:
- los factores de riesgo que éstos presentan y que
dependen de: sus características, tales como,
composición, pH, acidez, actividad de agua, etc.;
- grupo consumidor a quien va dirigido: adultos,
niños, lactantes, personas sensibles y otros grupos
de alto riesgo;
- la forma de preparación y consumo: consumo directo,
reconstituido, rehidratado, cocinado, etc.;
- la forma de mantención y conservación;
c) se configuran 15 categorías para los alimentos, de
acuerdo a la clase de peligro determinado por variables
propias y por aquellas relacionadas a las condiciones de
manipulación y consumo. Estas categorías se presentan en
la siguiente tabla:
Categorías de riesgo
Clase de peligro Condiciones normales en las que se
supone será manipulado y consumido
el alimento tras el muestreo
Grado de Sin cambio Aumenta la
peligrosidad de peligrosidad
reducido peligrosidad
Sin peligro Categoría 1 Categoría 2 Categoría 3
directo para 3 clases 3 clases 3 clases
la salud. n=5 c=3 n=5 c=2 n=5 c=1
(contaminación
general,
vida útil y
alteración)
Peligro para Categoría 4 Categoría 5 Categoría 6
la salud bajo, 3 clases 3 clases 3 clases
indirecto n=5 c=3 n=5 c=2 n=5 c=1
Moderado, Categoría 7 Categoría 8 Categoría 9
directo, 3 clases 3 clases 3 clases
difusión n=5 c=2 n=5 c=1 n=5 c=1
limitada
Moderado, Categoría 10 Categoría 11 Categoría 12
directo, 2 clases 2 clases 2 clases
difusión n=5 c=0 n=10 c=0 n=20 c=0
potencialmente
extensa
Grave, directo Categoría 13 Categoría 14 Categoría 15
2 clases 2 clases 2 clases
n=15 c=0 n=30 c=0 n=60 c=0
- en las categoría 1, 2 y 3 se usan parámetros que
tienen por objetivo definir la vida útil y alteración del
producto como recuento de microorganismos aeróbios
mesófilos ( RAM), mohos y levaduras, lactobacillus, etc.;
- en las categorías 4, 5 y 6 se usan como parámetros,
microorganismos indicadores tales como coliformes totales,
enterobacteriaceas, etc.;
- en las categorías 7, 8 y 9 se usan como parámetros
microorganismos que siendo considerados patógenos, en bajos
niveles pueden aceptarse, tales como, S. aureus, B. cereus.
- a partir de la categoría 10 se considera peligrosa
para la salud la presencia y/o concentración de ciertos
microorganismos como Salmonella, C. botulinum, entre otros patógenos;
d) se establecen planes de muestreo, que puedan ser de 2
tipos: plan de 2 clases y plan de 3 clases;
e) se establecen límites microbiológicos de acuerdo a
las recomendaciones internacionales (ICMSF);
f) se definen 18 grupos de alimentos según su origen
y/o tecnología aplicada en su elaboración. Estos son:
- grupo N° 1 Leches y productos lácteos
- grupo N° 2 Helados y mezclas para helados
- grupo N° 3 Productos grasos
- grupo N° 4 Caldos, sopas, cremas y
mezclas
deshidratadas
- grupo N° 5 Productos elaborados a partir de
cereales
- grupo N° 6 Azúcares y miel
- grupo N° 7 Productos de confitería
- grupo N° 8 Productos de panadería y pastelería
- grupo N° 9 Alimentos de uso infantil
- grupo N° 10 Carnes y productos cárneos
- grupo N° 11 Pescados y productos de la pesca
- grupo N° 12 Huevos y ovoproductos
- grupo N° 13 Salsas, aderezos, especias y condimentos
- grupo N° 14 Frutas y verduras
- grupo N° 15 Comidas y platos preparados
- grupo N° 16 Bebidas
- grupo N° 17 Estimulantes y fruitivos
- grupo N° 18 Conservas.
| NOTA: El Art.
transitorio del DTO 214, Salud, publicado el 04.02.2006,
dispuso que la modificación introducida al presente
artículo rige a contar de 180 días desde su publicación.
|
|
| DTO 475, SALUD
Art. Unico, Nº 46
D.O. 13.01.2000 |
| DTO 475, SALUD
Art. Unico, N° 1
D.O. 13.01.2000 |
| DTO
214, SALUD
Art. primero II Nº7
D.O. 04.02.2006 |
|
Párrafo III
Especificaciones microbiológicas por grupo de alimentos
|
|
Artículo 173.- Si en un alimento se detecta
la presencia de microorganismos
patógenos no contemplados en la lista indicada a
continuación, la autoridad sanitaria podrá considerarlo
alimento contaminado, conforme a la evaluación de los
riesgos que de su presencia se deriven.
Para los microorganismos incluidos en esta lista los
alimentos deberán cumplir con los requisitos
microbiológicos que en ella se
indican:
.
.
.
.
b) en caso de enfermedades transmitidas por alimentos,
especialmente en la investigación de la etiología de
toxi-infecciones se deben obtener todos los restos de
alimentos sospechosos. Los análisis microbiológicos a
realizar estarán de acuerdo a los antecedentes clínicos y
epidemiológicos del brote;
c) en los casos en que no se pueda obtener el número
establecido de unidades de muestras que se define en este
artículo 173 se aplicará el siguiente criterio de
calificación:
si n es igual o menor que 4 unidades de muestra, el
valor de los indicadores, recuento de aerobios mesófilos
(RAM), enterobacteriaceas, coliformes, etc., no deberá
sobrepasar el valor de M en ninguna de las unidades de
muestra y deberá cumplir con los valores de c establecidos
en este artículo. Para los microorganismos que representen
riesgo para la salud el valor no deberá exceder m.
| NOTA : El numeral 47
del Decreto 475, Salud, publicado el 13.01.2000, modifica el
cuadro inserto en el presente artículo de la siguiente
forma: En primer lugar, dispone modificar en la letra a) los
puntos 1.3; 1.6; 1.7; 1.8; 1.9; 1.10; 1.11; 10.3; 13.2; 14.3
y 16.3. Asimismo, modifica los siguientes puntos 1.4; 1.12;
2.1; 2.4; 3.1; 4.3; 4.4; 5.1; 5.2; 6.2; 8.2. Además, en el
número 9, incorpora los siguientes puntos 9.3. y 9.4.
nuevos, a continuación del punto 9.2. Finalmente, modifica
los siguientes puntos: 10.1; 10.2; 10.4; 10.6; 11.3; 12.1;
12.2; 13.1; 13.3; 14.1; 15.1; 17.1 y 17.2 de la manera que
la citada norma indica. |
| NOTA
1 El numeral 11 del Decreto 68, Salud,
publicado el 23.01.2006, modifica el cuadro inserto en el
presente artículo, en el sentido de reemplazar en los
puntos 6.1. y 7.2. la palabra "Azúcar" por "Azúcares".
Asimismo, el numeral 11, letra a) sustituye el punto 1.9; la
letra b) sustituye el punto 8.2; la letra c) sustituye el
punto 9, reemplaza el punto 9.1, 9.2, 9.3, 9.4 e incorpora
el punto nuevo 9.5; la letra d) sustituye el punto 10.3; la
letra e) sustituye el punto 10.4; la letra f) sustituye el
punto 13.3; la letra g) sustituye el punto 14, reemplaza el
14.1, 14.2, 14.3, 14.4, 14.5 e incorpora los puntos nuevos
14.6, 14.7, 14.8 y 14.9; la letra h) sustituye el punto
15.1; la letra i) sustituye el punto 15.2; la letra j)
agrega el nuevo punto 15.3; la letra k) modifica el punto
16; la letra l) modifica el punto 16.3; la letra m)
sustituye el punto 16.4, de la manera que la citada norma
indica. |
| NOTA 2
El numeral 8 del número II del artículo primero del
Decreto 214, Salud, publicado el 04.02.2006, modifica el
cuadro inserto en el presente artículo de la manera
siguiente: En el punto 1 sustituye la palabra "Leche" por
"Leches"; en el punto 1.1 reemplaza la expresión "Leche
Cruda" por "Leches Crudas"; en el punto 1.5 sustituye la
expresión "Leche Evaporada" por "Leches Evaporadas"; en el
punto 1.6 reemplaza la expresión "Leche Condensada
Azucarada" por "Leches Condensadas Azucaradas"; en los
puntos 1.2., 1.4., 2.1., y 2.2. sustituye la palabra "Leche"
por "Leches" y en el primer asterisco (*) de los puntos 2.4,
4.3., y 4.4. reemplaza la palabra "leche" por
"leches". |
| NOTA 3
El numeral 21 del artículo 1 del Decreto 106, Salud,
publicado el 23.04.2009 modifica el cuadro inserto en el
presente artículo, en el sentido de eliminar el parámetro
correspondiente a las enterobacteriaceas contenido en el
punto 5.1 Harinas y
Almidones. |
| NOTA 4
Los numerales 1 y 2 del artículo 1 del Decreto 21,
Salud, publicado el 05.10.2013, modifican el cuadro inserto
en el presente artículo, en el sentido de reemplazar los
puntos 14.2 y 14.3, respectivamente, por aquellos que la
citada norma indica. |
| NOTA
5 El numeral 2 del Artículo 1 del Decreto
15, Salud, publicado el 02.08.2017, modifica el cuadro
inserto en el presente artículo, en el sentido de
reemplazar el punto 14.2 e incorporar el 14.2.1 nuevo, de la
manera que el citada norma indica. Asimismo, el numeral 3,
reemplaza la Nota (*) contemplada al pie del punto 15.2 del
referido cuadro, por la siguiente: "(*) Excepto con
ingredientes fermentados o madurados con cultivos
bacterianos y/o vegetales crudos de las tablas 14.1 y 14.2
del presente artículo." |
| NOTA
6 El numeral 2 del artículo 1 del Decreto
31, Salud, publicado el 28.10.2017, modifica el cuadro
inserto en el presente artículo en el sentido de sustituir
el punto 9.1 de la manera que la citada norma
indica. |
|
| DTO 475, SALUD
Art. Unico, Nº 47
D.O.13.01.2000 |
|
Párrafo IV De otros criterios
microbiológicos
|
| Decreto 63, SALUD
Art. 1 Nº 2
D.O. 11.12.2009 |
|
Artículo 174.- En los alimentos Listos Para el
Consumo (LPC) se considera que no favorecen
el desarrollo de Listeria monocytogenes cuando cumplen
alguno de los siguientes parámetros:
1. pH menor o igual a 4,4;
2. actividad de agua (aw) menor o igual a 0,92;
3. combinación de pH y aw, con pH menor o igual de 5,0
y con aw, menor o igual a 0,94;
4. congelación, siempre que esta condición se
mantenga durante todo el período, hasta antes de ser
consumido;
5. vida útil en refrigeración por un lapso de menos
de 5 días.
Los alimentos LPC que no cumplan los parámetros
anteriores se considera que favorecen el desarrollo de
Listeria monocytogenes.
Criterios microbiológicos para Listeria monocytogenes
Excepcionalmente, para alimentos que favorecen el
desarrollo de Listeria monocytogenes, se aplicará el
criterio de aquellos alimentos que no favorecen su
desarrollo, cuando el fabricante o el productor, sea capaz
de garantizar y demostrar, a través de la aplicación de
tecnologías, que el producto no superará el límite de
100ufc/g durante su vida útil. Esta situación deberá ser
demostrada, en su caso, ante la autoridad sanitaria.
|
| Decreto 63, SALUD
Art. 1 Nº 3
D.O. 11.12.2009 |
|
TITULO VI
De la irradiación de alimentos
|
|
Párrafo I
Disposiciones generales
|
|
Artículo 175.- Las presentes disposiciones se
aplican a todas las instalaciones de
irradiación de alimentos y a todos los alimentos
irradiados. No se aplican a los alimentos expuestos a las
dosis emitidas por los instrumentos de medición utilizados
con fines de inspección. Sólo se podrá tratar con
energía ionizante los tipos de alimentos que determine el
Ministerio de Salud, cuando obedezca a necesidades de
carácter técnico o de higiene alimentaria. Se aplicará
básicamente para la inhibición de bulbos y tubérculos,
desinfección, desparasitación, retardo de la maduración y
reducción y/o eliminación de carga microbiana, saprófita
o patógena. Mediante resolución del Ministerio de Salud,
se establecerá la finalidad del proceso y la dosis media
que podrá recibir el respectivo alimento de acuerdo a la
finalidad autorizada. Esta tecnología no podrá ser usada
como sustituto de buenas prácticas de producción y/o
fabricación de los alimentos. La preservación de
alimentos por medio de radiación ionizante deberá atenerse
a las disposiciones de este reglamento relativas a la
seguridad microbiológica. Los materiales de empaque deben
ser apropiados para la irradiación y adecuados para
impedir la reinfestación, la recontaminación o el
deterioro del producto durante su almacenamiento y
transporte.
|
| DTO 475, SALUD
Art. Unico, Nº 48
D.O. 13.01.2000 |
| DTO 475, SALUD
Art. Unico, Nº 48
D.O. 13.01.2000 |
|
Artículo 176.- Los controles de calidad habituales, en
todas las etapas desde la producción al consumo, son de
responsabilidad del que solicita la preservación de estos
productos por energía ionizante. La ejecución y control
del proceso de irradiación será de responsabilidad de la
planta que aplique esta tecnología.
|
|
Párrafo II
Definiciones
|
|
Artículo 177.- Para los fines de este reglamento, se
entenderá por:
Energía ionizante: aquellas formas de radiación
ionizante que se señalan a continuación;
- Rayos gamma de los radionucleidos Co-60 o Cs-137
- Rayos X generados por máquinas que trabajen a
energías de 5
Mev o inferiores
- Electrones generados por máquinas que trabajen a
energías
de 10 Mev o inferiores.
Gray (Gy): Unidad de dosis absorbida equivalente a 1
Joule
por kilogramo
Rad : Unidad de dosis absorbida equivalente a
100 erg
por gramo
1 Gray = 100 rad
Dosis absorbida: la cantidad de energía
expresada en Joules, absorbida por un kilo de
producto sometido a tratamiento con radiación.
Dosis absorbida media global de 10 kGy: la dosis
promedio de radiación absorbida por el alimento, con la
condición de que por lo menos el 97.5% de la fracción de
masa del producto alimenticio reciba una dosis absorbida
menor de 15 kGy.
Lote o tanda de alimento irradiado: una cantidad de
alimento irradiado en las mismas condiciones y durante la
misma operación.
Alimento irradiado: cualquier alimento que haya sido
sometido a tratamiento con radiación ionizante.
Instalación de irradiación de alimentos: son los
establecimientos autorizados por los organismos competentes,
para irradiar alimentos.
Dosimetría: la medición de la energía radiante
absorbida.
Trazabilidad: la propiedad del resultado de una
medición o de un patrón tal que pueda relacionarse con
referencias establecidas, generalmente con patrones
nacionales o internacionales, por medio de una cadena
ininterrumpida de comparaciones, teniendo todas las
incertidumbres determinadas.
|
| DTO 475, SALUD
Art. Unico, Nº 49
D.O. 13.01.200 |
|
Párrafo III
De las instalaciones y control del proceso
|
|
Artículo 178.- El tratamiento de los alimentos por
energía ionizante se llevará a cabo sólo en las
instalaciones que hayan obtenido la autorización
correspondiente de los organismos competentes. Las
instalaciones deben disponer de un sistema de control de calidad documentado que
facilite la realización de auditorías. Los productos que
ingresen al proceso de irradiación deben mantenerse
físicamente separados de los productos tratados. Cuando
proceda podrá fijarse un indicador visual de irradiación
por cambio de color a fin de facilitar el control. La
irradiación de alimentos, incluido un procedimiento
dosimétrico adecuado, debe efectuarse en conformidad con
los Códigos de Buenas Prácticas de Irradiación del Grupo
Consultivo Internacional de Irradiación de Alimentos
(GCIIA), establecido bajo el auspicio de la Organización de
las Naciones Unidas para la Alimentación y la Agricultura
(FAO), el Organismo Internacional de Energía Atómica
(OIEA) y la Organización Mundial de la Salud (OMS). La
dosimetría debe ser trazable a patrones nacionales e
internacionales.
|
| DTO 475,
SALUD
Art. Unico, Nº 50
D.O. 13.01.2000 |
|
Artículo 179.- El control de las instalaciones se
ejercerá de conformidad a la legislación vigente.
Los estudios dosimétricos se deberán efectuar antes
de la irradiación de cualquier producto alimenticio para
comprobar que el proceso se ajusta a las especificaciones de
dosis absorbida, establecidas para ese tipo de alimento por
el Ministerio de Salud. Además deberán hacerse mediciones
dosimétricas:
a) al entrar en servicio una planta;
b) cada vez que se utilice un nuevo proceso de
irradiación;
c) siempre que se modifique la intensidad o el tipo de la
fuente o la geometría fuente-producto.
|
|
Artículo 180.- En la irradiación de alimentos
se deberá llevar a cabo la dosimetría
en la siguiente forma:
a) medición exacta y precisa de la dosis absorbida por el
alimento;
b) determinación de la distribución de la dosis e
interpretación de la información;
c) mantenimiento de dosímetros para calibrar la respuesta
de los instrumentos de medición y/o vigilancia radiológica
usados habitualmente en la instalación;
d) observancia de los criterios de selección de
dosímetros prescritos en el programa de control de calidad,
con el fin de asegurar una dosimetría y/o vigilancia
radiológica precisa, apropiada y eficiente;
e) mantenimiento de documentación completa de la
dosimetría y empleo de listas de comprobación de todas las
fases de los procedimientos de dosimetría.
|
| DTO 475, SALUD
Art. Unico, Nº 51
D.O. 13.01.2000 |
|
Artículo 181.- En toda instalación o planta en que
se aplique energía ionizante a los
alimentos se deberá llevar un registro de cada lote o
tanda, el que deberá contener, a lo menos, la siguiente
información:
a) identificación del propietario del alimento a irradiar
o de su representante legal;
b) el tipo y la cantidad de alimentos en el lote o tanda
irradiados, incluyendo información acerca de si es natural
o ha sido previamente sometido a otros procedimientos de
preservación, sean físicos o químicos;
c) el número de serie del lote o tanda de alimentos
irradiados;
d) la fecha de irradiación;
e) tipo de empaque utilizado durante el tratamiento de
irradiación, cuando proceda;
f) controles y mediciones efectuadas durante el
tratamiento. Dosis mínima y máxima absorbidas,
certificados de dosimetría;
g) fuente utilizada para el tratamiento;
h) descripción del almacenamiento en la planta;
i) fecha de vencimiento del producto, posterior a su
tratamiento con fines de preservación;
j) resultados y observaciones de las inspecciones
establecidas en el artículo siguiente, cuando corresponda.
En las plantas de irradiación se deberá mantener
dicho registro, por un período mínimo de dos años a
disposición de la autoridad sanitaria.
|
| DTO 475, SALUD
Art. Unico, Nº 51
D.O.13.01.2000 |
|
Artículo 182.- Las instalaciones destinadas a la
preservación de alimentos por energía ionizante, serán
inspeccionadas periódicamente y a lo menos una vez al año,
por personal especializado de la institución encargada del
control, conforme a su reglamento. El resultado u
observaciones técnicas, fecha y nombre del inspector,
serán estipuladas en el registro de la instalación que
establece el artículo anterior y una copia será enviada a
la autoridad que concedió la licencia.
Los propietarios responsables de las instalaciones
destinadas a preservar alimentos por energía ionizante, no
podrán negar el acceso inmediato a los inspectores
debidamente autorizados por la institución encargada del
control, para que realicen sus funciones, ni el acceso al
registro que establece el artículo 181 bajo ningún
pretexto.
|
|
Párrafo IV
De los alimentos preservados por energía ionizante
|
|
Artículo 183.- Además de lo dispuesto para el
etiquetado general, todo alimento que haya sido tratado con
radiación o energía ionizante debe llevar en el rótulo o
etiqueta, muy cerca del nombre del alimento, una indicación
de dicho tratamiento empleando algunas de las siguientes
frases: "Tratado con energía ionizante", "Procesado con
energía ionizante", o "Preservado con energía ionizante".
Además puede llevar el logo o símbolo, reconocido
internacionalmente para estos efectos. Los alimentos no
empacados, destinados al consumo directo, deberán presentar la misma
información señalada en el inciso anterior en lugar
visible y sobre los alimentos de que se trate.
|
| DTO 475, SALUD
Art. Unico, Nº 52
D.O. 13.01.2000 |
|
Artículo 184.- Cuando más del 5% de un
producto corresponda a materias irradiadas, la
etiqueta deberá contener una declaración que indique el
tratamiento.
Se prohíbe repetir la irradiación de los alimentos.
No se considerará repetición de la irradiación de un
alimento, cualquiera de los siguientes casos:
a) cuando se aplique para combatir la reinfestación por
insectos en alimentos de bajo contenido de humedad;
b) cuando los ingredientes fueron irradiados con otro fin
tecnológico;
c) cuando el alimento contiene menos de 5% de ingredientes
irradiados;
d) cuando el proceso de irradiación se haga en etapas
sucesivas, con un fin tecnológico concreto, y la suma de
las dosis parciales no supere la dosis completa de
radiación ionizante requerida para lograr el efecto
deseado.
En todos los casos, la dosis absorbida media global
acumulada no debe ser superior a 10 kGy.
|
| DTO 475, SALUD
Art. Unico, Nº 53
D.O. 13.01.2000 |
|
Artículo 185.- Todo alimento importado preservado por
energía ionizante deberá acreditar que la instalación
donde fue realizado el tratamiento está inscrita en el
Registro Internacional de Plantas para Irradiar Alimentos y
cualquier otro antecedente que compruebe que la tecnología
empleada en el país de origen es compatible con las normas
del presente reglamento.
|
|
TITULO VII
De la congelacion de los alimentos
|
|
Artículo 186.- Alimentos congelados son
aquellos, naturales o elaborados, que han sido
sometidos, mediante un equipo apropiado, a un proceso
térmico hasta que el producto alcance una temperatura de
-18°C en el centro térmico. En la rotulación de los
productos alimenticios congelados envasados que se expendan
al público en tal condición, se deberá indicar en forma
clara y legible la expresión "PRODUCTO CONGELADO", salvo
los helados comestibles definidos en el artículo 243.
|
| Decreto 23, SALUD
Art. 1 N° 1
D.O. 30.08.2016 |
|
Artículo 187.- Para reducir al mínimo la actividad
microbiológica, los alimentos precocidos destinados a la
congelación rápida, deberán enfriarse lo más
rápidamente posible en aparatos adecuados y someterse de
inmediato al proceso de congelación. Cuando ello no sea
posible el alimento deberá conservarse a una temperatura
superior a los 60ºC medido en el punto más frío del
producto hasta que pueda efectuarse el enfriamiento y la
subsiguiente congelación rápida.
|
|
Artículo 188.- Deberán adoptarse las medidas necesarias para evitar el aumento de
la temperatura después del proceso de congelación rápida
en la manipulación y durante el transporte a las cámaras
frigoríficas. En el caso de reenvasar un producto congelado
este procedimiento deberá realizarse en una sala
especialmente destinada a este fin, la que deberá disponer
de un dispositivo que permita mantener una temperatura no
superior a 8°C y de un sistema de registro permanente de
ésta.
|
| DTO
475, SALUD
Art. Unico, Nº 54
D.O. 13.01.2000 |
|
Artículo 189.- El almacenamiento de estos productos
deberá realizarse en cámaras frigoríficas cuya
temperatura se mantenga en -18ºC o inferior y con un
mínimo de fluctuación. Estas cámaras deberán disponer
de dispositivos que registren continuamente la temperatura.
|
|
Artículo 190.- El transporte interurbano de
alimentos congelados deberá efectuarse con
equipos capaces de mantener la temperatura del producto a
-18ºC o más baja. Los vehículos deberán estar provistos
de termómetros que permitan su lectura desde el exterior y
de dispositivos que registren las temperaturas durante el
transporte. Podrá tolerarse un aumento de la temperatura
del producto durante el transporte hasta -15ºC pero esta
situación deberá reducirse rápidamente sea durante el
transporte o inmediatamente después de la entrega.
|
| DTO 475, SALUD
Art. Unico, Nº 55
D.O. 13.01.2000 |
|
Artículo 191.- El transporte local de los alimentos
congelados destinados a la distribución a los minoristas
deberá efectuarse de tal manera que todo aumento de
temperatura del producto superior a -18ºC se mantenga por
el mínimo de tiempo y en ningún caso supere los -12ºC.
|
| DTO
475, SALUD
Art. Unico, Nº 56
D.O. 13.01.2000 |
|
Artículo 192.- Cuando los alimentos congelados
se ofrezcan a la venta en esta
condición deberán mantenerse en vitrinas congeladoras o
conservadoras destinadas a ese fin, las que deberán ser
capaces de mantener la temperatura del producto a -18°C y
estar provistas de termómetros. Se podrá tolerar, por
periodos breves, un aumento de la temperatura del producto
sin que sobrepase los -12°C.
Se podrán descongelar para su venta al consumidor
final siempre que el proceso de descongelación se realice
en establecimientos autorizados para elaborar alimentos, a
temperaturas adecuadas al producto y en condiciones de
higiene que garanticen la inocuidad del mismo, las que
deberán mantenerse hasta la venta. Respecto de estos
productos descongelados, se deberá observar estricto
cumplimiento de la totalidad de las obligaciones
establecidas en el presente reglamento para los alimentos
frescos o refrigerados, según corresponda a sus nuevas
condiciones de almacenamiento.
Se deberá indicar en la rotulación del envase del
producto descongelado o mediante un cartel junto a los
alimentos descongelados que se expendan a granel, la fecha
de elaboración original o lote de producción, la fecha de
descongelación y la fecha de vencimiento, de acuerdo a la
condición actual de producto descongelado. Además, en el
mismo rótulo o cartel, según corresponda, se deberá
indicar en forma clara y legible la expresión "PRODUCTO
DESCONGELADO. NO VOLVER A CONGELAR". Asimismo, deberán ser
informadas en el envase las nuevas condiciones de
almacenamiento del producto descongelado. Las informaciones
anteriores deberán ser aplicadas al rótulo por el
establecimiento descongelador, para lo cual, en el caso de
ser necesaria la sobreimpresión del etiquetado, no se
requerirá la autorización de la Autoridad Sanitaria,
contemplada en el artículo 109 del presente reglamento. Se
eximen de la obligación de informar la condición de
descongelado y la prohibición de volver a congelar
exclusivamente los productos de panadería, masas horneadas
o fritas, que no tengan relleno o estén rellenas con
algunos de los productos señalados en los Títulos XVIII y
XIX que se expendan a granel para su consumo inmediato.
|
| Decreto 23, SALUD
Art. 1 N° 2
D.O. 30.08.2016 |
|
Artículo 193.- Las vitrinas congeladoras o
conservadoras se instalarán de manera que la parte en que
se expone el producto no esté sometida a un calor
irradiante anormal (luz solar directa o proximidad de
elementos de calefacción). Estas vitrinas deberán
mantenerse cerradas y conectadas al suministro de
electricidad durante la noche y durante los días en que no
haya atención de público. Deberán programarse ciclos de
descongelación de tal forma que éstos se produzcan fuera
de las horas normales de venta, para poder acomodar los
productos en otras vitrinas congeladoras, sin que queden
expuestos a temperaturas superiores a las recomendadas por
el fabricante.
|
|
Artículo 194.- Las vitrinas congeladoras o
conservadoras no deberán cargarse por sobre la línea de
carga. Los productos no deberán retirarse de ellas y
volverse a colocar, salvo en caso de absoluta necesidad.
|
|
Artículo 195.- Los productos congelados sin envasar
deberán almacenarse y exponerse en compartimientos
separados de los que se utilicen para los alimentos
congelados envasados con el objeto de evitar riesgos de
contaminación y deshidratación.
|
|
Artículo 196.- Los establecimientos de expendio de
productos precocidos congelados a granel, deberán contar
con un manipulador encargado de fraccionar y envasar el
producto.
|
|
TITULO VIII
De las leches y productos lácteos
|
| DTO 214, SALUD
Art. primero II Nº9 |
|
Párrafo I
Disposiciones generales
|
|
Artículo 197.- Se regirán por las disposiciones del
presente reglamento la higienización, el transporte, la
industrialización, la distribución y el expendio de
las leches y de los productos lácteos.
| NOTA:
El Art. transitorio del DTO 214, Salud, publicado el
04.02.2006, dispuso que las modificaciones introducidas al
presente artículo rigen a contar de 180 días desde su
publicación.
|
|
| DTO 214, SALUD
Art. primero II Nº10
D.O. 04.02.2006 |
|
Artículo 198.- Leche es la secreción mamaria
normal exenta de calostro, de animales
lecheros, obtenida mediante uno o más ordeños, sin ningún
tipo de adición o extracción, destinada al consumo en
forma de leche líquida o a su elaboración ulterior.
Para efectos de etiquetado, leche sin otra
denominación, es el producto de la vaca. Las leches
provenientes de otros animales se denominarán según la
especie de la que proceden, como también los productos que
de ella se deriven
|
| Decreto 71, SALUD
Art. 1 N° 2
D.O. 06.03.2019 |
|
Artículo 199.- Pasteurización es el procedimiento por
el que se somete uniformemente la totalidad de las leches u otros productos lácteos a
una temperatura conveniente durante el tiempo necesario,
para destruir la mayor parte de la flora banal y la
totalidad de los gérmenes
patógenos, seguido de un enfriamiento rápido de las leches
o los productos lácteos así tratados.
| NOTA: El Art.
transitorio del DTO 214, Salud, publicado el 04.02.2006,
dispuso que la modificación introducida al presente
artículo rige a contar de 180 días desde su publicación.
|
|
| DTO
214, SALUD
Art. primero II Nº12
D.O. 04.02.2006 |
|
Artículo 200.- La pasteurización de la leche o
la aplicación de otros tratamientos
microbicidas para su higienización será obligatoria en
todo el país, como asimismo la de los productos derivados
de ella y mencionados en este Título destinados al consumo
humano, con la excepción señalada en el artículo 207.
|
| Decreto 71, SALUD
Art. 1 N° 3
D.O. 06.03.2019 |
|
Artículo 201.- Tratamiento a ultra alta
temperatura (UHT) es el procedimiento al que se
somete uniformemente la totalidad de las leches u otros
productos lácteos a una temperatura entre 130 y 145ºC
durante 2 a 4 segundos u otra combinación
tiempo-temperatura de tratamiento
equivalente.
| NOTA:
El Art. transitorio del DTO 214, Salud, publicado el
04.02.2006, dispuso que la modificación introducida al
presente artículo rige a contar de 180 días desde su
publicación.
|
|
| DTO 475, SALUD
Art. Unico, Nº 58
D.O. 13.01.2000
DTO 214, SALUD
Art. primero II Nº12
D.O. 04.02.2006 |
|
Artículo 202.- Esterilización es el procedimiento por
el que se somete uniformemente la totalidad de las leches u otros productos lácteos a
un proceso térmico en autoclave o equipo similar, por el
tiempo necesario para asegurar la ausencia de gérmenes
viables y esporas que germinen
en condiciones normales de almacenamiento.
| NOTA: El Art.
transitorio del DTO 214, Salud, publicado el 04.02.2006,
dispuso que la modificación introducida al presente
artículo rige a contar de 180 días desde su publicación.
|
|
| DTO
214, SALUD
Art. primero II Nº12
D.O. 04.02.2006 |
|
Artículo 203.- Las características de las
leches, serán las siguientes:
a) caracteres organolépticos normales;
b) exenta de materias extrañas;
c) exenta de sangre y pus;
d) exenta de antisépticos, antibióticos y
neutralizantes;
Los residuos de plaguicidas y otras sustancias nocivas
para la salud no deberán exceder los límites establecidos
por el Ministerio de Salud;
e) sus requisitos microbiológicos y su contenido de
materia grasa, serán los que determina este reglamento en
cada caso;
Además, en el caso específico de la leche de vaca,
las siguientes características:
f) peso específico: 1.028 a 1.034 a 20°C;
g) Índice crioscópico: -0,53 a -0,57 "Horvet" o
-0,512 a -0,550 °C".
h) pH: 6,6 a 6,8;
i) acidez: 12 a 21 ml de hidróxido de sodio 0,1 N/100 ml
de leche;
j) sólidos no grasos: 82,5 gramos por litro, como
mínimo.
| NOTA: El Art.
transitorio del DTO 214, Salud, publicado el 04.02.2006,
dispuso que la modificación introducida al presente
artículo rige a contar de 180 días desde su publicación.
|
|
| DTO 214, SALUD
Art. primero II Nº13
D.O. 04.02.2006 |
| Decreto 71, SALUD
Art. 1 N° 4
D.O. 06.03.2019 |
|
Párrafo II
De los requisitos de la leche
|
|
Artículo 204.- La leche se clasificará en:
a) leche natural es aquella que solamente ha sido
sometida a enfriamiento y estandarización de su
contenido de materia grasa antes del proceso de
pasteurización o tratamiento a ultra alta temperatura
(UHT) o esterilización;
b) leche reconstituida es el producto obtenido
por
adición de agua potable a la leche concentrada y a
la leche en polvo, en proporción tal, que cumpla
los requisitos establecidos en el artículo 203 y
su contenido de materia grasa corresponda a alguno
de los tipos de leche señalados en el artículo
205.
Deberá ser pasteurizada , sometida a tratamiento
UHT o esterilizada;
c) leche recombinada es el producto obtenido de la
mezcla de leche descremada, grasa de leche y agua
potable en proporción tal que cumpla los requisitos
del artículo 203 y su contenido de materia grasa
corresponda a alguno de los tipos de leche señalados
en el artículo 205. Deberá ser pasteurizada,
sometida
a tratamiento UHT o esterilizada.
|
| DTO
475, SALUD
Art. Unico, Nº 59
D.O. 13.01.2000 |
| DTO 165, SALUD
Art. Unico
D.O. 26.05.2000 |
| DTO 475, SALUD
Art. Unico, Nº 59
D.O. 13.01.2000 |
| DTO 475, SALUD
Art. Unico, Nº 59
D.O. 13.01.2000 |
|
Párrafo II
De los requisitos de la leche
|
|
Artículo 205.- De acuerdo a su contenido de
materia grasa láctea la leche se
clasificará en:
Eliminada
Leche entera es aquella con un contenido superior
a 30 g de materia grasa por litro.
Leche parcialmente descremada es aquella con un
contenido máximo de 30 g de materia grasa y un mínimo
superior a 5 g por litro.
Leche descremada es aquella con un contenido máximo
de hasta 5 gramos por litro de materia grasa.
| NOTA: El Art.
transitorio del DTO 214, Salud, publicado el 04.02.2006,
dispuso que la modificación introducida al presente
artículo rige a contar de 180 días desde su publicación.
|
|
| DTO 214, SALUD
Art. primero II Nº14
D.O. 04.02.2006 |
| DTO 475, SALUD
Art. Unico, Nº 60
D.O. 13.01.2000 |
|
Párrafo III
De la pasteurización de la leche
|
|
Artículo 206.- La leche cruda enviada a la planta por
el productor será sometida a lo menos a las siguientes
pruebas de control:
Pruebas de aceptación o rechazo:
a) eberán corresponder a las características estipuladas
en el artículo 203;
b) alcohol entre 68% v/v y 75% v/v".
En el caso de que la leche sea aceptada por la planta y deba ser sometida a
clasificación, podrán efectuarse las siguientes pruebas:
a) reductasa (azul de metileno) o recuento de
microorganismos totales en leches no refrigeradas;
b) recuento de microorganismos aerobios mesófilos y
psicrófilos en leches refrigeradas;
c) detección de inhibidores;
d) células somáticas.
|
| Decreto 71, SALUD
Art. 1 N° 5
D.O. 06.03.2019 |
| DTO
475, SALUD
Art. Unico, Nº 61
D.O. 13.01.2000 |
|
Párrafo III
De la pasteurización de la leche
|
|
Artículo 207.- Las leches crudas deberán ser
sometidas a tratamientos microbicidas, tales
como: pasteurización, temperatura ultra alta,
centrifugación, esterilización u otros, inmediatamente
después de su recepción en la planta o conservarse por
tiempos y temperaturas que impidan la multiplicación
bacteriana de modo de dar cumplimiento a lo dispuesto en los
artículos 61 y 62 del presente reglamento. Para lo
anterior, las plantas que reciban leche deberán mantener
registros sobre las validaciones realizadas que demuestren
que tales relaciones de tiempo-temperatura impiden la
multiplicación bacteriana y de las verificaciones del
cumplimiento de esos tiempos y temperaturas conforme a lo
dispuesto en el artículo 69 de este reglamento.
Se entiende por tratamientos microbicidas las medidas
de control que reducen sustancialmente o eliminan el número
de microorganismos presentes en los alimentos.
Los tratamientos microbicidas señalados anteriormente
no serán exigibles cuando los productores expendan leche
directamente al público en las condiciones señaladas en el
artículo 94 del presente reglamento".
|
| Decreto 71, SALUD
Art. 1 N° 6
D.O. 06.03.2019 |
|
Artículo 208.- Para el almacenamiento de las
leches, las plantas dispondrán de estanques
cerrados fijos que aseguren la conservación de la
temperatura, premunidos de termómetros o sensores de
temperatura para el control
correspondiente. Todo estanque, utensilio u otro elemento,
deberá ser de material inoxidable y no contaminante y de
fácil aseo y desinfección.
| NOTA: El Art.
transitorio del DTO 214, Salud, publicado el 04.02.2006,
dispuso que la modificación introducida al presente
artículo rige a contar de 180 días desde su publicación.
|
|
| DTO 214, SALUD
Art. primero II Nº12
D.O. 04.02.2006 |
|
Artículo 209.- Los equipos de pasteurización tendrán
dispositivos que verifiquen el correcto tratamiento de las
leches, entre otros, un termómetro que indique directamente la
temperatura de pasteurización y un termógrafo para
registrar la temperatura y el tiempo de
tratamiento.
Los gráficos de cada tratamiento deberán guardarse
durante seis meses, para su control por la autoridad
sanitaria.
| NOTA: El Art.
transitorio del DTO 214, Salud, publicado el 04.02.2006,
dispuso que la modificación introducida al presente
artículo rige a contar de 180 días desde su publicación.
|
|
| DTO 214, SALUD
Art. primero II Nº12
D.O. 04.02.2006 |
|
Artículo 210.- Se prohíbe la repasteurización de la
leche o leches devueltas o sobrantes alteradas. Estas leches no podrán ser
destinadas a la elaboración de alimentos de consumo
humano.
| NOTA:
El Art. transitorio del DTO 214, Salud, publicado el
04.02.2006, dispuso que la modificación introducida al
presente artículo rige a contar de 180 días desde su
publicación.
|
|
| DTO
214, SALUD
Art. primero II Nº16
D.O. 04.02.2006 |
|
Párrafo IV
Del envase, conservación y expendio de la leche
pasteurizada
|
|
Artículo 211.- Inmediatamente después de pasteurizada
las leches, deberán ser enfriadas a una temperatura no superior a 4°C,
envasadas y conservadas a esta misma temperatura hasta el
momento de su distribución, excepto las tratadas por el
proceso UHT.
Las leches pasteurizadas deberá dar la prueba de
fosfatasa negativa.
Toda la leche líquida, después de haber
sido sometida a los procesos térmicos señalados, que sea
usada como materia prima o para consumo directo, deberá ser
fortificada con vitamina D3 (colecalciferol) de la siguiente
manera:
- Leche líquida/fluida: Una dosis única de 1
µg/100ml, la que podrá excederse hasta en un 40%, llegando
a 1,4 µg/100ml.
La verificación de la fortificación de la leche
líquida se realizará en la leche fluida usada como materia
prima en otros alimentos, o bien, utilizada para el consumo
directo. En consecuencia, se excluirá la verificación de
fortificación a aquellos productos elaborados a partir de
la leche líquida o de sus subproductos.
| NOTA: El Art.
transitorio del DTO 214, Salud, publicado el 04.02.2006,
dispuso que la modificación introducida al presente
artículo rige a contar de 180 días desde su publicación.
|
|
| DTO 214, SALUD
Art. primero II Nº17
D.O. 04.02.2006 |
| Decreto 48, SALUD
Art. 1°, N° 1
D.O. 05.07.2022 |
|
Artículo 212.- Las plantas deberán vender las
leches pasteurizadas en envases
herméticamente cerrados y sellados para evitar su
contaminación. Estos envases deberán cumplir con los
requisitos establecidos en el
presente reglamento.
| NOTA: El Art.
transitorio del DTO 214, Salud, publicado el 04.02.2006,
dispuso que la modificación introducida al presente
artículo rige a contar de 180 días desde su publicación.
|
|
| DTO 214, SALUD
Art. primero II Nº18
D.O. 04.02.2006 |
|
Párrafo V
De los productos lácteos
|
|
Artículo 213.- Leche saborizada es el producto
obtenido a partir de la leche entera, parcialmente
descremada o descremada pasteurizada , sometida a tratamiento UHT o esterilizada, a
la que se ha adicionado saborizantes, aromatizantes,
edulcorantes y estabilizantes autorizados en el presente
reglamento con el objeto de obtener un producto con
caracteres organolépticos diferentes.
|
| DTO
475, SALUD
Art. Unico, Nº 62
D.O. 13.01.2000 |
|
ARTÍCULO 214. Leches concentradas son aquellas que
han sido privadas parcialmente de su
contenido de agua, se clasifican en:
a) Leche evaporada es el producto líquido obtenido por
eliminación parcial del agua de la leche.
b) Leche condensada es el producto proveniente de la
leche obtenido por evaporación parcial del agua, de
consistencia espesa que usualmente es de sabor dulce,
pudiendo tener adición de azúcares, edulcorantes,
polioles, fibras u otros ingredientes permitidos.
La acidez de las leches concentradas no excederá de 50
ml de hidróxido de sodio 0,1 N/100 g y la prueba de
fosfatasa deberá ser negativa.
|
| Decreto 82,
SALUD
Art. 1° N° 1
D.O. 26.01.2023 |
|
Artículo 215.- Sólo se podrá utilizar en la
elaboración de leches concentradas los siguientes aditivos: fosfato disódico, fosfato
tricálcico, citrato de sodio, cloruro de calcio y carbonato
de sodio, en dosis máxima del producto final de 2 g/kg,
solos o en combinación, y
expresados como sustancias anhidras; saborizantes y
colorantes autorizados. En la leche evaporada se podrá
utilizar, además, carragenina en una dosis máxima de 150
mg/kg.
| NOTA: El Art.
transitorio del DTO 214, Salud, publicado el 04.02.2006,
dispuso que la modificación introducida al presente
artículo rige a contar de 180 días desde su publicación.
|
|
| DTO
214, SALUD
Art. primero II Nº19
D.O. 04.02.2006 |
|
Artículo 216.- La leche en polvo y la crema o nata
de leche en polvo son los productos
obtenidos por la eliminación parcial del agua que contiene
la leche; contendrán un máximo de 5% de humedad, sin
considerar el agua de cristalización de la lactosa, y el
contenido mínimo de proteínas de la leche en el extracto
seco magro no deberá ser menor a 34% m/m incluyendo el agua
de cristalización de la lactosa.
Leche entera en polvo es aquella que contiene un
mínimo de 26% m/m de materia grasa de la leche.
Leche en polvo parcialmente descremada o semidescremada
es aquella que contiene más del 1,5% y menos del 26% m/m de
materia grasa de la leche.
Leche en polvo descremada es aquella que contiene un
máximo de 1,5% m/m de materia grasa de la leche.
La crema o nata en polvo deberá contener, como
mínimo, un 42% m/m de materia grasa de la leche.
El contenido de grasa y/o proteínas podrá ajustarse,
únicamente, para cumplir con los requisitos de composición
estipulados en este artículo, mediante incorporación y/o
extracción de los constituyentes de la leche, de manera que
no se modifique la proporción entre la proteína del suero
y la caseína de la leche utilizada como materia prima.
Podrá agregársele fluoruro bajo los límites que
señale la norma técnica que, para estos efectos, dicte el
Ministerio de Salud.
Toda la leche en polvo, que sea usada como
materia prima o para consumo directo, deberá ser
fortificada con vitamina D3 (colecalciferol) de la siguiente
manera:
- Leche en polvo: Una dosis única de 10 µg/100g, la
que podrá excederse hasta en un 40%, llegando a 14
µg/100g.
La leche en polvo que provenga de otros países podrá
venir fortificada desde el origen, o ser fortificada en
Chile, previo a su comercialización.
La verificación de la fortificación de la leche en
polvo se realizará en las plantas que elaboran o reenvasan
dicho producto, sea ésta para ser usada como materia prima
para otros alimentos, o bien, para el consumo directo. En
consecuencia, se excluirá la verificación de
fortificación a aquellos productos elaborados a partir de
la leche en polvo o de sus subproductos.
|
| Decreto 38, SALUD
Art. 1 N° 3
D.O. 02.02.2021 |
| Decreto 48, SALUD
Art. 1°, N° 2
D.O. 05.07.2022 |
|
Artículo 217.- Eliminado
|
| Decreto 38, SALUD
Art. 1 N° 4
D.O. 02.02.2021 |
|
Artículo 218.- Eliminado.
|
| Decreto 38, SALUD
Art. 1 N° 4
D.O. 02.02.2021 |
|
ARTÍCULO 219. Manjar o dulce de leche es el
producto obtenido a partir de leches cocidas
adicionadas o no de azúcares, edulcorantes, polioles,
fibras u otros ingredientes permitidos que, por efecto del
calor, adquiere su color característico. El contenido de
sólidos totales de leche será 25,5% como mínimo y no
contendrá más de 35% de agua. Se le podrá adicionar
sustancias amiláceas sólo al producto destinado a
repostería. Esta condición deberá declararse en el
envase, con una frase como "manjar de repostería" u otra
similar.
|
| Decreto 82,
SALUD
Art. 1° N° 2
D.O. 26.01.2023 |
|
Artículo 220.- Yogur es el producto lácteo coagulado
obtenido por fermentación láctica mediante la acción de
Lactobacillus bulgaricus y Streptococcus thermophilus, a
partir de leches pasteurizadas enteras, parcialmente descremadas o
descremadas, leches en polvo enteras, parcialmente
descremadas o descremadas o una mezcla de estos
productos.
En su elaboración se podrá adicionar:
a) ingredientes aromatizantes naturales: frutas (fresca, en conserva, congelada, en
polvo, puré, pulpa, jugo), cereales, miel, chocolate,
cacao, nueces, café, especias y otros aromatizantes
autorizados;
b) azúcar y/o edulcorantes autorizados de acuerdo a lo
señalado en el artículo 146 del presente reglamento;
c) aditivos alimentarios autorizados: aromatizantes,
colorantes, estabilizantes y como preservante ácido
sórbico y sus sales de sodio y potasio, cuya dosis máxima
será de 500 mg/kg expresada como ácido sórbico.
d) cultivos de bacterias adecuadas productoras de ácido láctico.
Los microorganismos lácticos presentes en el producto
final deberán ser viables y en cantidad superior a 10 6
UFC/g .
| NOTA: El Art.
transitorio del DTO 214, Salud, publicado el 04.02.2006,
dispuso que la modificación introducida al presente
artículo rige a contar de 180 días desde su publicación.
|
|
| DTO 214, SALUD
Art. primero II Nº23
D.O. 04.02.2006 |
| DTO
475, SALUD
Art. Unico, Nº 64
D.O. 13.01.2000 |
| DTO
475, SALUD
Art. Unico, Nº 64
D.O. 13.01.2000 |
| DTO 475, SALUD
Art. Unico, Nº 64
D.O. 13.01.2000 |
|
Artículo 221.- Crema de leche es el producto lácteo
relativamente rico en grasa separada de las leches que
adoptan la forma de emulsión tipo leches descremadas con grasa. Su
contenido de materia grasa deberá rotularse en forma
destacada.
| NOTA: El Art.
transitorio del DTO 214, Salud, publicado el 04.02.2006,
dispuso que la modificación introducida al presente
artículo rige a contar de 180 días desde su publicación.
|
|
| DTO 214, SALUD
Art. primero II Nº24
D.O. 04.02.2006 |
|
Artículo 222.- Se podrá utilizar en la elaboración
de crema de leche, los siguientes aditivos:
a) secuestrantes y emulsionantes autorizados en
una dosis máxima en el producto final de
2g/kg solos o 3 g/kg mezclados expresados como sustancias
anhidras;
b) espesantes autorizados en una dosis máxima en
el producto final de 5 g/kg solos o
mezclados; c) aromatizantes autorizados.
| NOTA: El Art. segundo
del DTO 68, Salud, publicado el 23.01.2006, dispuso que la
modificación introducida al presente artículo rige a
contar de 180 días después de su publicación.
|
|
| DTO 68, SALUD
Art. primero Nº 14
D.O. 23.01.2006 |
| DTO 475, SALUD
Art. Unico, Nº 66
D.O. 13.01.2000 |
|
Artículo 223.- La acidez de la crema de leche
no excederá de 20 ml de NaOH 0,1 N/100
g.
El expendio de las cremas de leche se hará,
exclusivamente, en los envases originales.
En la crema de leche pasteurizada deberá indicarse
claramente el código de lote y la fecha de vencimiento y,
además, que se debe mantener a una temperatura inferior a
4ºC.
Se prohíbe el expendio de crema cruda.
|
| Decreto 65, SALUD
Art. 1 N° 1
D.O. 29.11.2013 |
|
Artículo 224.- Se denominará "bebida láctea" a
los productos elaborados con base en
leche, con un mínimo de 30% de leche en el producto final,
tal como se consume de acuerdo a la definición de leche
líquida y en polvo establecida en los artículos 198 y 216,
a sus características señaladas en el artículo 203 y a
sus clasificaciones listadas en los artículos 204 y 205,
todos del presente reglamento. Podrá tener agregados de
otros ingredientes alimentarios, como nutrientes, factores
alimentarios y aditivos permitidos. La bebida láctea se
podrá presentar líquida lista para el consumo o en polvo
para reconstituir con un líquido apropiado antes del
consumo. En el rótulo se deberá etiquetar su denominación
"bebida láctea", de acuerdo a la letra a) del artículo 107
del Reglamento Sanitario de los Alimentos, y el porcentaje
de leche que contiene. Los límites de acidez adecuados para
los productos no fermentados ni acidificados son entre 11 y
18 ml de NaOH 0,1 N/100 g. Los parámetros microbiológicos
se regirán por el artículo 173 puntos 1.2, 1.3, 1.4 y 9.2
de este reglamento, según la presentación del producto tal
como se comercializa.
Se denominará "leche con..." a los productos
elaborados a partir de leche que cumple con la definición
de "leche" señalada en los artículos 198 y 216 del
Reglamento Sanitario de los Alimentos, estando presente en
una proporción igual o mayor al 75% de leche por porción
en el producto final, tal como se consume, al que se le
podrán adicionar otros ingredientes alimentarios, tales
como: concentrados de frutas, proteínas de soya, sólidos
lácteos, aceites vegetales, nutrientes, factores
alimentarios y aditivos permitidos. La "leche con..." se
podrá presentar líquida lista para el consumo o en polvo
para reconstituir con un líquido apropiado antes del
consumo. En el rótulo se deberá etiquetar su denominación
"leche con..." de acuerdo a la letra a) del artículo 107
del presente reglamento. Los parámetros microbiológicos se
regirán por el artículo 173 puntos 1.2, 1.3, 1.4 y 9.2 del
Reglamento Sanitario de los Alimentos, según la
presentación del producto tal como se comercializa.
|
| Decreto 65, SALUD
Art. 1 N° 2
D.O. 29.11.2013 |
|
Párrafo VI
De las mantequillas
|
|
Artículo 225.- Mantequilla, sin otra denominación,
es el producto lácteo derivado
exclusivamente de la crema pasteurizada de leches.
Los productos que usen la expresión de fantasía
"mantequilla de.", sin tratarse de un producto lácteo,
deberán rotular, además, el nombre del alimento de que se
trate, en los términos exigidos por la letra a) del
artículo 107 del presente reglamento, informando la
verdadera naturaleza del producto en forma específica.
|
| Decreto 37, SALUD
Art. 1 N° 1
D.O. 18.01.2017 |
|
Artículo 226.- Mantequilla de suero es el producto
lácteo derivado exclusivamente de la crema del suero de la
leche.
|
|
Artículo 227.- La mantequilla deberá responder a las
siguientes características:
a) caracteres organolépticos normales;
b) materia grasa de leche : mínimo 80%;
c) sólidos no grasos de leche : máximo 2%;
d) humedad : máximo 16%;
e) acidez de la materia grasa : máximo 18 ml de
hidróxido de sodio 0.1 N/100 g;
f) índice de peróxidos de la materia grasa en la planta
: máximo 0,3 meq 0 2/kg de grasa;
g) punto de fusión : 28 - 37ºC;
h) índice de refracción a 40ºC : 1,4546 - 1,4569;
i) grado de refracción a 40ºC: 40 - 45;
j) índice de yodo : 32 - 45;
k) índice de saponificación : 211 - 237;
l) su composición en ácidos grasos y triglicéridos
serán los de la grasa láctea.
|
|
Artículo 228.- Mantequilla fermentada es aquella
elaborada a partir de cremas fermentadas. Deberá cumplir
con las características del artículo 227, exceptuando los
parámetros de acidez.
|
|
Artículo 229.- Toda mantequilla deberá expenderse
envasada, rotulada y mantenerse refrigerada.
|
|
Artículo 230.- Grasa de mantequilla (butter oil),
grasa de mantequilla deshidratada y grasa de leche anhidra,
son productos obtenidos exclusivamente a partir de
mantequilla o crema debidamente pasteurizada y que resultan
de eliminar prácticamente la totalidad del contenido de
agua y del extracto seco magro.
|
|
Artículo 231.- La grasa de mantequilla deberá
contener:
a) materia grasa : mínimo 99,3%;
b) humedad : máximo 0,5%;
c) índice de peróxidos : máximo 0,8 meq oxígeno/kg de
grasa;
d) ácidos grasos libres : máximo 11,6 ml de hidróxido
de sodio 0.1 N/100 g.
|
|
Artículo 232.- La grasa de mantequilla deshidratada y
la grasa de leche anhidra deberá contener:
a) materia grasa : mínimo 99,8%;
b) humedad : máximo 0,1%;
c) índice de peróxidos : máximo 0,3 meq oxígeno/kg de
grasa;
d) ácidos grasos libres : máximo 11,6 ml de hidróxido
de sodio 0.1 N/100 g.
|
|
Artículo 233.- La grasa de mantequilla, grasa de
mantequilla deshidratada y grasa de leche anhidra no
destinadas al consumo directo ni para empleo en leche
recombinada o productos lácteos recombinados, solo podrán
contener como antioxidantes, los siguientes aditivos y en
las cantidades señalas en el Título III de este
reglamento:
Galatos de propilo, octilo y dodecilo
Butil-hidroxianisol (B.H.A.) Butil-hidroxitolueno (B.H.T.)
|
|
Párrafo VII
De los quesos
|
|
Artículo 234.- Queso es el producto madurado o sin
madurar, sólido o semisólido, obtenido coagulando leches,
leches descremadas, leches parcialmente descremadas, crema, crema de suero,
suero de queso o suero de mantequilla debidamente
pasteurizado o una combinación de estas materias, por la
acción de cuajo u otros
coagulantes apropiados (enzimas específicas o ácidos
orgánicos permitidos), y separando parcialmente el suero
que se produce como consecuencia de tal coagulación.
Queso Artesanal es el queso elaborado, en Plantas Queseras Familiares, con
leches producidas exclusivamente en el mismo predio donde se
fabrica este alimento y cuya producción diaria no exceda
los 500 litros. La producción,
elaboración, envase, almacenamiento, distribución y venta
de estos productos deberá ceñirse a lo establecido en el
presente reglamento y a las normas técnicas sobre
directrices para la elaboración de quesos artesanales
aprobadas por resolución del Ministerio de Salud, la que se
publicará en el Diario Oficial.
| NOTA: El Art.
transitorio del DTO 214, Salud, publicado el 04.02.2006,
dispuso que las modificaciones introducidas al presente
artículo rigen a contar de 180 días desde su publicación.
|
|
| DTO 214, SALUD
Art. primero II Nº25
D.O. 04.02.2006 |
| DTO 214,
SALUD
Art. primero II Nº25
D.O. 04.02.2006 |
|
Artículo 235.- En aquellas localidades donde no
rija la exigencia de la Ley Nº4869 de
pasteurización de la leche, todos los quesos deberán tener
un período de maduración previo no menor a 30 días para
su comercialización.
|
| Decreto 71, SALUD
Art. 1 N° 7
D.O. 06.03.2019 |
|
Artículo 236.- Para su elaboración a los quesos se le
podrá adicionar:
a) cultivos de bacterias productoras de ácido láctico;
b) cultivos de hongos o bacterias específicas para quesos
de características especiales;
c) cuajo u otras enzimas apropiadas para la coagulación;
d) cloruro de sodio;
e) agua;
f) cloruro de calcio;
g) nitrato de sodio o potasio: máximo 50 mg/kg de
queso;
h) caroteno, carotenoides, rocú o anato y riboflavina,
solos o mezclados;
i) sustancias aromatizantes o saborizantes naturales
autorizadas;
j) ácido cítrico y/o láctico;
k) frutos, semillas y especias.
| NOTA:
El artículo transitorio del DTO 115, Salud, publicado el
25.11.2003, dispone que la modificaciones a este artículo,
regirán 180 días después de su publicación.
|
|
| DTO 475, SALUD
Art. Unico, Nº 67
D.O. 13.01.2000 |
| DTO 115, SALUD
Art. primero Nº 15
D.O. 25.11.2003 |
|
Artículo 237.- Queso fresco y quesillo son aquellos
quesos de elaboración reciente que no han sufrido ninguna transformación ni
fermentación, salvo la láctica y son preparados con leches
pasteurizadas enteras, parcialmente descremadas o
descremadas.
Los quesos frescos y quesillos deberán ser enfriados a una temperatura no
superior a 5° C inmediatamente después de su elaboración
y mantenerse a esta temperatura hasta su expendio. El
producto final no podrá
contener nitratos ni nitritos.
Si en el proceso tecnológico propio de la elaboración de este tipo de quesos
se requiere de la adición de gelatinas, se aceptará como
máximo un 0,3% del producto
final.
Se prohíbe el fraccionamiento de queso fresco y
quesillo en los locales de expendio.
| NOTA: El artículo
transitorio del DTO 115, Salud, publicado el 25.11.2003,
dispone que la modificaciones a este artículo, regirán 180
días después de su publicación.
|
| NOTA 1: El
Art. transitorio del DTO 214, Salud, publicado el
04.02.2006, dispuso que la modificación introducida al
presente artículo rige a contar de 180 días desde su
publicación. |
|
| DTO
214, SALUD
Art. primero II Nº26
D.O. 04.02.2006 |
| DTO
115, SALUD
Art. primero Nº 16
D.O. 25.11.2003 |
| DTO
115, SALUD
Art. primero Nº 16
D.O. 25.11.2003 |
|
Artículo 238.- Queso maduro es el producto
que requiere de un período de
maduración a temperatura y en condiciones tales que se
produzcan los cambios bioquímicos y físicos necesarios
para obtener las características organolépticas que
tipifican los quesos.
|
| DTO 475, SALUD
Art. Unico, Nº 68
D.O. 13.01.2000 |
|
Artículo 239.- Queso fundido procesado untable
o cortable es el producto obtenido por
molienda, mezclado, fundición y emulsificación con la
ayuda de calor y agentes emulsificantes de una o más
variedades de queso aptos para el consumo, con o sin la
adición de sólidos lácteos y otros productos
alimenticios, tales como crema, mantequilla, grasa de
mantequilla, cloruro de sodio y especias.
A los quesos fundidos procesados untables o cortables se les podrá adicionar
aditivos alimentarios autorizados en el presente reglamento.
La dosis máxima de los emulsionantes en el producto
final será de 40 g/kg, solos o mezclados, pero sin que los
compuestos de fósforo agregados excedan de 9 g/kg
calculados como fósforo.
|
| DTO 475, SALUD
Art. Unico, Nº 69
D.O. 13.01.2000 |
| DTO
475, SALUD
Art. Unico, Nº 69
D.O. 13.01.2000 |
|
Artículo 240.- Los quesos podrán indicar además de
los requisitos generales establecidos en
este reglamento para la rotulación, el contenido mínimo de
materia grasa en el extracto seco.
|
| DTO 475, SALUD
Art. Unico, Nº 70
D.O. 13.01.2000 |
|
Artículo 241.- Cuando para la fabricación del
producto se emplee leche que no sea la de vaca deberá
indicarse la especie de donde procede la leche, así mismo
cuando se empleen mezclas de leches.
Sólo se podrá rotular como queso los productos que
cumplan con el artículo 234 de este reglamento.
|
|
Artículo 242.- Todo local de venta, que lamine
quesos con antelación al expendio, deberá
contar con una área adecuada para dicho propósito, la cual
deberá cumplir con lo establecido en el Título I del
presente reglamento.
El producto laminado, deberá manipularse respetando
todas las normas de higiene, procurando que su manipulación
y exposición a condiciones ambientales desfavorables, sea
mínima.
|
| DTO 475, SALUD
Art. Unico, Nº 71
D.O. 13.01.2000 |
|
TITULO IX
De los helados y mezclas de helados
|
|
Artículo 243.- Helados comestibles son los productos
obtenidos de una emulsión de grasa y proteínas, con la
adición de otros ingredientes o, de una mezcla de agua,
azúcares y otros ingredientes, que han sido tratados por
congelación y mantenidos en este estado.
|
|
Artículo 244.- Los ingredientes de leches que
se empleen en los helados y sus mezclas
deberán haber sido pasteurizados o sometidos a un
tratamiento térmico equivalente comprobado por la ausencia
de fosfatasa.
| NOTA: El Art.
transitorio del DTO 214, Salud, publicado el 04.02.2006,
dispuso que la modificación introducida al presente
artículo rige a contar de 180 días desde su publicación.
|
|
| DTO 214, SALUD
Art. primero II Nº3
D.O. 04.02.2006 |
|
Artículo 245.- Mezclas para helados son productos en
forma líquida o en polvo que se destinan a la preparación
de helados.
|
|
Artículo 246.- No se exigirá una nueva
pasteurización para los helados comestibles fabricados con
ingredientes concentrados o en polvo mediante la adición
exclusiva de agua potable, leches pasteurizadas y aromatizantes, que hayan sido
congelados en el plazo de una hora después de la adición
de tales
sustancias.
| NOTA:
El Art. transitorio del DTO 214, Salud, publicado el
04.02.2006, dispuso que la modificación introducida al
presente artículo rige a contar de 180 días desde su
publicación.
|
|
| DTO
214, SALUD
Art. primero II Nº27
D.O. 04.02.2006 |
|
TITULO X
De las grasas y aceites comestibles
|
|
Párrafo I
Disposiciones generales
|
|
Artículo 247.- Aceites y grasas son los triglicéridos
de ácidos grasos comercialmente puros, obtenidos de
materias primas sanas y limpias, libres de productos nocivos
derivados de su cultivo o manejo, o de los procesos de
elaboración.
|
|
Artículo 248.- El contenido de humedad y materias
volátiles, no deberá ser mayor a 0,2% en los aceites
comestibles y no más de 0,5% en las mantecas o grasas. No
deberán contener más de 0,25% de acidez libre, expresada
como ácido oléico y no más de 50 ppm de jabón. A la fecha de elaboración,
el límite máximo de peróxidos será de 2,5 meq de
oxígeno peróxido/kg de grasa y 10 meq de oxígeno
peróxido/kg de grasa en su
período de vida útil y almacenados de acuerdo a lo
indicado en la rotulación. No deberán presentar sus
características organolépticas alteradas.
Se exceptúan de esta disposición, respecto a la
acidez libre, el aceite de oliva y la manteca de cacao, cuya
acidez máxima será de 2,0% expresada en ácido oleico; el
aceite de palta, cuya acidez máxima será de 1,0% expresada
en ácido oleico, y la manteca de cerdo y grasa bovina, cuya
acidez máxima será de 0,8% expresado en ácido
oleico. Asimismo, se exceptúa
de esta disposición, respecto del índice de
peróxido, el aceite de oliva extra virgen, cuyo límite
máximo será de 20 meq. de oxígeno/k de aceite.
El contenido de ácidos grasos trans de origen
industrial en los alimentos deberá ser igual o
inferior al 2% del contenido total de
las grasas del producto.
| NOTA: El artículo
transitorio del DTO 115, Salud, publicado el 25.11.2003,
dispone que la modificaciones a este artículo, regirán 180
días después de su publicación.
|
|
| DTO 115,
SALUD
Art. primero Nº 17
D.O. 25.11.2003 |
| Decreto 18, SALUD
Art. 1 Nº 1
D.O. 05.10.2013 |
| DTO 475, SALUD
Art. Unico, Nº 72
D.O. 13.01.2000 |
| Decreto 106, SALUD
Art. 1 Nº 23
D.O. 23.04.2009 |
|
Artículo 249.- No se consideran aptos para el consumo
los alimentos grasos que estén rancios, alterados química
y/o microbiológicamente, que contengan materias extrañas,
restos de tejidos vegetales o animales, aceites de origen
mineral y aditivos no autorizados por el presente
reglamento.
Asimismo no se consideran aptos para el consumo humano
los alimentos grasos que contengan
solventes halogenados en
concentración máxima individual superior a 0,1 mg/kg o
concentración máxima total superior a 0,2 mg/kg.
En los aceite y grasas no se aceptará más de 2 ppb de
benzopirenos ni más de 5 ppb de la suma de los 8
hidrocarburos aromáticos policíclicos volátiles. Los
hidrocarburos aromáticos volátiles policíclicos
relacionados son los siguientes:
Benzo (a) pireno Benzo (e) pireno Benzo (a) antraceno
Benzo (b) fluoranteno Benzo (k) fluoranteno Dibenzo (a,h)
antraceno Benzo (g, h, i) perileno Indeno (1,2,3 - o,d)
pireno.
| NOTA: El
artículo transitorio del DTO 115, Salud, publicado el
25.11.2003, dispone que la modificaciones a este artículo,
regirán 180 días después de su publicación.
|
|
| DTO 115, SALUD
Art. primero Nº 18
D.O. 25.11.2003 |
|
Artículo 250.- La distribución y comercialización
de los aceites, mantecas y grasas
comestibles deberá realizarse en sus envases originales,
prohibiéndose su fraccionamiento en el punto de venta.
Para efectos de rotulación de los aceites, mantecas y
grasas comestibles como alimentos o ingredientes
alimenticios, será obligatoria la individualización del
fruto, semilla o especie animal de que provienen tales
productos y/o ingredientes. Se deberá declarar si los
aceites, mantecas y grasas comestibles se sometieron a
proceso de hidrogenación parcial y/o interesterificación
y/o fraccionamiento, según sea el caso. En las mezclas de
aceites, mantecas y grasas comestibles que se comercialicen
como productos terminados, se deberá declarar esta
condición en el listado de ingredientes como "mezcla de
aceites vegetales" o "mezcla de aceites, mantecas o grasa
animal" o "combinado de aceites, mantecas o grasas
animales", según corresponda, listando primero el aceite,
manteca o grasa que esté en mayor proporción. Se deberá
incluir en el rótulo la tabla nutricional correspondiente,
de acuerdo a lo establecido en el artículo 115 y último
inciso del artículo 116, del presente reglamento.
|
| Decreto 71,
SALUD
Art. 1 Nº 5
D.O. 23.08.2010 |
|
Párrafo II
De los aceites y mantecas o grasas de origen vegetal
|
|
Artículo 251.- Aceites comestibles de origen vegetal
son los obtenidos de los siguientes frutos o sus partes o de
semillas oleaginosas: algodón, cártamo, girasol o
maravilla, gérmen de maíz, maní o cacahuate, oliva, pepa
de uva, raps o colza, sésamo o ajonjolí, soja o soya,
avellana chilena, arroz, pepa de tomate, germen de trigo,
linaza, mosqueta, palta y otros autorizados por el Ministerio de
Salud, los que deberán ser de consistencia fluida a la
temperatura de 15ºC.
|
| DTO 73, SALUD
Art. 1º Nº 2
D.O. 03.08.2006 |
|
Artículo 252.- Los aceites no deberán contener un
porcentaje de ácido erúcico mayor de 5%.
|
|
Artículo 253.- Mantecas o grasas comestibles de origen
vegetal, son los alimentos grasos vegetales de consistencia
sólida o semisólida a la temperatura de 15ºC, obtenidas
de los siguientes frutos, sus partes o semillas: cacao,
coco, coco del Paraguay, babassú, palma, palmiste y otros
autorizados por el Ministerio de Salud.
|
|
Artículo 254.- Las constantes físicas y químicas de
los aceites y mantecas de origen vegetal deberán
corresponder a las indicadas en la tabla I. La composición
de ácidos grasos determinados por cromatografía
gas-líquido, señaladas en la tabla III, se considerarán
como de referencia.
|
|
Párrafo III
De los aceites y mantecas o grasas comestibles de origen
animal
|
|
Artículo 255.- Aceites comestibles de origen
marino son los obtenidos de animales marinos
y algas, con exclusión de anfibios y reptiles, de
consistencia fluida a 15ºC, que no han sido sometidos a
proceso de hidrogenación. Los aceites de algas deberán ser
autorizados por el Ministerio de Salud.
|
| Decreto 29, SALUD
Art. 1 N° 1
D.O. 12.10.2016 |
|
Artículo 256.- Mantecas o grasas comestibles de origen
animal, son las extraídas de los tejidos adiposos de
porcinos, ovinos, bovinos y aves, de consistencia sólida o
semisólida. Los puntos de fusión máximos serán:
. Manteca o grasa de cerdo 40ºC
. Grasa de bovino 45ºC
. Grasa de ovino 48ºC
. Grasa de ave 30ºC
|
|
Artículo 257.- Las constantes físicas y químicas de
los aceites, mantecas o grasas comestibles de origen animal
deberán corresponder a las indicadas en la tabla II. La
composición de ácidos grasos determinados por
cromatografía de gas-líquido, señaladas en las tablas III
y IV se considerarán como de referencia.
|
|
Párrafo IV
De otros alimentos grasos comestibles
|
|
Artículo 258.- Aceites marinos modificados
comestibles son los productos grasos de
consistencia fluida a la temperatura de 15°C, obtenidos de
especies pelágicas y sometidos a procesos de hidrogenación
y/o fraccionamiento.
|
| Decreto 29, SALUD
Art. 1 N° 2
D.O. 12.10.2016 |
|
Artículo 259.- Mantecas modificadas son los productos
obtenidos de aceites vegetales o marinos que han sido
sometidos a procesos de hidrogenación y eventualmente a
transesterificación, interesterificación y
fraccionamiento. Su punto de fusión máximo será de
45ºC. En materias primas se permitirán puntos de fusión
mayores.
|
|
Artículo 260.- Manteca emulsionada, es la emulsión
obtenida a partir de mantecas o grasas de origen animal
marino y/o vegetal con agua. Deberá declararse el contenido
de agua.
|
|
Artículo 261.- Aceite combinado es el producto
obtenido de la mezcla de aceites de origen marino con
aceites vegetales. El porcentaje máximo permitido de
aceite de origen marino a agregar en la mezcla será de un
50%.
|
|
Artículo 262.- Margarina es el producto en forma de
emulsión usualmente del tipo agua/aceite, obtenido de
grasas y aceites comestibles. Las margarinas deberán
cumplir on las siguientes características:
a) margarina de mesa es aquella cuya materia grasa
presenta un punto de fusión máximo de 37ºC. Su contenido
de agua será de 16% como máximo y su contenido de materia
grasa será de 80% como mínimo;
Igualmente se consideran margarinas de mesa aquellas que presenten un contenido
de materia grasa menor de 80% y mayor de 16% de agua. Estas
margarinas deberán indicar el contenido de agua.
b) margarina de repostería es aquella cuya materia grasa
presenta un punto de fusión máximo de
45ºC.
Su contenido de agua y su uso se indicarán en la
rotulación.
| NOTA: El artículo
transitorio del DTO 57, Salud, publicado el 06.05.2005,
dispone que las modificaciones a la presente norma entrarán
en vigencia dieciocho meses después de su publicación.
|
|
| DTO
475, SALUD
Art. Unico, Nº 73
D.O. 13.01.2000
DTO 57, SALUD
Art. único Nº 9
D.O. 06.05.2005 |
|
Artículo 263.- Las margarinas deberán cumplir con las
siguientes características:
a) La acidez de la materia grasa, expresada en ácido
oléico, no será superior al 0,25%;
b) Las margarinas de mesa deben contener por kg de
producto terminado 30.000 U.I. de vitamina A y 70g de
ácido linoleico.
|
|
Artículo 264.- Las margarinas deberán almacenarse
refrigeradas o, en su defecto, mantenerlas en lugares
exentos de humedad y protegidas de los rayos solares.
| NOTA Los Numerales 2,
3 y 4 del artículo 1º del Decreto 18, Salud, publicado el
05.10.2013, modifica la Tabla I Constantes físico-química
de Aceites y Mantecas de Origen Vegetal y Tabla III
Composición de Ácidos Grasos de Aceites y Mantecas de
Origen Vegetal, de la manera indicada en la propia
norma. |
|
|
Párrafo V
De los aceites y mantecas usados en fritura
|
|
Artículo 265.- Los aceites y mantecas utilizados en la
producción industrial e institucional de alimentos fritos,
deberán tener un contenido máximo de ácido linolénico de
un 2%. Podrán estar adicionados de antioxidantes y sinergistas
autorizados en el presente reglamento.
|
| DTO 475, SALUD
Art. Unico, Nº 74
D.O. 13.01.2000 |
|
Artículo 266.- No deberán utilizarse los aceites o
mantecas cuando sobrepasen los siguientes límites:
a) acidez libre expresada como ácido oléico
superior
al 2,5%;
b) punto de humo inferior a 170°C;
c) 25% de compuestos polares como máximo.
Cuando los resultados de los análisis de la acidez
libre de los aceites, expresadas como ácido oleico
sobrepasen el 2,5%, el representante del establecimiento
muestreado, deberá demostrar a las autoridades sanitarias
que los compuestos polares del aceite en estudio no superan
el 25%.
|
| DTO 475, SALUD
Art. Unico, Nº 75
D.O. 13.01.2000 |
| DTO 475,
SALUD
Art. Unico, Nº 75
D.O. 13.01.2000
DTO 475, SALUD
Art. Unico, Nº 75
D.O. 13.01.2000 |
|
Artículo 267.- Se prohíbe el uso de los aceites y
mantecas provenientes de los procesos de frituras,
descartados o reprocesados, en otros alimentos de uso
humano.
|
|
TITULO XI
De los alimentos cárneos
|
|
Párrafo I
De la carne de abasto
|
|
Artículo 268.- Con la denominación de carne se
entiende la parte comestible de los músculos de los
animales de abasto como bovinos, ovinos, porcinos, equinos,
caprinos, camélidos, y de otras especies aptas para el
consumo humano.
Las carnes de animales de caza en sus procedimientos de
manejo, elaboración, envase, almacenamiento, distribución y venta deberán
ceñirse a lo establecido en el presente reglamento y a la
norma técnica dictada para éstas, aprobada por decreto del
Ministerio de Salud, la que se publicará en el Diario
Oficial.
|
| Decreto
106, SALUD
Art. 1 Nº 24
D.O. 23.04.2009 |
|
Artículo 269.- La carne comprende todos los tejidos
blandos que rodean el esqueleto, incluyendo su cobertura
grasa, tendones, vasos, nervios, aponeurosis, huesos propios
de cada corte cuando estén adheridos a la masa muscular
correspondiente y todos los tejidos no separados durante la
faena, excepto los músculos de sostén del aparato hioídeo
y el esófago. Se entiende por subproducto comestible a
las partes y órganos tales como:
corazón, hígado, riñones, timo, ubre, sangre, lengua,
sesos o grasa, de las especies de abasto. Se exceptúan de
esta categoría los pulmones y los establecidos en el
artículo 274.
|
| DTO 475, SALUD
Art. Unico, Nº 76
D.O. 13.01.2000 |
| DTO 214, SALUD
Art. primero I Nº10
D.O. 04.02.2006 |
|
Artículo 270.- La carne recién faenada debe
tener apariencia marmórea, con superficie
brillante, ligeramente húmeda y elástica al tacto. El
olor y el color deben ser característicos de la especie. La
grasa debe ser firme al tacto y no debe contener zonas o
puntos hemorrágicos.
|
| DTO 475, SALUD
Art. Unico, Nº 77
D.O. 13.01.2000 |
|
Artículo 271.- Carne fresca es aquella que, aparte
de haber sido refrigerada o enfriada en
un rango de temperatura que va entre 0° a +7°C, según
medición dispuesta en el artículo 22 del decreto Nº 94,
de 2008, de los Ministerios de Agricultura y Salud, no ha
recibido, a los efectos de su conservación, otro
tratamiento que el envasado protector y que conserva sus
características naturales.
|
| Decreto 83, SALUD
Art. 1 N° 4
D.O. 25.06.2010 |
|
Artículo 272.- Derogado.
|
| Decreto 83, SALUD
Art. 1 N° 5
D.O. 25.06.2010 |
|
Artículo 273.- Carne congelada es aquella
cuya temperatura interna medida en el
centro de la masa muscular es de -18°C como máximo. Sin
embargo, para fines de transporte de las mismas, se
considerarán igualmente como carnes congeladas, aquellas
definidas en los artículos 190 y 191 del presente
reglamento.
|
| DTO 475, SALUD
Art. Unico, Nº 80
D.O. 13.01.2000 |
| Decreto 83, SALUD
Art. 1 N° 6
D.O. 25.06.2010 |
|
Artículo 274.- Se prohíbe destinar los labios,
ollares y las orejas de animales de abasto para el consumo
directo así como formando parte de productos elaborados,
incluida la carne molida, con la excepción del cerdo
destinado a la elaboración de cecinas.
|
| Decreto 24, SALUD
Art. 1 Nº 1
D.O. 24.11.2011 |
|
Artículo 275.- Carne molida es la carne triturada
apta para el consumo humano. Se permitirá
solamente su expendio:
a) A pedido y molida en presencia del comprador.
b) Envasada proveniente de establecimientos
autorizados.
Las carnes molidas deberán declarar la especie animal
de la que proceden y estar exentas de aditivos alimentarios,
proteína vegetal y sustancias amiláceas.
Solo a la carne molida envasada en establecimientos
industriales podrá adicionársele antioxidantes y
preservantes autorizados.
El contenido de grasa total de la carne molida de
vacuno podrá ser hasta 10%, pudiendo rotularse dicho
contenido de grasa total junto con el nombre del producto.
Para efectos de fiscalización de lo anterior, se aplicarán
los límites de tolerancia señalados en el artículo 115
del presente reglamento.
|
| Decreto 26, SALUD
Art. 1 N° 1
D.O. 03.10.2016 |
|
Artículo 276.- Carne marinada de res es aquella
carne proveniente de las reses de abasto,
que mediante inyección u otro método adecuado, ha sido
adicionada de salmuera, adobos y aditivos alimentarios
permitidos. El proceso de marinado deberá ser realizado una
vez finalizada la faena y en el momento en que la carne haya
alcanzado una temperatura menor o igual a 7° C.
Adicionalmente, el proceso de marinado deberá ser
realizado de acuerdo a las buenas prácticas de manufactura
(BPM), e informado en el rótulo con caracteres visibles, en
la cara principal del envase, de tal modo que permita una
clara identificación del proceso de marinado por parte del
consumidor y que lo diferencie totalmente de su similar no
sometido a dicho proceso.
Sin perjuicio de cumplir con los requisitos generales
de rotulación, las carnes marinadas deberán informar
además la proporción del peso que representa el marinado
con respecto al peso total del producto, mediante la
utilización de alguna de las siguientes frases: "Marinado
al X %" o Contiene hasta un X% de marinado. "
En el caso de las carnes marinadas de reses que se
vendan a granel, directamente al público, la información
sobre el porcentaje de marinado se colocará en un cartel,
junto al nombre del producto, de tal modo que permita una
clara identificación del proceso de marinado por parte del
consumidor y que lo diferencie totalmente de su similar no
sometido a dicho proceso.
|
| Decreto 106, SALUD
Art. 1 Nº 25
D.O. 23.04.2009 |
|
Artículo 277.- Sólo en establecimientos autorizados
se permitirá la tenencia,
almacenamiento, distribución y venta de carnes de bovinos,
ovinos, caprinos, porcinos, equinos y otras especies aptas
para el consumo humano.
Su venta directa al público, mediante sistema de
autoservicio, se realizará en envases individuales, los que
deberán cumplir con las disposiciones sobre envase y
rotulación de este reglamento.
Los establecimientos que expendan carnes de especies
diferentes al bovino, deberán indicar claramente al
consumidor la especie de que se trata.
|
| Decreto 106, SALUD
Art. 1 Nº 26
D.O. 23.04.2009 |
|
Artículo 278.- Se prohíbe la tenencia y
comercialización de carnes y subproductos comestibles
cuando:
a) estén en estado de alteración organoléptica debido a
causas
físicas, químicas o biológicas;
b) provengan de animales mortecinos o de fetos;
c) se consideren no aptas para el consumo por la autoridad
sanitaria.
d) no provenga de establecimientos autorizados
para el faenamiento.
|
| DTO
475, SALUD
Art. Unico, Nº 84
D.O. 13.01.2000 |
|
Artículo 279.- Se prohíbe la comercialización,
a cualquier título de carnes, visceras
y subproductos con residuos de hormonas no endógenas
promotoras de crecimiento o sustancias de efecto hormonal
que excedan los límites fijados por el Ministerio de Salud
mediante la correspondiente norma técnica.
Si durante la inspección post-mortem hubiera indicios
de que la carne o las visceras pudieran exceder los límites
de residuos fijados por el Ministerio de Salud, éstas se
retendrán, se identificarán, se mantendrán en condiciones
adecuadas y se someterán a todos los exámenes de
laboratorio necesarios para comprobar su inocuidad. De
resultar, como producto de estos exámenes, niveles de
residuos por sobre los límites establecidos, el dictamen
final será ''no apto para consumo humano''. Cuando no sea
posible mantener la carne y las visceras en condiciones
adecuadas, en espera de los resultados de laboratorio, la
declaración de inaptitud se hará de inmediato.
En toda importación de carne y subproductos
comestibles, la autoridad sanitaria podrá requerir que se
acredite mediante certificado oficial de origen que los
residuos de hormonas, promotores de crecimiento y sustancias
de efecto hormonal de uso veterinario están bajo los
límites establecidos.
|
| DTO 475, SALUD
Art. Unico, Nº 85
D.O. 13.01.2000 |
|
Artículo 280.- Sin perjuicio de lo establecido en
el artículo precedente, se prohíbe la
comercialización, a cualquier título, de carnes y sus
subproductos con residuos de plaguicidas, residuos de
medicamentos de uso veterinario y de aditivos, usados en la
alimentación animal, que estén por sobre los límites de
tolerancia fijados. El Ministerio de Salud fijará mediante
la dictación de la correspondiente norma técnica los
límites máximos para residuos de medicamentos de uso
veterinario en la carne y otros alimentos.
En toda importación de carne y sus subproductos
comestibles, la autoridad sanitaria podrá requerir que se
acredite mediante certificado oficial de origen que los
residuos de plaguicidas, medicamentos de uso veterinario y
de aditivos usados en la alimentación animal están bajo
los límites establecidos.
|
| DTO 475, SALUD
Art. Unico, Nº 85
D.O. 13.01.2000 |
|
Párrafo II
De la carne de ave
|
|
Artículo 281.- Ave faenada es el producto de
cualquiera de las especies de aves criadas en cautividad que
hayan sido sacrificadas en mataderos de aves, a las que se
les ha extraído la sangre, las plumas, las patas, la
cabeza, el buche, la tráquea, el esófago, las vísceras,
los pulmones y los órganos genitales.
|
|
Artículo 282.- Carne de ave es la parte muscular de
las especies de aves a que se refiere el presente
reglamento, constituida por todos los tejidos blandos que
rodean la estructura del esqueleto. Incluye la piel,
cobertura grasa, tendones, vasos, nervios, aponeurosis y
todos aquellos tejidos que no se separan durante el
faenamiento.
|
|
Artículo 283.- Ave trozada o partes de ave es
cualquiera parte o partes comestibles de las aves faenadas,
excluidas las menudencias y despojos.
|
|
Artículo 284.- Menudencia (menudillo o menudo ) es el
conjunto de órganos constituidos por hígado sin vesícula
biliar, estómago muscular (molleja) desprovisto de la
mucosa y su contenido, corazón con o sin pericardio y el
pescuezo desprovisto de tráquea y esófago.
|
|
Artículo 285.- Despojos corresponden a la cabeza y las
patas de las aves faenadas. No se permitirá su inclusión
en la cavidad abdominal de las aves faenadas.
|
|
Artículo 286.- Las aves faenadas, aves trozadas, así
como las menudencias y despojos deben ser enfriados a 2°C como máximo y para su
expendio en el punto de venta, mantenidos a una temperatura
de hasta 6ºC, medida en el interior de la masa
muscular.
| NOTA: El Art. segundo
del DTO 68, Salud, publicado el 23.01.2006, dispuso que la
modificación introducida al presente artículo rige a
contar de 180 días después de su publicación.
|
|
| DTO
68, SALUD
Art. primero Nº 17
D.O. 23.01.2006 |
|
Artículo 287.- Las aves faenadas, aves trozadas, así
como las menudencias y despojos que han sido sometidas a
refrigeración se deben mantener a una temperatura comprendida entre 4°C y
-18°C.
| NOTA:
El Art. segundo del DTO 68, Salud, publicado el
23.01.2006, dispuso que la modificación introducida al
presente artículo rige a contar de 180 días después de su
publicación.
|
|
| DTO 68, SALUD
Art. primero Nº 18
D.O. 23.01.2006 |
|
Artículo 288.- Las aves faenadas, aves trozadas, así
como las menudencias y despojos que han sido sometidos a
congelación se deben mantener a una temperatura interna de
-18ºC como máxima, medida en el centro de la masa
muscular.
|
|
Artículo 289.- Las aves faenadas, sean éstas
enfriadas, refrigeradas o congeladas, sólo se podrán
comercializar y expender evisceradas.
|
|
Artículo 290.- Toda ave faenada, en el momento del
empaque, deberá ser identificada con una etiqueta que
indique :
a) individualización del matadero donde fue
sacrificada y de la resolución que lo autorizó;
b) fecha de vencimiento del producto.
|
| DTO 475,
SALUD
Art. Unico, Nº 86
D.O. 13.01.2000 |
|
Artículo 291.- Las aves enfriadas, refrigeradas
o congeladas, enteras o trozadas de
venta directa al público, mediante sistema de autoservicio,
se comercializarán en envases individuales, los que
deberán cumplir con las disposiciones sobre envases y
rotulación de este reglamento.
Las aves faenadas refrigeradas o congeladas se podrán
comercializar con sus menudencias, siempre que éstas estén
incorporadas en la cavidad torácica, envasadas en bolsas de
material plástico cerradas.
|
| Decreto 106, SALUD
Art. 1 Nº 27
D.O. 23.04.2009 |
|
Artículo 292.- Carne marinada de ave, es aquella
carne proveniente de las aves de corral,
que mediante inyección u otro método adecuado, ha sido
adicionada de salmuera, adobos y aditivos alimentarios
permitidos. El proceso de marinado deberá ser realizado una
vez finalizada la faena y en el momento en que la carcasa
haya alcanzado una temperatura igual o menor a 6° C.
Adicionalmente, el proceso de marinado deberá ser
realizado de acuerdo a las buenas prácticas de manufactura
(BPM), e informado en el rótulo con caracteres visibles, en
la cara principal del envase, de tal modo que permita una
clara identificación del proceso de marinado por parte del
consumidor y que lo diferencie totalmente de su similar no
sometido a dicho proceso.
Sin perjuicio de cumplir con los requisitos generales
de rotulación, las carnes marinadas deberán informar
además, la proporción del peso que representa el marinado
con respecto al peso total del producto, mediante la
utilización de alguna de las siguientes frases: "Marinado
al X %" o Contiene hasta un X % de marinado".
En el caso de las carnes marinadas de aves que se
vendan a granel, directamente al público, dicha
información se colocará en un cartel, junto al nombre del
producto, de tal modo que permita una clara identificación
del proceso de marinado por parte del consumidor y que lo
diferencie totalmente de su similar no sometido a dicho
proceso.
|
| Decreto 106, SALUD
Art. 1 Nº 28
D.O. 23.04.2009 |
|
Artículo 293.- En las aves faenadas refrigeradas
o congeladas no se permitirá
porcentajes de agua residual mayores a los establecidos en
este artículo. Se entiende por agua residual, el contenido
de agua admitida en las carcasas, cuya absorción en el
proceso de enfriado es técnicamente inevitable:
La medición del contenido de agua residual, será
realizada por metodologías analíticas validadas por el
Instituto de Salud Pública de Chile.
|
| Decreto 106, SALUD
Art. 1 Nº 29
D.O. 23.04.2009 |
|
Artículo 294.- El sacrificio, tenencia,
almacenamiento, distribución y venta de carne de aves,
sólo se permitirá en establecimientos autorizados.
Se prohíbe la tenencia y comercialización de carnes
de aves y subproductos comestibles cuando:
a) estén en estado de alteración organolépticas, sea
por causas físicas, químicas o biológicas;
b) provengan de animales mortecinos;
c) contengan residuos de hormonas sintéticas o productos
con actividad hormonal, residuos de productos veterinarios,
antisépticos y aditivos, por sobre los niveles de
tolerancias fijadas por el Ministerio de Salud mediante
resolución fundada.
|
|
Párrafo III
De las cecinas
|
|
Artículo 295.- Cecinas, sin otra denominación, son
aquellos productos elaborados a base de carne y grasa de
vacuno o cerdo, adicionados o no de aditivos, condimentos,
especias, agua o hielo.
Los productos elaborados que contengan carnes
provenientes de otras especies, en cualquiera proporción,
deberán declararlo en la rotulación.
Todo local de venta que fraccione cecinas con antelación al expendio, deberá
contar con un lugar adecuado para dicho propósito el cual
deberá cumplir con lo establecido en el T�tulo I del
presente reglamento.
El producto fraccionado deberá manipularse respetando las
normas de higiene, procurando que su manipulación y
exposición a condiciones ambientales desfavorables sea
mínima. Queda prohibido su reenvasado y cualquier adulteración del envase original y
su rotulación en el lugar de
expendio.
| NOTA:
El Art. segundo del DTO 68, Salud, publicado el
23.01.2006, dispuso que la modificación introducida al
presente artículo rige a contar de 180 días después de su
publicación.
|
|
| DTO
475, SALUD
Art. Unico, Nº 89
D.O. 13.01.2000 |
| DTO
68, SALUD
Art. primero Nº 19
D.O. 23.01.2006 |
|
Artículo 296.- Cecinas crudas frescas son aquellas
que, como resultado de su elaboración, no sufren
alteración significativa en los valores de aw y pH respecto a los de la carne fresca.
Pueden o no ser sometidas a proceso de aireación,
curación, secado y/o ahumado.
| NOTA: El Art. segundo
del DTO 68, Salud, publicado el 23.01.2006, dispuso que la
modificación introducida al presente artículo rige a
contar de 180 días después de su publicación.
|
|
| DTO
68, SALUD
Art. primero Nº 20
D.O. 23.01.2006 |
|
Artículo 297.- Cecinas crudas maduradas son aquellos
productos ahumados o no, sometidos a procesos de curación y
maduración, de duración prolongada y que, como
consecuencia de su elaboración, sufren una disminución de
su pH y aw respecto a las de la carne fresca.
| NOTA:
El Art. segundo del DTO 68, Salud, publicado el
23.01.2006, dispuso que la modificación introducida al
presente artículo rige a contar de 180 días después de su
publicación.
|
|
| DTO 68, SALUD
Art. primero Nº 20
D.O. 23.01.2006 |
|
Artículo 298.- Cecinas crudas acidificadas son
aquellos productos ahumados o no, que como
consecuencia de su elaboración sufren una
disminución del valor de su pH respecto al de la carne
fresca.
| NOTA:
El Art. segundo del DTO 68, Salud, publicado el
23.01.2006, dispuso que la modificación introducida al
presente artículo rige a contar de 180 días después de su
publicación.
|
|
| DTO 68, SALUD
Art. primero Nº 20
D.O. 23.01.2006 |
|
Artículo 299.- Cecinas cocidas son aquellos
productos que, cualquiera sea su forma de
elaboración, son sometidos a un tratamiento térmico, en
que la temperatura medida en el centro del producto, no sea
inferior a 68ºC.
| NOTA:
El Art. segundo del DTO 68, Salud, publicado el
23.01.2006, dispuso que la modificación introducida al
presente artículo rige a contar de 180 días después de su
publicación.
|
|
| DTO 475, SALUD
Art. Unico, Nº 90
D.O. 13.01.2000
DTO 68, SALUD
Art. primero Nº 20
D.O. 23.01.2006 |
|
Artículo 300.- Hamburguesa, sin otra denominación,
es el producto elaborado con carne
picada o molida, adicionada o no de grasa animal,, sal,
aditivos permitidos y especias. Previo a la cocción,
su contenido de grasa no podrá
exceder de 24%.
| NOTA: El Art. segundo
del DTO 68, Salud, publicado el 23.01.2006, dispuso que la
modificación introducida al presente artículo rige a
contar de 180 días después de su publicación.
|
|
| DTO 68, SALUD
Art. primero Nº 21
D.O. 23.01.2006 |
|
Artículo 301.- En la elaboración de cecinas y
hamburguesas se permitirá usar como extensor de la carne
proteínas no cárnicas autorizadas. En el caso de usar
proteínas texturizadas su proporción máxima será de 10%
en base seca.
INCISO SUPRIMIDO
| NOTA:
El Art. segundo del DTO 68, Salud, publicado el
23.01.2006, dispuso que la modificación introducida al
presente artículo rige a contar de 180 días después de su
publicación.
|
|
| DTO 68, SALUD
Art. primero Nº 22
D.O.
23.01.2006 |
|
Artículo 302.- Las cecinas crudas frescas,
acidificadas y cecinas cocidas se deben mantener en
refrigeración (0-6ºC) inmediatamente después de su
elaboración, y en los locales de expendio al público. Las
cecinas maduradas se deben mantener en lugar fresco y seco
(máximo 12ºC).
|
|
Artículo 303.- El transporte y distribución de todo
tipo de cecinas deberá efectuarse en vehículos autorizados
bajo condiciones de refrigeración (entre 0 y 6ºC). Esta
última exigencia se hará efectiva después de
transcurridos 24 meses de la entrada en vigencia del
presente reglamento.
|
|
Artículo 304.- Jamón es una cecina cocida y
curada, preparada con carne de pierna de
cerdo, entera o trozada, separada del resto en un punto
posterior al extremo del hueso de la cadera y sin pernil,
adicionada con agua, sal y aditivos permitidos, y con o sin
otros ingredientes permitidos. Su humedad no será superior
a 77%.
|
| DTO 475, SALUD
Art. Unico, Nº 92
D.O. 13.01.2000 |
|
Artículo 305.- Fiambre de jamón es una cecina cocida
y curada, preparada con carne de cerdo
trozada, picada o molida, y adicionada de agua, sal,
aditivos y otros ingredientes permitidos. Este producto
deberá contener como mínimo 12% de proteína y un máximo
de 5% de grasa libre.
|
| DTO 475, SALUD
Art. Unico, Nº 92
D.O. 13.01.2000 |
|
Artículo 306.- Salchicha o vienesa es una
cecina cocida y curada, de masa homogénea,
elaborada en base a carne de cerdo, vacuno u otras especies
y adicionada con grasa o aceite, agua, sal, aditivos, con o
sin cuero, y otros ingredientes permitidos. Este producto
deberá contener como mínimo 12% de proteínas (N x 6,25) y
un máximo 25% de grasa libre.
|
| DTO 475, SALUD
Art. Unico, Nº 92
D.O. 13.01.2000 |
|
Artículo 307.- Cuando se usen membranas artificiales
no comestibles en el embutido de cecinas, su rotulación
deberá advertir que ellas deben ser retiradas antes de
consumir el producto.
|
|
Artículo 308.- Se prohíbe agregar colorantes artificiales a las carnes y pastas,
empleadas en la elaboración de cecinas. Se permite el uso
de estos colorantes en tripas naturales y en membranas
artificiales no comestibles y siempre que el colorante no
difunda al contenido.
|
| DTO
475, SALUD
Art. Unico, Nº 92
D.O. 13.01.2000 |
|
Artículo 309.- Se prohíbe agregar sustancias
amiláceas a las cecinas, salvo las que se expendan
enlatadas, en cuyo caso se permitirá hasta un 5%.
|
|
Artículo 310.- En la elaboración de cecinas se
permitirá el uso de nitrito de sodio, nitrato de sodio y
nitrato de potasio, solos o en mezcla bajo las siguientes
condiciones:
a) como "sal nitrificada". Sal nitrificada es
una
mezcla de cloruro de sodio, adicionado de nitrito
de sodio en una concentración de 0,7 a 0,8%;
b) "sales de cura" mezcla de cloruro de sodio, nitrito de
sodio, nitrato de sodio o potasio, y otros aditivos
permitidos. El porcentaje total de nitrito de sodio y
nitrato de sodio o potasio, expresado como nitrito de
sodio
no debe ser superior al 10%;
c) la sal nitrificada y sales de cura deben ser elaboradas
exclusivamente en establecimientos autorizados para
estos
fines por la autoridad sanitaria, quedando prohibida su
elaboración en las fábricas de cecinas.
Queda asimismo prohibido mantener nitrito de sodio,
nitrato
de sodio y/o potasio como tales, en fábricas de
cecinas;
d) en la sal nitrificada y las sales de cura se deberán
declarar en forma destacada en su rótulo los
porcentajes de
nitrito de sodio y nitrato de sodio y/o potasio que
contiene,
como asimismo sus recomendaciones de uso.
e) las sales de cura deberán ser coloreadas para
diferenciarlas de la sal común. Para ello se
utilizará el colorante azorrubina en una cantidad
que no supere los 250 mg/kg de sal de cura.
|
| DTO 475, SALUD
Art. Unico, Nº 93
D.O. 13.01.2000 |
| DTO
475, SALUD
Art. Unico, Nº 93
D.O. 13.01.2000 |
|
Artículo 311.- En cecinas se permitirá:
a) un contenido máximo de 125 mg/kg de nitrito de sodio
residual;
b) un contenido máximo de 30 mg/kg de nitrosaminas
expresadas como nitrosodimetilamina.
|
|
Párrafo IV
De los jugos y extractos de carne
|
|
Artículo 312.- Los productos elaborados de carne y
productos cárneos, comprenden entre otros:
a) jugo de carne es la parte líquida de las fibras
musculares obtenida por presión y concentración al vacío,
a baja temperatura. No debe contener más de 15% de cenizas
totales, no más de 2,5% de cloruro de sodio y no menos de
12% de nitrógeno, calculados sobre materia seca;
b) extracto de carne es el producto resultante de la
filtración y concentración, hasta consistencia pastosa,
del caldo preparado con tejido muscular de reses bovinas,
prácticamente libres de grasas, tendones, cartílagos y
huesos. El extracto de carne de otras especies deberá
expenderse con indicación precisa de la especie de origen.
El extracto de carne debe contener como mínimo 6% de
creatinina total y como máximo 22% de humedad, 2% de
materia grasa, 10% de cloruro de sodio y 1% de residuo
insoluble;
c) gelatina es el producto obtenido del tejido colágeno o
ligamentos de origen animal, en medio ácido o alcalino y
que se presenta en forma de polvo, láminas o tabletas
transparentes. Contendrá como mínimo 15% de nitrógeno
total y un máximo de 3,5% de cenizas totales.
La solución al 1% en agua dará al enfriarse una jalea
inodora.
|
|
TITULO XII
De los pescados
|
|
Artículo 313.- Pescado fresco es aquel recientemente
capturado y que no ha sido sometido a ningún proceso
después de su extracción, a excepción del eviscerado
cuando corresponda. Desde el momento de la extracción se deberán adoptar
las medidas necesarias para reducir la temperatura de los
productos, a través de mecanismos adecuados, que no
contaminen el recurso extraído.
Durante la distribución estos productos deberán ser
conservados a temperaturas no superiores a 5º C.
|
| DTO 45, SALUD
Art. único Nº 3
D.O. 12.07.2006 |
|
Artículo 314.- Pescado fresco enfriado es aquel que
después de su extracción, ha sido eviscerado y enfriado a
una temperatura entre 0 y 3ºC con el objeto de conservarlo
durante su distribución.
|
|
Artículo 315.- Pescado congelado es aquel que
recientemente capturado, es procesado y sometido a una
temperatura de -18°C como máxima, medida en su centro
térmico.
|
|
Artículo 316.- Pescado ahumado es aquel, que
previamente salado o no, es sometido a la acción del humo
de maderas duras u otro procedimiento.
|
|
Artículo 317.- Todos los pescados frescos y enfriados
que se expenden o elaboren deben ser eviscerados tan pronto
sean capturados, excepto algunas especies de talla reducida
(sardinas, pejerreyes, anchovetas y otros).
|
|
Artículo 318.- El pescado fresco que no sea eviscerado
inmediatamente después de su captura, sólo podrá
comercializarse si ha sido sometido de inmediato a la
congelación a temperatura de -18ªC como máxima, medida en
su centro térmico.
|
|
Artículo 319.- El pescado fresco destinado a la
exportación, podrá transportarse y comercializarse sin
eviscerar previa autorización en tal sentido del Director
del Servicio de Salud correspondiente.
|
|
Artículo 320.- El pescado fresco y el pescado fresco
enfriado, deberán cumplir con las características
físico-organolépticas siguientes:
a) aspecto general: buen aspecto, pigmentación bien
definida, mucosidad cutánea escasa, transparente, incolora
o bien ligeramente opaca;
b) olor: fresco a mar o algas frescas;
c) consistencia muscular: superficie rígida, que no se
hunde a la presión del dedo o bien, si lo hace, retorna de
inmediato a su condición normal. Existencia de rigor
mortis o en tránsito a desaparecer;
d) ojos: el globo ocular convexo llena la cavidad
orbitaria o bien se presenta ligeramente hundido. Pupilas
negras y brillantes, de forma y contorno definido. Córnea
transparente e iris pigmentado;
e) branquias: color rojo brillante, olor propio o neutro.
Laminillas perfectamente separadas unas de otras, de
longitud similar yuxtapuestas regularmente;
f) cavidad abdominal:
- ejemplares enteros: vísceras tersas y brillantes,
perladas y sin daño aparente.
- ejemplares eviscerados: peritoneo adherente, restos
de sangre roja;
g) escamas: adheridas con brillo metálico.
|
|
Artículo 321.- El pescado fraccionado deberá cumplir
con las siguientes características
físico-organolépticas:
a) aspecto externo
- tronco: mantener la pigmentación externa;
- medallones y filetes: color rosado traslúcido;
blanquecino en carnes provenientes de pescados de carne
blanca;
b) olor: fresco y propio;
c) consistencia muscular: firme, no se hunde a la presión
del dedo, o bien retorna a su condición normal;
d) textura: miómeros definidos;
e) pH: máximo 6,8.
|
|
Artículo 322.- Todo local de venta que
fraccione pescado con antelación al expendio,
deberá contar con un lugar adecuado para dicho propósito
el cual deberá cumplir con lo establecido en el Título I
del presente reglamento. El producto fraccionado, deberá
manipularse respetando todas las normas de higiene,
procurando que su manipulación y exposición a condiciones
ambientales desfavorables sea mínima.
|
| DTO 475, SALUD
Art. Unico, Nº 94
D.O. 13.01.2000 |
|
Artículo 323.- Los pescados que se comercialicen
para el consumo humano deberán estar
refrigerados y exentos de parásitos y sus quistes.
|
| DTO 45, SALUD
Art. único Nº 4
D.O. 12.07.2006 |
|
Artículo 324.- Los pescados frescos, frescos enfriados
y congelados no deberán contener más de:
a) 30 mg/100g de nitrógeno básico volátil total (NBVT)
para peces no seláceos;
b) 70 mg/100g de nitrógeno básico volátil total (NBVT)
para peces seláceos;
c) 20 mg/100g de histamina.
|
|
TITULO XIII
De los mariscos
|
|
Artículo 325.- Marisco es todo aquel animal
invertebrado comestible que tiene en el agua su medio normal
de vida. Comprende moluscos, crustáceos, equinodermos,
tunicados y otros.
|
|
Artículo 326.- Los mariscos que pueden
permanecer vivos fuera de su medio natural
(bivalvos, crustáceos, equinodermos y tunicados), cuando se
expendan en estado fresco, deberán ser conservados vivos
hasta el momento de su venta.
|
| DTO 475, SALUD
Art. Unico, Nº 96
D.O. 13.01.2000 |
|
Artículo 327.- Marisco fresco es aquel recientemente
capturado y que no ha sido sometido a ningún proceso
después de su extracción. Desde el momento de la extracción se
deberán adoptar las medidas necesarias para reducir la
temperatura de los productos, a través de mecanismos
adecuados, que no contaminen el recurso extraído.
Durante la distribución estos productos deberán ser
conservados a temperaturas no superiores a 5º C.
|
| DTO 45, SALUD
Art. único Nº 5
D.O. 12.07.2006 |
|
Artículo 328.- Marisco fresco enfriado es aquel que
después de su extracción ha sido enfriado a una
temperatura entre 0 y 3ªC, con el objeto de conservarlo
durante su distribución.
|
|
Artículo 329.- Marisco congelado es aquel que
inmediatamente después de su extracción ha sido procesado
y sometido a una temperatura de -18ºC como máxima, medidos
en su centro térmico.
|
|
Artículo 330.- Para evaluar el estado de frescura de
los mariscos, deberán observarse las siguientes
características:
Moluscos bivalvos y gastrópodos:
a) aspecto general: vivos, buen aspecto;
b) olor: fresco y propio;
c) estimulación física:cierre de valvas en bivalvos,
retracción dentro o bajo la caparazón en gastrópodos.
Moluscos cefalópodos:
a) aspecto externo: pigmentación muy definida con
cromatóforos intactos; piel lisa, sana e intacta;
b) olor: neutro;
c) color: propio, carne blanca, firme y nacarado;
d) tentáculos: bien adheridos al manto;
Crustáceos:
a) aspecto general: vivos, buen aspecto, ausencia de
melanósis;
b) ojos: negros, brillantes y turgentes;
d) membrana tóraco-abdominal: resistente, brillante y
clara;
e) olor: neutro;
Equinodermos:
a) aspecto general: vivos, buen aspecto;
b) olor: propio;
c) espículas: móviles y erectas.
|
|
Artículo 331.- Los mariscos que se comercialicen
para el consumo humano deberán estar
exentos de quistes de parásitos .
|
| DTO 475, SALUD
Art. Unico, Nº 97
D.O. 13.01.2000 |
|
Artículo 332.- El Nitrógeno Básico Volátil Total
(N.B.V.T.), en mariscos frescos, enfriados y congelados con
excepción de crustáceos, será de 30mg/100 gramos como
máximo. En crustáceos no se debe sobrepasar los 60mg/100
gramos como máximo.
|
|
Artículo 333.- Los contenidos máximos de
toxinas marinas en mariscos destinados al
consumo humano (cuerpo entero o cualquier parte consumible
por separado) deberán ser los que se indican a
continuación:
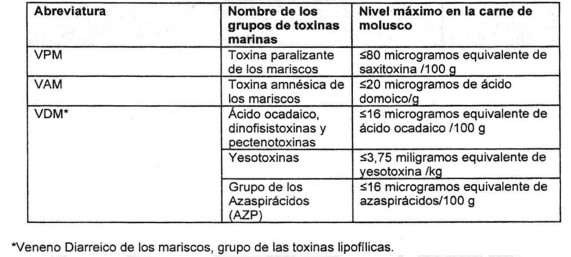
|
Los análisis para las determinaciones de toxinas
marinas serán la prueba del bioensayo u otros métodos
instrumentales reconocidos internacionalmente, los que
serán establecidos mediante resolución emanada de este
Ministerio.
Los análisis deberán realizarse en laboratorios
reconocidos por la Autoridad Sanitaria o por laboratorios
reconocidos o autorizados por otras instituciones del Estado
que desarrollen acciones de diagnóstico y control para
toxinas marinas.
En las áreas declaradas como afectadas por marea roja
por la autoridad sanitaria, ésta establecerá, mediante
resolución, las especies de mariscos cuya recolección o
captura queda prohibida. En tales áreas, la autoridad
sanitaria podrá autorizar, mediante resolución fundada, la
recolección, captura y procesamiento industrial de mariscos
contaminados con toxinas de marea roja en aquellos casos en
que se demuestre que su procesamiento disminuye los niveles
de toxina por debajo de los límites establecidos en el
presente reglamento.
|
| Decreto 20,
SALUD
Art. 1° N° 1)
D.O. 14.01.2025 |
|
Artículo 334.- El marisco expuesto a posibles
contaminaciones, sean naturales o provocadas por el hombre,
deberá ser sometido a un proceso de purificación, debiendo
la autoridad sanitaria controlar la inocuidad del producto
purificado.
|
|
Artículo 335.- La instalación y funcionamiento de
establecimientos destinados a la crianza, cultivo, engorda y
purificación de mariscos destinados al consumo, así como
los viveros dedicados a la comercialización de dichas
especies, deberán ubicarse en lugares con agua limpia,
cuyas condiciones microbiológicas permitan a los productos
cumplir los requisitos establecidos en el Título V de este
reglamento y contar con la autorización otorgada por el
Servicio de Salud correspondiente.
|
|
TITULO XIV
De los huevos
|
|
Artículo 336.- Huevo es el óvulo
completamente evolucionado de la gallina. Los
huevos de otras aves deben designarse con la calificación
complementaria de la especie de ave que proceda.
|
| DTO 90, SALUD
Art. 1°
D.O. 28.04.2000 |
|
Artículo 337.- Huevo fresco es el huevo entero en
su cáscara que no ha sufrido ningún
proceso de conservación y que tiene un período de
almacenaje no superior a 8 días. La cámara de aire del
huevo fresco no deberá ser superior a 8 mm.
|
| DTO 90, SALUD
Art. 1°
D.O. 28.04.2000 |
|
Artículo 338.- Huevo conservado es el huevo entero
en su cáscara que se ha mantenido
refrigerado o en un lugar fresco y que tiene un período de
almacenaje no superior a 30 días. La cámara de aire no
deberá ser superior a 10 mm. El envase de este tipo de
huevos deberá ser rotulado con las palabras ''Huevo
conservado en lugar fresco''.
|
| DTO 90, SALUD
Art. 1°
D.O. 28.04.2000 |
|
Artículo 339.- Huevo refrigerado es el huevo entero
en su cáscara que ha sido sometido
desde su producción a la acción del frío y mantenido en
esas condiciones durante más de 30 días, a una temperatura
máxima de 2°C y a una humedad relativa entre 80 y 90%. El
pH de la clara y la yema no será mayor de 8,8 y 6,9
respectivamente; y la cámara de aire no deberá exceder de
10 mm. El envase de este tipo de huevos deberá ser rotulado
con las palabras ''Huevo Refrigerado''.
|
| DTO 90, SALUD
Art. 1°
D.O. 28.04.2000 |
|
Artículo 340.- Todo huevo entero en su
cáscara, destinado a consumo directo, deberá
ser transportado a los sitios de expendio en envases o
bandejas nuevas.
Todos los embalajes que se usen en el transporte de los
huevos (cajas o bandejas), deben ser de primer uso. Se
permite el empleo de embalajes de retorno siempre que sea
posible lavarlos y desinfectarlos para lograr una correcta
higienización de los mismos, la eficacia de dicho proceso
deberá ser verificada por la autoridad sanitaria.
Los huevos deben ser transportados en vehículos
cerrados cuyas estructuras sean de materiales y
construcción tal, que permitan mantener una temperatura
adecuada, su limpieza y desinfección.
|
| DTO 90, SALUD
Art. 1°
D.O. 28.04.2000 |
|
Artículo 341.- Queda prohibida la venta de huevos
que presenten las siguientes
alteraciones:
- Manchados
- Cáscara fisurada
- Cáscara trizada o rota
- Signos de putrefacción
- Manchas de sangre
- Embriones en franco desarrollo
- Mohos y parásitos
- Alta deshidratación
- Cuerpos extraños
|
| DTO 90, SALUD
Art. 1°
D.O. 28.04.2000 |
|
Artículo 342.- Huevo entero deshidratado o desecado
es aquel desprovisto de su cáscara y al
que se le ha extraído el agua por evaporación. No deberá
contener más de un 5% de agua si se usa antiaglutinante; de
no hacerlo se aceptará hasta un 8% de agua. El contenido de
proteínas no será menor de 45% y el de grasa 42%. No
deberá contener colorantes artificiales.
|
| DTO 90, SALUD
Art. 1°
D.O. 28.04.2000 |
|
Artículo 343.- Huevo entero líquido es aquel
privado de la cáscara, que conserva las
proporciones naturales de la clara y de la yema, las que
mezcladas dan lugar a un producto homogéneo. No se
permitirá el uso de aditivos alimentarios artificiales para
su conservación.
Los huevos o sus partes en estado líquido que han sido
congelados deben mantenerse en envases de cierre hermético.
Deberán preservarse a una temperatura inferior a -12°C, la
que se mantendrá hasta la descongelación necesaria para su
uso inmediato.
|
| DTO 90, SALUD
Art. 1°
D.O. 28.04.2000 |
|
Artículo 344.- Se permite el agregado como antiaglomerante o antihumectante al
huevo en polvo de no más de 1% en peso de dióxido de
silicio, y no más de 1,5% en peso de silicato de aluminio y
sodio.
|
| DTO
90, SALUD
Art. 1°
D.O. 28.04.2000 |
|
Artículo 345.- Los establecimientos que elaboren
huevo líquido y huevo congelado deberán
someter los huevos a utilizar como materia prima a un
proceso de lavado previo con agua potable de flujo continuo
o adicionando a la misma, antisépticos autorizados
atóxicos, en aquellos casos en que el proceso de
elaboración no contemple alguna etapa tendiente a reducir
la flora bacteriana tal como pasteurización u otros.
|
| DTO 90, SALUD
Art. 1°
D.O. 28.04.2000 |
|
TITULO XV
De los alimentos farináceos
|
|
Párrafo I
Disposiciones generales
|
|
Artículo 346.- La denominación genérica de alimentos
farináceos está reservada para designar a los productos
naturales, simples o transformados, que se caracterizan por
contener sustancias amiláceas como componente dominante,
acompañado o no de otros nutrientes, tales como proteínas,
grasas, azúcares y otros.
|
|
Párrafo II
De las harinas
|
|
Artículo 347.- Harina, sin otro calificativo, es el
producto pulverulento obtenido por la molienda gradual y
sistemática de granos de trigo de la especie Triticum
aestivum sp. vulgare, previa separación de las impurezas,
hasta un grado de extracción determinado.
|
|
Artículo 348.- El producto pulverulento proveniente de
la molienda de otros granos, será designado con la palabra
harina, seguida de un calificativo que indique la o las
especies de grano de la que provenga.
|
|
Artículo 349.- La harina deberá responder a
los siguientes requisitos:
a) contener hasta un máximo de 15,0% de humedad;
b) contener hasta un máximo de 0,25% de acidez expresada
en ácido sulfúrico, sobre la base de 14,0% de humedad;
c) contener hasta un máximo de 0,65% de cenizas, sobre la
base de 14,0% de humedad;
d) contener hasta un máximo de 0,4% de fibra cruda sobre
la base de 14,0% de humedad;
e) no contener menos de 7,0% de materias nitrogenadas (N x
5,7), sobre la base de 14,0% de humedad, y
f) ser blanca, marfil o ligeramente amarillenta.
|
| DTO 475, SALUD
Art. Unico, Nº 100
D.O. 13.01.2000 |
|
Artículo 350.- La harina deberá contener como
mínimo las siguientes cantidades de
vitaminas y sales minerales:
Tiamina 6,3 mg/kg
Riboflavina 1,3 mg/kg
Niacina 13,0 mg/kg
Hierro 30,0 mg/kg
El hierro debe agregarse en forma de sulfato ferroso,
en el evento de no ser esto posible podrá usarse fumarato
ferroso siempre que se mantenga la equivalencia con el
sulfato ferroso.
Asimismo, la harina debe contener 1,8 mg/kg de ácido
fólico, sin embargo éste se aceptará que esté presente
en un rango de 1,0 a 2,6 mg/kg.
La harina deberá ser fortificada con
vitamina D3, en la cual deberá usarse preferentemente
vitamina D 3 vegetal. Cuando se utilice vitamina D 3
animal, el producto necesariamente deberá comercializarse
envasado de manera que se advierta al consumidor respecto al
origen animal de la vitamina D empleada.
La harina deberá ser fortificada con vitamina D3,
colecalciferol, de origen vegetal o animal, en una cantidad
mínima de 2,25 µg/100g, pudiendo excederse hasta en un
40%, alcanzando el nivel de 3,15 µg/100g.
El origen vegetal o animal de la vitamina D3 utilizada,
deberá declararse, de acuerdo a lo establecido en el
artículo 107 letra h) del presente reglamento, como:
"vitamina D 3 vegetal" o "vitamina D3 animal", según
corresponda.
La verificación de la fortificación se realizará en
la harina como materia prima, para ser utilizada en otros
alimentos o comercializada a público. En consecuencia, se
excluirá la verificación de fortificación a aquellos
productos elaborados a partir de la harina o de sus
subproductos.
|
| Decreto 75, SALUD
Art. 1 Nº 1
D.O. 16.03.2010 |
| Decreto 48, SALUD
Art. 1°, N° 3
D.O. 05.07.2022 |
|
Artículo 351.- Las mezclas vitamínicas que se
comercialicen para enriquecer la harina sean nacionales o
importadas deberán indicar en su rotulación las cantidades
de nutrientes que aportan por gramo de mezcla.
El Ministerio de Salud mediante
decreto, dictado bajo la fórmula "Por orden del Presidente
de la República", aprobará la directriz sobre los
parámetros técnicos adecuados para que la composición de
la premezcla vitamínica para harinas sea uniforme.
|
| Decreto 75, SALUD
Art. 1 Nº 2
D.O. 16.03.2010 |
|
Artículo 352.- Harina integral es el producto
resultante de la trituración del cereal previa limpieza y
acondicionamiento, hasta llegar a un 100% de extracción.
|
|
Artículo 353.- La harina integral deberá cumplir con
las características siguientes:
a) humedad, no más de 15,0%;
b) fibra cruda, no más de 1,5% sobre la base de 14,0% de
humedad;
c) cenizas, no más de 1,5%, sobre la base de 14,0% de
humedad, y d) acidez, no más de 0,3% expresada en ácido
sulfúrico sobre la base de un 14% de humedad.
|
|
Artículo 354.- Las harinas de legumbres no
deben contener más de 10 unidades de
inhibidor de tripsina por miligramo de harina seca, 300
unidades de hemoaglutinantes por gramo de harina seca ni
más de 0,1 mg de ácido cianhídrico por gramo de harina
seca. Las harinas de lupino además no deberán contener
más de 0,05% de alcaloides.
|
| DTO 475, SALUD
Art. Unico, Nº 102
D.O. 13.01.2000 |
|
Artículo 355.- Las harinas no deberán contener
insectos, partes de éstos o sus estados evolutivos, ácaros
ni otros elementos extraños.
|
|
Párrafo III
Del pan y los productos de pastelería y repostería
|
|
Artículo 356.- Con el nombre de pan sin otra
denominación, se entiende el producto de la cocción de la
masa resultante de una mezcla de harina de trigo, levadura
de panificación, agua potable y sal comestible, con o sin
adición de mejoradores de panificación y/o enriquecedores,
tales como: leche, azúcar, materias grasas u otros
autorizados por este reglamento.
Si el pan se fabrica con otra harina, se denominará
con el nombre de la harina que se emplee.
|
|
Artículo 357.- El pan deberá presentar las
características siguientes:
a) olor y sabor característico;
b) cocción y panificación normales;
c) limpio y sin cuerpos extraños;
d) agua, no más de 36% en muestra tomada 1 hora después
de salida del horno, y
e) acidez, no más de 0,25% expresada en ácido sulfúrico
y calculada sobre la base de 30,0% de agua.
|
|
Artículo 358.- Con el nombre de masas o pastas
horneadas se designan diversos productos elaborados en base
a harinas, y adicionados o no de especies y otros
ingredientes o aditivos permitidos, las que deberán cumplir
con las siguientes especificaciones:
a) el aspecto de la masa será homogéneo, adecuado
para
dar la característica típica del producto;
b) acidez no superior al 0,25% expresada en ácido
sulfúrico.
|
| DTO 475, SALUD
Art. Unico, Nº 103
D.O. 13.01.2000 |
|
Artículo 359.- El pan, los pasteles, las masas, pastas
y otros productos de pastelería y repostería, no deberán
contener sustancias extrañas, insectos, parte de éstos o
sus estados evolutivos, ni ácaros.
|
|
Artículo 360.- Las mezclas de aditivos mejoradores de
panificación usados en la industria panadera no deberán
contener bromato de potasio.
|
|
Párrafo IV
De los fideos y productos afines
|
|
Artículo 361.- Fideos son los productos constituidos
por mezclas de sémolas de trigo y/o harina con agua
potable, no fermentadas, sin cocción y que han sido
sometidos a un proceso de desecación. Podrán adicionarse
huevos, hortalizas y otros ingredientes y aditivos
autorizados.
|
|
Artículo 362.- Los fideos deberán cumplir con los
siguientes requisitos:
a) agua, máximo 13,5% y
b) acidez total no superior a 0,25%, expresada en ácido
sulfúrico, sobre la base de 14,0% de humedad.
Las demás exigencias y características
corresponderán a las de la materia prima de origen, sin
considerar nutrientes u otras sustancias agregadas
permitidas.
|
|
Artículo 363.- Fideos enriquecidos con vitaminas y
sales minerales son aquellos que contienen como mínimo los
siguientes nutrientes por cada kilogramo de producto final:
Tiamina 9,0 mg
Riboflavina 3,0 mg
Niacina 57,0 mg
Hierro 30,0 mg
El hierro debe agregarse en forma de sulfato ferroso o
pirofosfato ferroso.
|
|
Artículo 364.- Fideos o pastas con o al huevo son
aquellos a los cuales se les ha agregado huevos frescos
enteros o su equivalente deshidratado, de modo que contengan
como mínimo 330 mg de colesterol, por cada kilogramo de
producto terminado.
|
|
Artículo 365.- Pastas alimenticias frescas son los
productos fabricados con sémolas de trigo y/o harina con
agua potable, adicionados o no con huevos, hortalizas u
otros ingredientes y aditivos autorizados, y que no han
sufrido un proceso de desecación.
|
|
Artículo 366.- Las pastas alimenticias frescas deben
cumplir con los siguientes requisitos:
a) humedad, máximo 35%, y
b) acidez, máximo 0,20% expresada en ácido sulfúrico,
sobre la base de un 14,0% de humedad.
|
|
Artículo 367.- Los fideos y productos afines no
deberán contener insectos o sus estados evolutivos, ácaros
ni hongos.
|
|
Párrafo V
De otros productos farináceos
|
|
Artículo 368.- Los productos farináceos para
coctel que se comercializan envasados, tales
como: papas fritas, ramitas, productos extruidos, cereales
dilatados, tortillas de maíz y similares, deberán
presentar un máximo 40% de materia grasa y 5% de humedad.
|
| DTO 475, SALUD
Art. Unico, Nº 104
D.O. 13.01.2000 |
|
Artículo 369.- Los cereales para el desayuno son
los productos elaborados a base de
harinas o granos de cereales adicionados o no de aditivos
autorizados, sal con aceites vegetales y/o jarabes
azucarados comestible u otros ingredientes alimenticios.
Pueden ser recubiertos y enriquecidos con vitaminas y
minerales.
|
| DTO 475, SALUD
Art. Unico, Nº 105
D.O. 13.01.2000 |
|
Artículo 370.- Los productos descritos en este
párrafo deberán presentar los caracteres que les son
propios como sabor, olor, aspecto, textura y estar exentos
de sustancias extrañas, insectos o parte de ellos.
|
|
Párrafo VI
De los derivados de cereales y tubérculos
|
|
Artículo 371.- Se incluyen en este grupo diversos
productos derivados de cereales y tubérculos tales como:
chuchoca es el producto total de la molienda gruesa del
grano de maíz tierno (choclo), previamente cocido y seco;
maicena es la fécula de maíz blanco, variedad dulce;
mote es el grano de trigo blando y tierno, obtenido por
cocción y descortezado con lejía de ceniza u otro
procedimiento equivalente autorizado y lavado con agua
potable hasta eliminación total del álcali (pH 6,9);
mote de maíz es el maíz cocido y descortezado
mediante lejía caliente de ceniza u otro procedimiento
autorizado, y lavado con agua potable hasta eliminación del
álcali (pH 6,9);
polenta es el producto de la molienda gruesa del grano
de maíz seco y descortezado;
sémola es el producto de estructura granulosa,
obtenido por la molienda gruesa y cernida del trigo duro
(Triticum durum);
tapioca es el producto obtenido de la fécula de
mandioca, humedecida y granulada;
avena laminada es el producto obtenido, por compresión
mecánica del grano de avena industrialmente limpio y
desprovisto de sus tegumentos;
chuño es el producto obtenido a partir de fécula de
papa y puede contener hasta un máximo de 18% de humedad;
afrecho o salvado de trigo es el producto obtenido en
el proceso de molienda del cereal y corresponde a las
materias fibrosas no digeribles obtenidas a partir de las
envolturas externas (pericarpio y testa) de la semilla o
cariopse;
gérmen de trigo es el producto obtenido en el proceso
de molienda a partir de la extracción del embrión de la
semilla o cariopse.
|
|
TITULO XVI
De las levaduras de panificación y de los agentes
leudantes
|
|
Artículo 372.- Levadura para panificación es el
producto obtenido de la propagación industrial de levaduras
del género Saccharomyces en medios de cultivos adecuados.
|
|
Artículo 373.- Levadura prensada o filtrada para
panificación corresponde a la levadura que ha sido
centrifugada, prensada o filtrada, de manera que su humedad
no sea mayor de 75% en peso.
|
|
Artículo 374.- Levadura seca y levadura seca
instantánea para panificación corresponde a la levadura
que ha sido deshidratada, de manera que su humedad no sea
superior al 10% en peso.
|
|
Artículo 375.- Polvos de hornear son aquellos
productos formados de ácido carbónico y sus sales sódica,
potásica, cálcica y amónica y otros leudantes químicos
autorizados, pudiendo adicionarles excipientes como material
inerte.
|
|
Artículo 376.- Se podrán usar como agentes leudantes
otros productos, siempre que estén expresamente autorizados
para este fin en este reglamento.
|
|
TITULO XVII
De los azúcares y de la miel
|
|
Párrafo I
De los azúcares
|
|
Artículo 377.- Con el nombre de azúcar sólo podrá
denominarse a la sacarosa natural cristalizada proveniente
de la raíz de la remolacha azucarera (Beta vulgaris
var.saccharina o saccharifera) o de los tallos de la caña de azúcar
(Saccharum officinarum).
| NOTA:
El Art. segundo del DTO 68, Salud, publicado el
23.01.2006, dispuso que la modificación introducida al
presente artículo rige a contar de 180 días después de su
publicación.
|
|
| DTO 68, SALUD
Art. primero Nº 23
D.O. 23.01.2006 |
|
Artículo 378.- Azúcar crudo es el producto sólido
cristalizado, obtenido de la caña de azúcar o de la
remolacha azucarera, constituido esencialmente por cristales
sueltos de sacarosa cubiertos de una película de su licor
madre. Su polarización mínima a 20ºC debe ser de 96.
|
|
Artículo 379.- Azúcar blanco granulado o refinado es
el producto que contiene por lo menos un 99,5% de sacarosa y
no más de 0,1% de sustancias insolubles en agua. No
deberá contener más de 0,10% de cenizas, 0,10% de
sustancias reductoras ni más de 0,10% de humedad y su color
será como máximo 150 unidades ICUMSA.
Al azúcar blanco podrá adicionarse hasta en un 2%, en
total, de silicatos o fosfatos de calcio como agentes
antihumectantes u otros productos permitidos.
|
|
Artículo 380.- Azúcar rubio granulado es el producto
cristalizado obtenido de la caña de azúcar o de la
remolacha azucarera que contiene como mínimo 98.5% de
sacarosa y como máximo 0,2% de sustancias insolubles en
agua, 0,4% de cenizas y 0,10% de humedad.
|
|
Artículo 381.- Azúcar flor o azúcar en polvo
(azúcar glacé) es el producto que se obtiene al moler
finamente el azúcar blanco granulado o el azúcar refinado
granulado. Sus características deben corresponder a las
del azúcar utilizado en su fabricación, permitiéndose
agregar silicato o fosfato de calcio u otros agentes
antihumectantes, en las concentraciones indicadas en este
reglamento. Como ingrediente facultativo, se podrá
utilizar almidón en una concentración
máxima de 5% a condición de que no se emplee otro
antiaglutinante o antihumectante.
|
| DTO 475, SALUD
Art. Unico, Nº 106
D.O. 13.01.2000 |
|
Artículo 382.- Chancaca es el producto obtenido al
concentrar y cristalizar el jugo purificado de caña o de
remolacha. Debe contener como mínimo 80% de sacarosa y
como máximo 1% de sustancias insolubles en agua, 1,2% de
cenizas y 6% de humedad.
|
|
Artículo 383.- Con el nombre de azúcares se
entenderá a los carbohidratos endulzantes,
monosacáridos y disacáridos refinados, concentrados y/o
cristalizados, para efectos de rotulación, los que deberán
rotularse con su nombre específico.
Los azúcares se clasificarán en azúcares
"tradicionales" y azúcares "no tradicionales".
Por azúcares "tradicionales" se entenderá a los
carbohidratos, monosacáridos y disacáridos refinados,
concentrados y/o cristalizados, que aportan 4 kcal por
gramo, tales como: glucosa, fructosa, galactosa, sacarosa,
lactosa y maltosa.
Por azúcares "no tradicionales" se entenderá a los
siguientes carbohidratos: Tagatosa y Alulosa.
Cuando, en este reglamento, se mencione a los azúcares
sin otra denominación, se entenderá por ellos a los
azúcares tradicionales. Además, en el caso de establecer a
los azúcares como una condición en los ingredientes de
diversos productos regulados en este reglamento, se
aceptará su reemplazo, total o parcial, por azúcares no
tradicionales.
Ambos tipos de azúcares, tradicionales y no
tradicionales, deberán rotularse con su nombre específico
en el listado de ingredientes.
En la declaración de nutrientes, los azúcares no
tradicionales deberán declararse con su nombre específico
y no deberán considerarse ni en el aporte del total de
azúcares o azúcares totales, ni en el aporte de hidratos
de carbonos disponibles.
El aporte calórico de los azúcares no tradicionales
deberá ser considerado en el aporte energético del
producto, y se calculará según los factores de conversión
energética establecidos, para estos efectos, por el
Ministerio de Salud mediante norma técnica publicada en el
Diario Oficial.
En los productos elaborados con azúcares no
tradicionales, se deberá rotular la siguiente frase, según
sea el caso:
- Para el caso de la Alulosa: "Ingestas de 28
gramos/porción o más de Alulosa, podrán producir
malestares gastrointestinales o efecto laxante".
- Para el caso de la Tagatosa: "Ingestas de 30
gramos/porción o más de Tagatosa, podrán producir
malestares gastrointestinales o efecto laxante".
|
| Decreto 41,
SALUD
Art. 1º Nº 1)
D.O. 16.04.2024 |
|
Párrafo II
De los jarabes
|
|
Artículo 384.- Se reserva la denominación de jarabes
a los derivados, sucedáneos y subproductos de los azúcares
naturales que comprenden a las sustancias cuya nomenclatura
y requisitos se detallan en los artículos siguientes.
|
|
Artículo 385.- DEROGADO
| NOTA: El Art. segundo
del DTO 68, Salud, publicado el 23.01.2006, dispuso que la
modificación introducida al presente artículo rige a
contar de 180 días después de su publicación.
|
|
| DTO 68, SALUD
Art. primero Nº 25
D.O. 23.01.2006 |
|
Artículo 386.- DEROGADO
| NOTA: El Art. segundo
del DTO 68, Salud, publicado el 23.01.2006, dispuso que la
modificación introducida al presente artículo rige a
contar de 180 días después de su publicación.
|
|
| DTO 68, SALUD
Art. primero Nº 25
D.O. 23.01.2006 |
|
Artículo 387.- Jarabe de glucosa es una
solución concentrada y purificada de
sacáridos nutritivos obtenidos del
almidón.
| NOTA:
El Art. segundo del DTO 68, Salud, publicado el
23.01.2006, dispuso que la modificación introducida al
presente artículo rige a contar de 180 días después de su
publicación.
|
|
| DTO 68, SALUD
Art. primero Nº 26
D.O. 23.01.2006 |
|
Artículo 388.- El jarabe de glucosa destinado a la
fabricación de productos de confitería podrá contener
como máximo 400 mg/kg de anhídrido sulfuroso, aceptándose
para el jarabe de glucosa destinado a otros usos un máximo
de 40 mg/kg de anhídrido sulfuroso.
|
|
Artículo 389.- Jarabe de glucosa "deshidratada" es el
jarabe de glucosa del que se ha separado parcialmente el
agua. Debe contener como mínimo 20% m/m de azúcares
reductores (equivalente en dextrosa), expresados en
D-glucosa en seco y 90% m/m de sólidos totales y como
máximo 1% m/m en seco de cenizas sulfatadas y 1 mg/kg de
arsénico. El jarabe de glucosa deshidratado destinado a
la fabricación de productos de
confitería deberá contener como máximo 150 mg/kg de
anhídrido sulfuroso, aceptándose para el jarabe de glucosa
deshidratado destinado a otros usos un máximo de 40 mg/kg
de anhídrido sulforoso.
|
| DTO 238, SALUD
Art. 1°, N° 4
D.O. 26.05.2000 |
|
Artículo 390.- Jarabe de maíz de alta fructosa, es
un jarabe de maíz, obtenido por
isomerización enzimática de una solución de alta
dextrosa, conteniendo al menos un 70,5% de sólidos, no
menos de un 92% de monosacáridos, conteniendo como mínimo
un 42% de fructosa y no más de un 8% de otros sacáridos.
|
| DTO 238, SALUD
Art. 1°, N° 5
D.O. 26.05.2000 |
|
Artículo 391.- Jarabes naturales son los
jugos naturales azucarados de productos
vegetales (caña, maíz, remolacha, palma, frutas y otros),
concentrados hasta la consistencia de jarabe, debiendo tener
como mínimo 62º Brix y no contener sustancias aromáticas
artificiales ni sustancias colorantes.
|
| DTO 475, SALUD
Art. Unico, Nº 107
D.O. 13.01.2000 |
|
Artículo 392.- Jarabes artificiales son las soluciones
concentradas de azúcares en agua potable, con adición de
sustancias aromáticas, colorantes y ácidos permitidos.
|
|
Párrafo III
De la miel
|
|
Artículo 393.- Se entiende por "miel" la
sustancia dulce natural producida por abejas
Apis mellifera a partir del néctar de las plantas o de
secreciones de partes vivas de éstas o de excreciones de
insectos succionadores de plantas que quedan sobre partes
vivas de las mismas y que las abejas recogen, transforman y
combinan con sustancias específicas propias, y depositan,
deshidratan, almacenan y dejan en el panal para que madure y
añeje.
"Miel de flores" o "miel de néctar" es la miel que
procede del néctar de las plantas.
"Miel de mielada" es la miel que procede principalmente
de excreciones que los insectos succionadores (Hemiptera)
dejan sobre las partes vivas de las plantas o de secreciones
de partes vivas de las mismas.
La miel se compone esencialmente de diferentes
azúcares, predominantemente fructosa y glucosa, además de
otras sustancias como ácidos orgánicos, enzimas y
partículas sólidas derivadas de la recolección. El color
de la miel varía de casi incoloro a pardo oscuro. Su
consistencia puede ser fluida, viscosa, o total o
parcialmente cristalizada. El sabor y el aroma varían, pero
derivan de la planta de origen.
La miel deberá cumplir con las siguientes
restricciones y características:
a) No contener ningún ingrediente adicional, incluidos
los aditivos alimentarios u otra sustancia que no sea
definida como miel.
b) No contener ninguna materia, sabor, aroma o mancha
objetables que hayan sido absorbidas desde materias
extrañas durante su procesamiento y almacenamiento.
c) No haber comenzado a fermentar o producir
efervescencia.
d) No haber sido sometida a extracción de polen ni
ningún constituyente particular de la miel, excepto cuando
sea imposible evitarlo para garantizar la ausencia de
materias extrañas, inorgánicas u orgánicas.
e) No deberá calentarse ni elaborarse la miel de forma
tal que se modifique su composición esencial y/o se
menoscabe su calidad.
f) No se deberán utilizar tratamientos químicos o
bioquímicos para influir en la cristalización de la miel.
g) Debe contener como máximo 20% de agua, con
excepción de las mieles descritas en la norma del Codex
Alimentarius para la miel "Norma para la Miel CODEX STAN
12-1981", de acuerdo a su última versión, para las cuales
regirá el valor según corresponda.
h) Debe contener no menos de 60 gramos de fructosa más
glucosa por 100 gramos de miel o 45 gramos de fructosa más
glucosa por 100 gramos de miel de mielada o mezclas de miel
de mielada con miel de flores.
i) Debe contener no más de 5 gramos de sacarosa por
100 gramos de miel con excepción de las mieles descritas en
la norma del Codex Alimentarius para la miel "Norma para la
Miel CODEX STAN 12-1981", de acuerdo a su última versión,
para las cuales regirá el valor que corresponda.
j) No debe contener más de 0,1 gramo de sólidos
insolubles en agua por 100 gramos de miel obtenida mediante
la centrifugación de los panales desoperculados, sin
larvas, u obtenida mediante el drenaje de los panales
desoperculados, sin larvas, o no contener más de 0,5 gramo
de sólidos insolubles en agua por 100 gramos de miel
obtenida mediante el prensado de los panales, sin larvas.
Los envases de miel destinados al consumidor final
deberán rotular en su cara principal la siguiente frase:
"Este producto no debe ser consumido por menores de 12
meses". Las características de las letras deberán
corresponder a lo establecido en el artículo 115, letra c),
números 1 y 2, de este reglamento.
|
| Decreto 75, SALUD
Art. 1 N° 3
D.O. 12.11.2019 |
|
Artículo 393 bis.- Se entenderá
por "polen corbicular" el conglomerado de polen extraído
desde las flores por la abeja de la especie Apis mellifera,
la cual mezcla y aglutina con secreciones salivales y
néctar, para ser depositadas en forma de gránulos
redondeados en las corbículas de su tercer par patas
traseras y transportadas a la colmena. Para efectos de
rotulación, se aceptará el uso de la denominación
"polen", "polen de abeja", "polen granulado" u otro que
informe a los consumidores sobre la naturaleza de este
producto, resguardando el cumplimiento del artículo 110 del
presente reglamento.
Se entenderá por "jalea real" la sustancia cremosa
semifluida de color blanco amarillento, de sabor ácido,
ligeramente picante, la cual es producida por la acción
combinada de la glándula hipofaringeas y por la glándula
mandibulares de las abejas nodrizas de la especie Apis
mellifera
|
| Decreto 75, SALUD
Art. 1 N° 4
D.O. 12.11.2019 |
|
Artículo 394.- Podrá denominarse como "miel de
palma" al producto dulce, viscoso y de color
caramelo oscuro, obtenido por concentración de savia de
palma chilena (Jubea chilensis). El producto no deberá
contener saborizantes/aromatizantes, preservantes,
espesantes y/o colores artificiales.
|
| Decreto 75, SALUD
Art. 1 N° 5
D.O. 12.11.2019 |
|
TITULO XVIII
De los productos de confitería y similares
|
|
Párrafo I
De la confitería de azúcar
|
|
Artículo 395.- Productos de confitería son
las preparaciones de diferentes formas de
presentación y consistencia, que contienen azúcares como
materia básica característica, o en su reemplazo total o
parcial edulcorantes no nutritivos, con o sin adición de
miel, leche, materias grasas, frutas al estado natural o
elaboradas, semillas u otros ingredientes y aditivos
permitidos.
|
| Decreto 106, SALUD
Art. 1 Nº 30
D.O. 23.04.2009 |
|
Párrafo II
De los productos del cacao y del chocolate
|
|
Artículo 396.- Semilla de cacao o cacao en grano es la
semilla sana y limpia del Theobroma cacao L., que ha sido
sometida a fermentación y posterior desecación. Deberá
contener como máximo 8% de humedad, 12% de cáscara y no
contener insectos o sus estados evolutivos.
|
|
Artículo 397.- Cacao o cacao en polvo es el producto
obtenido de la pulverización de la torta de cacao. Deberá
contener como máximo 8% de humedad y 5% de cascarillas o
sustancias extrañas, expresadas sobre materia seca
desgrasada. Si su contenido de materia grasa es igual o
superior al 10% se denominará "Cacao natural en polvo" y si
es menor de 10% se denominará como "Cacao desgrasado en
polvo".
|
|
Artículo 398.- Chocolate es el producto
homogéneo obtenido de un proceso de
fabricación adecuado de materias de cacao que puede ser
combinado con productos lácteos, azúcares y/o
edulcorantes, emulsificadores y/o saborizantes. Debe
contener como mínimo 20% de sólidos de cacao del cual, por
lo menos 18% será manteca de cacao. Pueden agregarse hasta
un límite de un 40% del peso total del producto terminado
otros ingredientes alimenticios.
|
| DTO 475, SALUD
Art. Unico, Nº 109
D.O. 13.01.2000 |
|
Artículo 399.- Chocolate sucedáneo es el producto en
el que la manteca de cacao ha sido reemplazada parcial o
totalmente por materias grasas de origen vegetal, debiendo
poseer los demás ingredientes del chocolate. Deberá
contener como mínimo un 4% de sólidos no grasos de cacao y
su humedad no deberá ser superior al 3%. El chocolate
sucedáneo de leche deberá contener un mínimo de 12% de sólidos de leche
desgrasados y el chocolate blanco sucedáneo deberá
contener como mínimo un 4% de manteca de cacao. En la
rotulación de estos productos deberá destacarse claramente
Sabor a chocolate.
|
| DTO 475, SALUD
Art. Unico, Nº 110
D.O. 13.01.2000 |
|
Artículo 400.- Cacao azucarado en polvo es el producto
obtenido a partir de cacao en polvo, con la adición de
azúcar y destinado a ser disuelto en agua o leche. Deberá contener como
máximo 65% de azúcar y como mínimo 20% de sólidos de
cacao. Podrá llevar adicionado leche en polvo u otros
ingredientes y aditivos
permitidos, no podrá contener colorantes.
| NOTA: El Art. segundo
del DTO 68, Salud, publicado el 23.01.2006, dispuso que la
modificación introducida al presente artículo rige a
contar de 180 días después de su publicación.
|
|
| DTO 68,
SALUD
Art. primero Nº 28
D.O. 23.01.2006 |
|
Párrafo III
De los productos en polvo para preparar postres y
refrescos
|
|
Artículo 401.- Con el nombre genérico de producto en
polvo para preparar postres y refrescos, se denominan los
productos en polvo o granulados que, por dispersión en agua
y/o leche, permiten la obtención de las preparaciones
correspondientes (gelatinas, flanes, budines, refrescos u
otros).
|
|
Artículo 402.- Polvos para preparar postres de
gelatina son los productos constituidos por mezclas de
gelatina y azúcares o edulcorantes autorizados, adicionados
o no de acidulantes, saborizantes, colorantes y otros
ingredientes autorizados por este reglamento. Su contenido
máximo de humedad será de 5%. Cuando se utilicen otros
espesantes o hidrocoloides autorizados que no sea gelatina de
origen animal, deberá indicarse en el rótulo "gelatina de
origen vegetal", sin perjuicio de la
correspondiente declaración de
los nombres específicos de los espesantes o hidrocoloides
constituyentes.
| NOTA: El
artículo transitorio del DTO 115, Salud, publicado el
25.11.2003, dispone que la modificaciones a este artículo,
regirán 180 días después de su publicación.
|
|
| DTO 115, SALUD
Art. primero Nº 20
D.O. 25.11.2003 |
|
Artículo 403.- La gelatina utilizada en la
elaboración de postres debe provenir de la
hidrólisis selectiva del colágeno principal proteína
estructural de la piel, tejido conectivo y huesos de
animales sanos. Deberán
cumplir con las normas de identidad y pureza de
FAO/OMS.
| NOTA: El
artículo transitorio del DTO 115, Salud, publicado el
25.11.2003, dispone que la modificaciones a este artículo,
regirán 180 días después de su publicación.
|
|
| DTO 115, SALUD
Art. primero Nº 21
D.O. 25.11.2003 |
|
Artículo 404.- Polvos para preparar refrescos
o bebidas instantáneas en polvo son
los productos constituidos por azúcares o mezclas de
azúcares y edulcorantes autorizados o mezclas de
edulcorantes autorizados,
acidulantes, saborizantes, colorantes, con o sin adición de
enturbiantes y otros ingredientes.
Estos productos deberán contener lo siguiente:
a) porcentaje máximo de humedad de 5% al momento de
envasar estos productos;
b) porcentaje máximo de cenizas totales 2% con excepción
de los enriquecidos o fortificados, para los cuales no
regirá este límite;
c) porcentaje mínimo de 85% de azúcares totales en peso
del producto final, salvo para los refrescos o bebidas
instantáneas en polvo, en los que se ha sustituido total o
parcialmente los azúcares por edulcorantes no nutritivos.
| NOTA: El Art. segundo
del DTO 68, Salud, publicado el 23.01.2006, dispuso que la
modificación introducida al presente artículo rige a
contar de 180 días después de su publicación.
|
|
| DTO 68, SALUD
Art. primero Nº 29
D.O. 23.01.2006 |
|
Artículo 405.- La rotulación de edulcorantes en estos
productos deberá ajustarse a lo estipulado en el Título
III. De los Aditivos Alimentarios de este reglamento.
|
|
TITULO XIX
De las confituras y similares
|
|
Artículo 406.- Con la denominación genérica de
"confituras", se entienden los productos obtenidos por
cocción de frutas, hortalizas o tubérculos (enteros o
fraccionados), sus jugos y/o pulpas, con azúcares (azúcar,
dextrosa, azúcar invertido, jarabe de glucosa o sus
mezclas) con o sin adición de otros edulcorantes, aditivos
e ingredientes. Comprenden mermeladas, dulces, jaleas,
frutas confitadas, glaseadas, cristalizada o escarchadas,
escurridas y almibaradas.
|
|
Artículo 407.- Las frutas y hortalizas confitadas,
glaseadas cristalizadas o escarchadas, escurridas y
almibaradas, deberán cumplir con lo siguiente:
a) deben estar libres de hojas, fragmentos de insectos y
materias ajenas al producto;
b) los frutos deben poseer un mínimo de transparencia,
brillo y turgencia y su textura debe ser firme y no
desintegrarse al ser presionada entre los dedos;
c) podrán contener colorantes y aromatizantes u otros
aditivos autorizados.
|
|
TITULO XX
De las conservas
|
|
Párrafo I
Disposiciones generales
|
|
Artículo 408.- Conserva es el producto
alimenticio contenido en envase herméticamente
sellado y que ha sido sometido posteriormente a un
tratamiento térmico que garantice su esterilidad comercial.
|
| DTO 475, SALUD
Art. Unico, N° 113
D.O. 13.01.2000 |
|
Artículo 409.- Envase herméticamente sellado es aquel
que ha sido diseñado para impedir la entrada de
microorganismos durante y después del tratamiento térmico,
con el objeto de mantener la esterilidad comercial.
|
|
Artículo 410.- Tratamiento térmico son las
condiciones de tiempo y temperatura necesarias para
conseguir la esterilidad comercial.
|
|
Artículo 411.- Tratamiento programado es el
tratamiento térmico utilizado por el fabricante para un
producto determinado y un tamaño de envase definido, para
conseguir la esterilidad comercial.
|
|
Artículo 412.- Esterilidad comercial es el estado que
se consigue aplicando calor suficiente, solo o en
combinación con otros procesos de conservación de
alimentos, que aseguren la destrucción de formas viables de
microorganismos patógenos y de otros microorganismos
capaces de alterar el producto y que pudieran multiplicarse
a temperatura ambiente, durante su almacenamiento y
distribución.
|
|
Artículo 413.- Alimento ácido es todo alimento cuyo
pH natural sea de 4.5 o menor.
|
|
Artículo 414.- Alimento de baja acidez es cualquier
alimento con un valor de pH mayor de 4.5 y una actividad de
agua mayor de 0.85. Incluye frutas, vegetales o productos
vegetales de acidez naturalmente baja, a los cuales se les
ha reducido el pH por acidificación, previo a su
tratamiento térmico.
|
|
Artículo 415.- Alimento en conserva acidificado es
todo alimento que haya sido tratado para obtener un pH de
equilibrio de 4.5 o menor después del tratamiento térmico.
|
|
Artículo 416.- El agua utilizada para el enfriamiento
de las conservas deberá ser clorada, debiendo controlarse,
para asegurar en todo momento un nivel no inferior a 0,2
mg/l de cloro libre residual. Si esta agua se recircula debe
separarse toda materia orgánica insoluble.
|
| DTO 475, SALUD
Art. Unico, N° 114
D.O. 13.01.2000 |
|
Artículo 417.- Se debe asegurar la hermeticidad de
las conservas mediante procedimientos
idóneos. Se deberá llevar un registro de los controles de
hermeticidad.
|
| DTO 475, SALUD
Art. Unico, N° 115
D.O. 13.01.2000 |
|
Artículo 418.- Los autoclaves utilizados en el
tratamiento térmico deben estar provistos de un termómetro
de precisión de 1ºC y además de un dispositivo de
registro de la temperatura y tiempo de esterilización.
|
|
Artículo 419.- Se prohíbe la tenencia, distribución
y expendio de conservas cuyos envases se presenten
hinchados, abollados, con evidencia de haber perdido su
hermeticidad por daño en sus cierres, visiblemente oxidados
o que haya excedido el plazo recomendado para su consumo
establecido por el fabricante. Estos productos no podrán
ser reprocesados para consumo humano.
|
|
Artículo 420.- En productos en conserva, la fecha
o código de elaboración se estampará
en una de las tapas del envase bajo relieve o con equipos
automáticos de impresión mediante tinta indeleble, en la
forma y orden establecidos en este reglamento.
|
| DTO 475, SALUD
Art. Unico, N° 116
D.O. 13.01.2000 |
|
Párrafo II
De los requisitos para alimentos de baja acidez
|
|
Artículo 421.- El tratamiento térmico deberá ser
establecido por el fabricante para cada producto,
formulación y formato mediante instrumentos y estudios de
curvas de penetración de calor realizados en los autoclaves
de la industria. Este tratamiento deberá supervisarse por
personal técnicamente competente.
|
|
Párrafo III
De los requisitos para alimentos en conserva
acidificados
|
|
Artículo 422.- Deberá llevarse en registro para cada
carga que contenga la siguiente información:
a) condiciones del tratamiento térmico;
b) productos empleados para el ajuste del pH.
El producto final deberá tener un pH de equilibrio
igual o menor a 4,5.
|
|
Párrafo IV
De los requisitos para conservas de carne
|
|
Artículo 423.- Las conservas de carne no
deberán contener más de 100 mg/Kg de nitrito
residual, expresado como nitrito de sodio.
|
| DTO 475, SALUD
Art. Unico, N° 117
D.O. 13.01.2000 |
|
TITULO XXI
De los encurtidos
|
|
Artículo 424.- Encurtidos o pickles son los frutos u
hortalizas sometidas a fermentación láctica con adición
de sal, conservados o no en vinagre. Los encurtidos deben
cumplir los siguientes requisitos:
a) las frutas y hortalizas utilizadas como materias primas
deberán ser sanas, de madurez adecuada y estar libres de
alteraciones producidas por agentes físicos, químicos o
biológicos;
b) el líquido de cobertura de los encurtidos conservados
en vinagre deberá tener una acidez mínima de 1,5%
expresada como ácido acético, y un pH no mayor de 3,8 (a
20ºC).
Debe contener un máximo de 100 mg/kg de anhídrido
sulfuroso total, cuando las materias primas hayan sido
tratadas con sulfito, bisulfitos o anhídrido sulfuroso.
|
|
Artículo 425.- Las aceitunas conservadas por
esterilización térmica (como las aceitunas aderezadas
ennegrecidas por oxidación) deberán haber recibido un
tratamiento suficiente, tanto en tiempo como en temperatura
para destruir las esporas de Clostridium botulinum.
|
|
TITULO XXII
De los caldos y sopas deshidratadas
|
|
Artículo 426.- Caldo deshidratado es el
producto constituido por verduras o mezclas de
carne y sus extractos, grasa, sal comestible, condimentos,
especias y acentuantes del sabor. Pueden contener verduras
deshidratadas, proteínas hidrolizadas, extractos de
levaduras y aditivos autorizados en este reglamento. Los
caldos deshidratados no deben contener más de un 5% de
humedad y reconstituidos de acuerdo a su rotulación, deben
contener como máximo 12,5 g de cloruro de sodio y como
mínimo 100 mg de nitrógeno total por litro de caldo. Los
caldos de carne de vacuno deben contener como mínimo 20 mg
de creatinina total y los de otras carnes 10 mg de
creatinina total por litro de caldo preparado.
|
| DTO 475, SALUD
Art. Unico, N° 118
D.O. 13.01.2000 |
|
Artículo 427.- Sopas y sopas cremas deshidratadas son
aquellos productos elaborados a base de mezclas de cereales
y sus derivados, leguminosas sometidas a tratamiento
térmico, verduras deshidratadas, callampas, carnes en
general incluyendo las de aves, pescados y mariscos, leche y
sus derivados, alimentos grasos, extractos de carnes y
levaduras, proteínas hidrolizadas, sal, especias y sus
extractos y otros productos alimenticios acentuantes del
sabor y aditivos permitidos. Para su consumo requieren la
adición de agua y cocción de acuerdo a lo indicado en su
rotulación. Las sopas cremas deshidratadas deberán
contener como mínimo 0,8% de nitrógeno total y como
máximo un 8% de humedad. Deberán contener por litro de
sopa como máximo 12,5 g de cloruro de sodio. Las sopas
cremas en cuyas denominaciones se haga alusión a la
presencia de carne, deben contener como mínimo 60 mg de
creatinina total por litro de sopa preparada cuando
corresponda a variedades con carne de vacuno y 10 mg de
creatinina total en variedades con otras carnes.
|
| DTO 475, SALUD
Art. Unico, N° 119
D.O. 13.01.2000 |
|
Artículo 428.- Sopas y sopas cremas deshidratadas
instantáneas no necesitarán cocción y para ser consumidas
sólo requieren la adición de agua de acuerdo a las
instrucciones de preparación indicadas en su rótulo. Deben
cumplir los mismos requisitos que las sopas y sopas cremas
deshidratadas no instantáneas.
|
|
Artículo 429.- La creatinina de los caldos, sopas y
sopas cremas debe corresponder exclusivamente a los
componentes del producto natural.
|
|
TITULO XXIII
De las especias, condimentos y salsas
|
|
Párrafo I
De las especias
|
|
Artículo 430.- La denominación de "especias"
comprende a plantas o partes de ellas (raíces, rizomas,
bulbos, hojas, cortezas, flores, frutos y semillas) que
contienen sustancias aromáticas, sápidas o excitantes, o
sus principios activos suspendidos en un soporte alimenticio
adecuado, empleadas para condimentar alimentos y bebidas. Se
incluyen en esta denominación, entre otras, las siguientes
especias:
Anís común o verde : Frutos desecados del Pimpinela
anisum L.
Anís estrellado : Frutos del Illicium verum H.
Azafrán : Filamentos de color rojo-anaranjado
provenientes de los estigmas
desecados de
la flor del Croccus sativus L.
Canela de Ceylán : Corteza desecada y privada en su
mayor
parte de la capa epidérmica,
proveniente el
Cinnamomum zeylanicum N. Toda canela
que
no corresponda a los caracteres macro
y
microscópicos de la de Ceylán, como
la del
Cinnamomum cassia, debe denominarse
"canela
común"
Cardamomo : Semillas del Elettaria cardamomum L.
Clavo de olor : Botones florales secos del
Caryophyllus
aromaticus L. o Eugenia Caryphyllata
T.
Comino : Frutos del Cuminum cyminum L.
Comino alemán o
alcaravea : Frutos del Carum carvi L.
Curcuma : Rizoma del Curcuma longa L.
Curry : Mezcla de especies de sabor picante,
constituida por diversas especias
como
pimientas, jengibre, cúrcuma y otros
condimentos
Jengibre : Rizoma lavado y desecado de Zingiber
officinale R.
Macis : Envoltura o arilo que recubre la
semilla de
la nuez moscada Myristica fragans H.
Mejorana : Hojas y partes aéreas floridas del
Origa
num mejorana L.
Menta piperita : Hojas y partes aéreas floridas de la
Mentha
piperita L.
Mostaza blanca : Semillas de la Sinapis alba
Mostaza negra : Semillas de la Brassica nigra L.
Nuez moscada : Semilla desecada de Myristica fragans
H.,
desprovista totalmente de su
envoltura
(macis)
Pimienta blanca : Fruto maduro y seco, privado de la
parte
exterior de su pericarpio,
proveniente del
Piper nigrum L.
Pimienta negra : Fruto incompletamente maduro y seco,
proveniente del Piper nigrum L.
Pimienta de Jamaica : Fruto de Pimienta officinalis B. o
Allspice
Pimienta de Cayena : Frutos especialmente picantes del
Capsicum
frutescens
Vainilla : Fruto inmaduro, fermentado y desecado
de
vainilla olanifolia A.
|
|
Artículo 431.- Las especias deben ser sanas, limpias,
genuinas y presentar las características que les son
propias. Deben contener la totalidad de sus principios
activos y estar privadas de otras partes del vegetal exentas
de valor como condimento.
|
|
Artículo 432.- Las especias no deben estar agotadas,
alteradas, contaminadas con insectos o parásitos, ni en mal
estado de conservación o higiene. Queda prohíbido
adicionarles sustancias inertes, amiláceas o cualquier otra
materia extraña.
|
|
Artículo 433.- Las especias que a continuación se
indican deben cumplir con los siguientes límites de
humedad, cenizas totales,cenizas insolubles en ácido
clorhídrico, fibra cruda y esencias:
Especia Humedad Cenizas Cenizas Fibra
Esen-
materias totales insolubles cruda
cia
volátiles HCL 10
máx. % máx. % máx. % máx.
% mín.%
Anís común 13 9,0 1,5 -
2
Anís estrellado - 3,0 1 -
4,5
Azafrán 15 8 1 5
4,5
Canela de Ceylán 10 6 2 20
2
Cardamomo 12 8 3 -
0,5
Clavo de olor 15 8 2 15
2
Comino 9 9,5 1 7
0,3
Comino alemán 9,5 9 1 18
10
Curcuma 10 8 1 6
2,5
Jengibre 14 7,5 2 8
2,5
Macis 17 3 0,5 10
4
Mejorana 15 15 5 19
0,7
Menta piperita 12 12 1 -
0,8
Mostaza blanca - 5 1 22
-
Mostaza negra - 5 1,5 -
0,6
Nuez moscada 14 5 0,8 20
5
Pimienta blanca 15 2 0,3 5
1,5
Pimienta negra 12 7 1 12,5
2
Pimienta de 10 8 1 -
-
Cayena
Pimienta de 10 6 0,4 25
-
Jamaica
Vainilla 30 7 - -
1,5
|
|
Artículo 434.- Si se sustituye la vainilla natural por
vainillina o etil-vainillina, los rótulos y publicidad
deberán indicar: "aromatizado con vainillina o
etil-vainillina".
|
|
Párrafo II
De la Sal Comestible
|
|
Artículo 435.- Sal comestible es el cloruro de sodio
proveniente de depósitos geológicos, de lagos salados o de
agua de mar. Se incluye en esta definición aquella destinada al consumo directo,
así como aquella destinada a la elaboración y preparación
de alimentos por la industria.
|
| DTO 475,
SALUD
Art. Unico, N° 120
D.O. 13.01.2000 |
|
Artículo 436.- La sal comestible, sin
otra denominación, sea cristalizada o
molida, deberá contener un mínimo de 97% de cloruro de
sodio en base seca, con exclusión de los aditivos.
|
| Decreto 33, SALUD
Art. 1 N° 1
D.O. 28.11.2016 |
|
Artículo 437.- La sal comestible con menor
contenido de sodio deberá ceñirse a las
especificaciones que para cada descriptor nutricional
establece el artículo 120 del presente reglamento.
|
| DTO 475, SALUD
Art. Unico, N° 121
D.O. 13.01.2000 |
|
Artículo 438.- Toda sal comestible deberá
contener yodo adicionado, en forma de yodatos
o de yoduros de sodio o de potasio, en una concentración
entre 0,015 y 0,025 gramos de yodo por kilogramo de
sal. Cuando se utilicen
sucedáneos de la sal comestible o sal baja en sodio, ella
deberá ser yodada según lo dispuesto en el inciso
anterior.
Se exceptuarán de la utilización de sal yodada los
quesos en general, frescos, semimaduros y maduros.
| NOTA El artículo
segundo transitorio del Decreto 70, Salud, publicado el
11.11.2022, dispone que el rango de concentración de yodo
en la sal señalado en la presente norma, entrará en
vigencia en forma progresiva conforme a lo señalado en el
cuadro contenido en la referida disposición. |
|
| Decreto 70, SALUD
Art. 1° N° 1
D.O. 11.11.2022 |
|
Artículo 439.- Toda sal comestible deberá estar
exenta de cualquier sustancia tóxica. No
deberá contener:
a) más de 0,5% de nitratos, expresados como nitrato de
potasio;
b) no más de 1,5% de sulfatos expresados como sulfato de
sodio;
c) no más de 1% de sólidos insolubles en agua; y
d) no más de 1 mg/kg de nitritos como NO 2 .
|
| DTO 475, SALUD
Art. Unico, N° 123
D.O. 13.01.2000 |
|
Párrafo III
Del Vinagre
|
|
Artículo 440.- La designación de "vinagre" o "vinagre
de vino" corresponde al producto de la fermentación
acética del vino. Los vinagres obtenidos por fermentación
de otras bebidas o líquidos alcohólicos deberán llevar,
en la rotulación de sus envases, la declaración de
"vinagre...", seguido del nombre de la materia prima de
origen.
|
|
Artículo 441.- El vinagre o vinagre de vino debe
presentar las siguientes características: a) líquido de
color, olor y sabor propios de su naturaleza,
límpido, sin presentar hongos y levaduras, ni otras
alteraciones;
b) su contenido de alcohol no debe sobrepasar el 1% en
volumen y su acidez total, expresada en ácido
acético, debe ser como mínimo 5%;
c) deberá contener como mínimo 10 g/l de extracto seco,
una acidez fija, expresada en tartrato ácido de
potasio, de 5g/l y cenizas totales 1 g/l.
|
| DTO 475,
SALUD
Art. Unico, N° 124
D.O. 13.01.2000 |
|
Artículo 442.- Los vinagres que no procedan de vino
(alcohol, azúcares, hidromiel, zumos de frutas, cerveza,
malta, sidra, suero lácteo u otros) corresponderán a la
composición normal de sus materias de origen y su acidez
total, expresada en ácido acético, no será inferior a 4%.
|
|
Artículo 443.- Los vinagres, en general, no deben
contener sustancias extrañas a su materia prima de origen,
ni se aceptará que sean adicionados de ácidos minerales ni
orgánicos, incluso ácido acético, materias acres,
irritantes o tóxicas, colorantes extraños como tampoco, de
otras sustancias destinadas a realzar artificialmente las
propiedades características de los vinagres genuinos.
|
|
Artículo 444.- No se permitirá la elaboración,
distribución o expendio bajo el nombre de vinagre, de
productos a base de ácido acético o láctico, que no
provengan de la fermentación acética natural de los
productos de origen.
|
|
Párrafo IV
De las Salsas
|
|
Artículo 445.- Se denomina salsa a los productos
preparados, de consistencia líquida o semilíquida a base
de pulpa de frutos, condimentos naturales o elaborados,
ácidos orgánicos, productos aromáticos o picantes,
azúcares, sal u otros productos permitidos.
|
|
Artículo 446.- Salsa de mostaza es la mezcla de harina
de mostaza con vinagre, sal, otros condimentos y acidulantes
permitidos. Debe responder a los siguientes requisitos:
a) contener hasta un máximo de 75% de humedad;
b) no contener menos de un 0,1% de esencia de mostaza
natural, expresada en base seca;
c) contener hasta un máximo de 12% de cenizas totales,
expresadas en base seca;
e) acidez no menor de 1% expresada como ácido acético.
|
|
Artículo 447.- Toda mezcla con otras sustancias
espesantes, colorantes permitidos u otros ingredientes no
señalados en la definición de salsa de mostaza, sólo
puede expenderse como "condimento de mostaza".
|
|
Artículo 448.- Salsa de tomates es el producto
resultante de la molienda y tamizaje parcial de tomates de
las variedades rojas (Lycopersicum esculentum Mill), sanos,
maduros, cuya pulpa y jugo parcialmente libre de piel y
semillas ha sido concentrado por evaporación y adicionado
de condimento, sal y aditivos permitidos. Debe responder a
los siguientes requisitos:
a) sólidos solubles mínimo 8° Brix;
b) acidez total expresada como ácido cítrico anhidro,
máximo 2,5%.
|
|
Artículo 449.- Ketchup es el producto obtenido de la
molienda y tamizaje de tomates de las variedades rojas
(Lycopersicum esculentum Mill.), sanos y maduros cuya pulpa
y jugo, libre de piel y semillas ha sido evaporado y
adicionado de vinagre, azúcar, condimentos, sal y aditivos
permitidos. Debe responder a los siguientes requisitos:
a) sólidos solubles mínimo 26º Brix;
b) pH:4,4 como máximo.
|
|
Artículo 450.- Mayonesa es la emulsión de
aceite comestible en huevo y agua,
adicionada de vinagre, jugo de limón, otros ácidos
orgánicos, sal comestible, condimentos y aditivos. Se
permite la adición de caroteno y otros aditivos
autorizados.
En los locales de atención a público que ofrezcan o
incluyan mayonesa en alimentos, la mayonesa sólo se podrá elaborar a base de
huevos pasteurizados, líquidos, congelados o deshidratados
que cumplan con las especificaciones microbiológicas del
artículo 173 del presente reglamento o estar lista para el
consumo procedente de fábricas autorizadas
|
| DTO 475, SALUD
Art. Unico, N° 125
D.O. 13.01.2000 |
| Decreto 11,
SALUD
Art. 1 N° 1
D.O. 29.10.2011 |
|
Artículo 451.- Aderezos para ensaladas (salad
dressings) son las emulsiones en las cuales el aceite comestible se
encuentra finamente disperso en un medio acuoso que puede
contener uno o más de los siguientes ingredientes: sal,
azúcares, vinagre, especias, huevo y/o derivados lácteos y
aditivos autorizados. En caso de incluir huevo, deberá
cumplirse con lo establecido en el artículo precedente.
|
| Decreto 11, SALUD
Art. 1 N° 2
D.O. 29.10.2011 |
|
TITULO XXIV
De los estimulantes o fruitivos
|
|
Párrafo I
Del té
|
|
Artículo 452.- Té, sin otra denominación es el
producto obtenido de hojas tiernas, yemas, pecíolos o
pedúnculos, sanos y limpios de las especies del género
Thea, preparado por deshidratación, con o sin
fermentación/oxidación enzimática.
|
| Decreto 32, SALUD
Art. 1 N° 1
D.O. 26.01.2013 |
|
Artículo 453.- Las materias primas para la
elaboración de los distintos tipos de té deben
cumplir con los siguientes requisitos:
a) Contener un máximo de:
20% de tallos, pecíolos o pedúnculos en conjunto.
12% de humedad.
8% de cenizas totales y 1% de cenizas insolubles en
ácido clorhídrico
al 10%, ambos expresados en base seca.
b) Contener un mínimo, expresado en base seca, de 1% de
cafeína.
Los té elaborados podrán comercializarse en distintas
formas, hojas, molido, bolsitas preparadas o líquida como
infusión o reconstituida con agua, ya sea solo o en mezcla,
los que, al igual que todos los alimentos, deben rotularse y
comercializarse de acuerdo a lo establecido en el Título
II, párrafo II, del Reglamento Sanitario de los Alimentos,
de acuerdo a sus características y composición.
Té en polvo soluble o té instantáneo es el producto
resultante de la deshidratación del extracto obtenido,
exclusivamente, a partir del té hasta consistencia de
polvo. No debe tener menos de 2,0% de cafeína en base seca
y su humedad no debe ser mayor a 5%.
|
| Decreto 32, SALUD
Art. 1 N° 2
D.O. 26.01.2013 |
|
Párrafo II
De la Yerba Mate
|
|
Artículo 454.- Yerba Mate es el producto constituido
por hojas, ramas jóvenes, brotes, pecíolos o pedúnculos
desecados, ligeramente tostados o desmenuzados, de especies
del género Ilex (I.brasiliensis, I. paraguariensis). La
yerba mate elaborada debe cumplir con los siguientes
requisitos:
a) contener un mínimo de 0,7% de cafeína y de 25% de
extracto acuoso, expresados en base seca;
b) no contener más de 11% de humedad 9% de cenizas
totales, 1,5% de cenizas insolubles en ácido clorhídrico
al 10% y 30% de palos que no pasen por un tamiz con
perforaciones de 70 mm de largo y 2,5 mm de ancho.
c) no contener sustancias vegetales extrañas: máximo
1,0%, semillas de yerba mate: máximo 1,0% y no
deberá estar quemada, alterada o agotada.
La yerba mate podrá comercializarse en distintas
formas, hojas, polvo, preparada o líquida como infusión o
reconstituida con agua, ya sea sola o en mezcla, los que al
igual que todos los alimentos deben rotularse y
comercializarse según lo establecido en el Título II,
párrafo II, del Reglamento Sanitario de los Alimentos, de
acuerdo a sus características y composición."
|
| Decreto 32, SALUD
Art. 1 N° 3
D.O. 26.01.2013 |
|
Párrafo III
Del café
|
|
Artículo 455.- Café tostado es el producto
constituido por las semillas sanas y limpias de
las diferentes especies del género Coffea, que por medio
del calor han tomado una coloración oscura y aroma
característico. No contendrá más de: 5% de granos
carbonizados 1% de materias extrañas 5% de humedad
Contendrá como mínimo 0,9% de cafeína y 20% de extracto
acuoso, ambos expresados en base seca. El café tostado
descafeinado no deberá tener más de 0,1% de cafeína,
expresado en base seca.
|
| DTO 475, SALUD
Art. Unico, N° 125
D.O. 13.01.2000 |
|
Artículo 456.- Café soluble o café instantáneo es
el producto resultante de la
deshidratación del extracto obtenido exclusivamente a
partir del café en grano recientemente tostado y secado
hasta consistencia de polvo o gránulo, sin adición de
otros ingredientes. Su contenido de humedad no debe ser
mayor a 5%.
El café soluble o instantáneo descafeinado no deberá
tener más de 0,3% de cafeína, expresado en base seca.
El café tostado y café soluble o instantáneo,
descafeinado o no, se podrá comercializar en distintas
formas, grano, polvo, preparados o líquidos como infusión
o reconstituidos con agua, ya sea solo o en mezcla, los que,
al igual que todos los alimentos, deben rotularse y
comercializarse según lo establecido en el Título II,
párrafo II, del Reglamento Sanitario de los Alimentos, de
acuerdo a sus características y composición.
|
| Decreto 38, SALUD
Art. 1 N° 5
D.O. 02.02.2021 |
| Decreto 32, SALUD
Art. 1 N° 4
D.O. 26.01.2013 |
|
Artículo 457.- Sucedáneos del café son aquellos
productos de origen vegetal (soya, higo, achicoria u otros),
que desecados y/o tostados o tostados con azúcar o en
mezcla, permiten la preparación de infusiones semejantes a
la del café. La naturaleza de sucedáneo de café debe
estar claramente indicada en el rótulo.
|
|
Artículo 458.- Sucedáneo del café instantáneo o
soluble es el producto resultante de la deshidratación del
extracto acuoso de los sucedáneos del café mencionados en
el artículo anterior. Su humedad no será mayor a 5% . La
naturaleza de sucedáneo de café instantáneo o soluble
deberá estar claramente indicada en el rótulo.
Los sucedáneos del café y los sucedáneos del café
soluble o instantáneo se podrán comercializar en
distintas formas, polvo, preparados o líquidos como
infusión o reconstituidos con agua, ya sea solo o en
mezcla, los que, al igual que todos los alimentos, deben
rotularse y comercializarse según lo establecido en el
Título II, del párrafo II, del Reglamento Sanitario de los
Alimentos, de acuerdo a sus características y composición.
|
| Decreto 32, SALUD
Art. 1 N° 5
D.O. 26.01.2013 |
|
Párrafo IV
De las hierbas aromáticas
|
|
Artículo 459.- La denominación de hierbas
aromáticas comprende ciertas plantas o partes de ellas
(raíces, rizomas, bulbos, hojas, cortezas, flores, frutos y
semillas) que contienen sustancias aromáticas, y que por
sus sabores característicos, se destinan a la preparación
de infusiones de agrado.
|
| DTO 475, SALUD
Art. Unico, N° 126
D.O. 13.01.2000 |
|
Artículo 460.- Las hierbas aromáticas deben ser
genuinas, sanas, presentar las características
macroscópicas y microscópicas que les son propias. No
deben contener materias o cuerpos extraños a su naturaleza
ni más de 20% de otras partes del vegetal exentas de valor
como aromatizantes.
|
|
Artículo 461.- Las hierbas aromáticas deben contener
la totalidad de sus principios activos y otros metabolitos
secundarios de importancia para su caracterización
química.
|
|
Artículo 462.- Las hierbas aromáticas pueden expenderse enteras o molidas, ya sea
solas o en
mezclas.
| NOTA:
El artículo transitorio del DTO 115, Salud, publicado el
25.11.2003, dispone que la modificaciones a este artículo,
regirán 180 días después de su publicación.
|
|
| DTO
115, SALUD
Art. primero Nº 22
D.O. 25.11.2003 |
|
Artículo 463.- Las hierbas aromáticas no deberán
tener materias o sustancias contaminantes en niveles nocivos
para la salud, ni principios activos en concentraciones terapéuticas,
asimismo las hierbas aromáticas/infusiones no deberán
estar afectas a la ley Nº 19.366, que sanciona el tráfico
ilícito de estupefacientes y
sustancias
sicotrópicas.
| NOTA: El
artículo transitorio del DTO 115, Salud, publicado el
25.11.2003, dispone que la modificaciones a este artículo,
regirán 180 días después de su publicación.
|
|
| DTO 115, SALUD
Art. primero Nº 23
D.O. 25.11.2003 |
|
Artículo 464.- Las hierbas aromáticas deben
envasarse en materiales apropiados que permitan
conservar en condiciones óptimas su sabor y aroma.
Las hierbas aromáticas se podrán comercializar en
distintas formas, hojas, polvo o bolsitas,
preparada o líquida como infusión o reconstituidas con
agua, ya sea solas o en mezcla, las que, al igual que todos
los alimentos, deben rotularse y comercializarse según lo
establecido en el Título II, párrafo II, del Reglamento
Sanitario de los Alimentos, de acuerdo a sus
características y composición.
|
| DTO 475, SALUD
Art. Unico, N° 127
D.O. 13.01.2000 |
| Decreto 32, SALUD
Art. 1 N° 6
D.O. 26.01.2013 |
|
TITULO XXV
De las comidas y platos preparados
|
|
Artículo 465.- Comidas o platos preparados son
aquellas elaboraciones culinarias que se expenden, listos
para su consumo, sean fríos o calientes o que requieran
sólo de un proceso de calentamiento.
Las materias primas, ingredientes y el producto final
deberán cumplir con los requisitos establecidos en este
reglamento.
|
|
Artículo 466.- Las comidas o platos preparados que se
expendan calientes deberán mantenerse y transportarse en
receptáculos térmicos que aseguren la conservación de
éstas a una temperatura uniforme y permanente de 65ºC. Las
comidas o platos preparados que se expendan fríos deberán
conservarse y transportarse a una temperatura máxima de
5ºC.
Esta disposición rige igualmente sobre la
distribución de alimentos en todo tipo de transporte de
pasajeros.
|
|
Artículo 467.- Las vitrinas en que se exhiban comidas
o platos preparados deberán cumplir con los requisitos
establecidos en este reglamento.
|
|
Artículo 468.- Las comidas o platos preparados que
se presenten envasados para la venta,
que se expendan para llevar en porciones y/o variedades
predefinidas por el elaborador deberán rotularse con el
nombre del alimento, domicilio del establecimiento
elaborador del alimento, nombre del representante legal de
este último, número y fecha de la resolución sanitaria
que autorizó el funcionamiento de dicho establecimiento de
alimentos y nombre de la autoridad sanitaria que la emitió,
fecha de elaboración, fecha de vencimiento o plazo de
duración del producto, instrucciones para el
almacenamiento, contenido neto y toda la información
descrita en el artículo 115 del presente reglamento, salvo
el número de porciones por envase.
Esta información deberá estar impresa en el envase o
contenida en una etiqueta adherida al mismo, de modo
visible, indeleble y fácil de leer en circunstancias
normales de compra y uso.
|
| Decreto 13, SALUD
Art. 1 N° 7
D.O. 26.06.2015 |
|
TITULO XXVI
Del agua potable, de las aguas minerales y del hielo
|
|
Artículo 469.- Agua potable es aquella agua apta para
usos alimentarios, y deberá cumplir con la normativa
sanitaria vigente.
|
|
Artículo 470.- Agua mineral de mesa es aquella de
composición química especial proveniente de fuentes
naturales oficialmente registradas, que es apropiada para
servir como bebida de uso común y cuya mineralización es
inferior a 1,5 g/l.
|
|
Artículo 471.- El agua mineral de mesa
deberá obtenerse en condiciones que
garantice la pureza bacteriológica original y envasarse en
su fuente de origen, salvo que su aducción sea hecha desde
la captación al punto de envase por medio de tuberías.
|
| DTO 475, SALUD
Art. Unico, N° 128
D.O. 13.01.2000 |
|
Artículo 472.- El agua mineral natural embotellada
deberá cumplir con la normativa sanitaria vigente. (Decreto Nº 106 de 1997, del
Ministerio de Salud, Reglamento de Aguas Minerales).
|
| DTO
475, SALUD
Art. Unico, N° 129
D.O. 13.01.2000 |
|
Artículo 473.- El agua mineral no deberá contener
los contaminantes ni sobrepasar los
límites de las sustancias que específicamente determina el
Reglamento de Aguas Minerales.
|
| DTO 475, SALUD
Art. Unico, N° 130
D.O. 13.01.2000 |
|
Artículo 474.- La rotulación del envase de agua
mineral, deberá cumplir con los siguientes requisitos
adicionales a los establecidos en el Título II:
a) cuando el producto contenga más de 600 mg/l de sulfato
que no sea sulfato de calcio, se incluirá en forma
destacada la siguiente leyenda " puede ser laxante";
b) cuando el producto contenga más de 1000 mg/l de
sólidos totales disueltos o 600 mg/l de HCO3-, se incluirá
en forma destacada la siguiente leyenda "puede ser
diurético";
c) no se incluirá declaración alguna de propiedades o
efectos medicinales.
|
|
Artículo 475.- El anhídrido carbónico empleado en la
preparación de aguas de bebidas carbonatadas debe contener
un mínimo de 98% de este gas y no más de 0,2% de monóxido
de carbono y estará exento de sustancias extrañas que le
confieran olor y/o sabor desagradable o de cualquiera otra
naturaleza.
|
|
Artículo 476.- Hielo para consumo humano es el
producto obtenido por congelación de agua potable. Sus
características químicas y microbiológicas serán las
exigidas para el agua potable.
|
|
Artículo 477.- Se prohíbe el fraccionamiento del
hielo en barras para ser incorporado a los alimentos.
|
|
TITULO XXVII
De las bebidas analcohólicas, jugos de frutas y hortalizas y aguas envasadas
|
| DTO
68, SALUD
Art. primero Nº 30
D.O. 23.01.2006 |
|
Párrafo I
De las bebidas analcohólicas
|
|
Artículo 478.- Son bebidas analcohólicas aquellas
elaboradas a base de agua potable, carbonatada o no, y
adicionadas de una o más de las siguientes sustancias:
azúcares, jugos de fruta, extractos vegetales, ácidos,
esencias, proteínas, sales minerales, colorantes y otros
aditivos permitidos; que no contengan más de 0,5%
en volumen de alcohol etílico, con
excepción de los jarabes, los que podrán contener hasta
2,5 % en volumen de alcohol etílico.
| NOTA: El Art. segundo
del DTO 68, Salud, publicado el 23.01.2006, dispuso que la
modificación introducida al presente artículo rige a
contar de 180 días después de su publicación.
|
|
| DTO 475, SALUD
Art. Unico, N° 131
D.O. 13.01.2000 |
|
Artículo 479.- Bebida refrescante de fruta, es aquella
bebida analcohólica a la cual se le ha adicionado jugos de
frutas o sus extractos y cuyo contenido de sólidos solubles
procedentes de frutas es igual o mayor al 10% m/m de los
sólidos solubles de la fruta madura que se declara.
|
|
Artículo 480.- Bebida de fantasía, es aquella bebida
analcohólica que no contiene jugos de frutas o sus
extractos, o que ha sido adicionada de éstos pero en
cantidad tal que su contenido de sólidos solubles de fruta
es menor al 10% m/m.
|
|
Artículo 481.- Las bebidas analcohólicas que
contengan cafeína o quinina no deberán exceder la cantidad
de 180 mg/l de cafeína, ni 130 mg/l de quinina o sus sales
expresadas en quinina anhidra.
|
|
Párrafo II
De los jugos, néctares y concentrados de frutas y
hortalizas
|
|
Artículo 482.- Jugo o zumo puro de fruta u hortaliza
es el producto sin fermentar, pero fermentable, pulposo,
turbio o claro, destinado al consumo directo, obtenido por
procedimientos mecánicos a partir de frutas u hortalizas
maduras en buen estado o de sus carnes y conservados
exclusivamente por medios físicos. El jugo podrá haber
sido concentrado y luego reconstituido con agua para
conservar la composición esencial y los factores de calidad
del mismo.
Los productos que usen la expresión de
fantasía "agua de.", siendo líquidos provenientes de una
especie vegetal determinada, deberán rotular, además, el
nombre del alimento de que se trate, en los términos
exigidos por la letra a) del artículo 107 del presente
reglamento, informando la verdadera naturaleza del producto
en forma específica.
|
| Decreto 37, SALUD
Art. 1 N° 2
D.O. 18.01.2017 |
|
Artículo 483.- El jugo o zumo puro de frutas u
hortalizas deberá cumplir los siguientes requisitos:
a) el contenido de sólidos solubles, con exclusión de
los azúcares añadidos, será igual al contenido de
sólidos solubles de la fruta u hortaliza madura de la que
provenga;
b) el producto deberá tener el color, aroma y sabor
característicos de la fruta u hortaliza de origen. Se
permitirá la restitución de los componentes volátiles
naturales del jugo cuando hayan sido extraídos, con
componentes volátiles exclusivamente naturales;
c) cuando el producto lo requiera podrá añadirse uno o
más de los azúcares sólidos definidos en este
reglamento, en una cantidad total que no exceda los 50 g/kg,
excepto para frutas muy ácidas, en cuyo caso no deberá
exceder de 200 g/kg de producto terminado.
|
|
Artículo 484.- Jugo o zumo concentrado es el producto
sin fermentar pero fermentable una vez reconstituido,
conservado exclusivamente por medios físicos y obtenido
mediante un proceso de concentración de jugo puro de fruta
u hortaliza.
El producto obtenido por la reconstitución del jugo
concentrado, mediante la adición de agua en la cantidad
indicada por el fabricante, deberá tener las
características físico-químicas y organolépticas del
jugo de la fruta u hortaliza de origen.
Se permitirá el uso de coadyuvantes de elaboración,
antioxidantes, antiespumantes y acidulantes establecidos en
el presente reglamento.
|
|
Artículo 485.- Néctar de fruta es el producto pulposo
o no pulposo, sin fermentar pero fermentable, obtenido mezclando el jugo o zumo de
fruta y/o toda la parte comestible de frutas maduras y
sanas concentrado o sin concentrar, con adición de
agua y azúcares o miel, y
aditivos autorizados.
| NOTA: El Art. segundo
del DTO 68, Salud, publicado el 23.01.2006, dispuso que la
modificación introducida al presente artículo rige a
contar de 180 días después de su publicación.
|
|
| DTO 68,
SALUD
Art. primero Nº 31
D.O. 23.01.2006 |
| DTO 475, SALUD
Art. Unico, N° 132
D.O. 13.01.2000 |
|
Artículo 486.- El néctar de frutas deberá cumplir
los siguientes requisitos:
a) el contenido de sólidos solubles de los néctares, con
exclusión de azúcares añadidos, será mayor o igual
al 20% m/m
de los sólidos solubles de la fruta madura de la que
provenga;
b) podrán adicionarse uno o más azúcares
sólidos
definidos en este reglamento. La cantidad total de
azúcar o miel adicionada no podrá exceder de 200
g/kg calculados como extracto seco, en el producto
final;
c) el producto deberá tener el color, aroma y
sabor
característico de la fruta con que ha sido
elaborado.
d) ELIMINADA
|
| DTO 475, SALUD
Art. Unico, N° 133
D.O. 13.01.2000 |
| DTO 475, SALUD
Art. Unico, N° 133
D.O. 13.01.2000
DTO 475, SALUD
Art. Unico, N° 133
D.O. 13.01.2000 |
|
Artículo 487.- Los valores mínimos de sólidos
solubles en las frutas que se enuncian a
continuación son referenciales: Frutas
Sólidos solubles,
% m/m mínimo
Boysenberry 10,0
Chirimoya 7,5
Ciruela 10,0
Coco 5,0
Damasco 10,0
Durazno 10,0
Frambuesa 10,0
Frutilla 6,0
Kiwi
8,0
Limón 6,0
Mango 10,0
Maracujá 6,0
Manzana 10,0
Melón 8,7
Membrillo 10,0
Naranja 9,0
Papaya 5,0
Pera
10,0
Piña 10,0
Pomelo 9,0
Tomate 6,0
Uva 13,0
En mezclas de frutas se deberá considerar como base la
fruta que se encuentre en mayor proporción de acuerdo a lo
declarado en la rotulación.
| NOTA: El Art. segundo
del DTO 68, Salud, publicado el 23.01.2006, dispuso que las
modificaciones introducidas al presente artículo rigen a
contar de 180 días después de su publicación.
|
|
| DTO 68, SALUD
Art. primero
Nº 32 a)
D.O. 23.01.2006 |
| DTO
68, SALUD
Art. primero
Nº 32 b)
D.O. 23.01.2006 |
| Decreto 37, SALUD
Art. 1 N° 3
D.O. 18.01.2017 |
| DTO
68, SALUD
Art. primero
Nº 32 b)
D.O. 23.01.2006 |
|
Párrafo III De las aguas envasadas
|
| DTO 68, SALUD
Art. primero Nº 33
D.O. 23.01.2006 |
|
Artículo 487 A.- Aguas envasadas, son aguas
potables tratadas que pueden ser o no
purificadas (destilación, nanofiltración, osmosis inversa
o cualquier otro método similar) y podrán ser
coloreadas, saborizadas,
carbonatadas, mineralizadas, y debiendo estar exentas de
edulcorantes naturales y/o artificiales.
| NOTA: El Art. segundo
del DTO 68, Salud, publicado el 23.01.2006, dispuso que la
modificación introducida al presente artículo rige a
contar de 180 días después de su publicación.
|
|
| DTO 68, SALUD
Art. primero Nº 33
D.O. 23.01.2006 |
|
Artículo 487 B.- Las aguas envasadas sin gas
deberán ser sometidas a procesos necesarios
para asegurar su calidad sanitaria, estos procesos pueden
ser: ozonificación, UV o cualquier otro que asegure
la inocuidad del producto
envasado.
| NOTA: El Art. segundo
del DTO 68, Salud, publicado el 23.01.2006, dispuso que la
modificación introducida al presente artículo rige a
contar de 180 días después de su publicación.
|
|
| DTO 68, SALUD
Art. primero Nº 33
D.O. 23.01.2006 |
|
Artículo 487 C.- Las aguas envasadas solo
podrán expenderse cuando contengan
electrolitos y deberán contener como mínimo 10 mg/l de
sólidos
totales.
| NOTA:
El Art. segundo del DTO 68, Salud, publicado el
23.01.2006, dispuso que la modificación introducida al
presente artículo rige a contar de 180 días después de su
publicación.
|
|
| DTO 68, SALUD
Art. primero Nº 33
D.O. 23.01.2006 |
|
Artículo 487 D.- A las aguas envasadas se les
podrán incorporar nutrientes, en
concentraciones según la normativa respectiva. Los
nutrientes incorporados a estas aguas no deberán estar
comprendidos en los programas
de Salud Pública, en este tipo de productos.
| NOTA: El Art. segundo
del DTO 68, Salud, publicado el 23.01.2006, dispuso que la
modificación introducida al presente artículo rige a
contar de 180 días después de su publicación.
|
|
| DTO 68, SALUD
Art. primero Nº 33
D.O. 23.01.2006 |
|
Artículo 487 E.- La rotulación de las aguas
envasadas deberá incluir, la composición y
concentración de las sales minerales o electrolitos, según
corresponda a su definición, la que será adicional a los
requisitos de rotulación
establecidos en el Título II Párrafo II del presente
Reglamento.
| NOTA: El Art. segundo
del DTO 68, Salud, publicado el 23.01.2006, dispuso que la
modificación introducida al presente artículo rige a
contar de 180 días después de su publicación.
|
|
| DTO 68, SALUD
Art. primero Nº 33
D.O. 23.01.2006 |
|
Artículo 487 F.- El anhídrido carbónico empleado en
la elaboración de aguas envasadas, debe
contener un mínimo de 98% de este gas y no más de 0,2% de
monóxido de carbono y estará exento de sustancias
extrañas que le confieran olor
y/o sabor desagradable o de cualquier otra naturaleza.
| NOTA: El Art. segundo
del DTO 68, Salud, publicado el 23.01.2006, dispuso que la
modificación introducida al presente artículo rige a
contar de 180 días después de su publicación.
|
|
| DTO 68, SALUD
Art. primero Nº 33
D.O. 23.01.2006 |
|
TITULO XXVIII
De los alimentos para regimenes especiales
|
|
Párrafo I
Disposiciones generales
|
|
Artículo 488.- Los alimentos para regímenes
especiales son aquellos elaborados o preparados,
especialmente, para satisfacer necesidades fisiológicas o
fisiopatológicas, particulares de nutrición.
Los productos regulados por este artículo deberán
formularse de acuerdo a principios médicos y nutricionales
aceptados, científicamente reconocidos o consensuados
internacionalmente y deberán satisfacer las necesidades
particulares de nutrición que indica el productor. Se
excluyen de esta categoría los alimentos de uso por vía
parenteral, los que serán regulados por el decreto supremo
Nº 1.876/05 del Ministerio de Salud.
|
| Decreto 24, SALUD
Art. 1 Nº 3
D.O. 24.11.2011 |
|
Artículo 489.- Los alimentos para
regímenes especiales, sin perjuicio del
cumplimiento de las normas generales de etiquetado del
presente reglamento, deberán indicar en la cara principal
del envase la(s) característica(s) esencial(es) o
modificación(es) realizada(s).
La información y rotulación nutricional de los
alimentos comprendidos en el párrafo II del presente
Título, deberán expresarse por cada 100 g o 100 ml, según
corresponda y por cada 100 kilocalorías (kcal) utilizables
del producto, opcional por cada porción del producto listo
para el consumo.
La información y rotulación nutricional de los
alimentos comprendidos en el párrafo III del presente
Título deberán expresarse por cada 100 g o 100 ml, según
corresponda, y por cada porción del producto listo para el
consumo, opcional por cada 100 kilocalorías (kcal)
utilizables del producto.
La información y rotulación nutricional de los
alimentos comprendidos en el párrafo V del presente Título
deberán expresarse por cada 100 g o 100 ml, según
corresponda, y por cada 100 kilocalorías (kcal) utilizables
del producto, opcional por cada porción del producto listo
para el consumo.
La información y rotulación nutricional de los
alimentos para uso médico o medicinal para mayores de 36
meses deberá dar cumplimiento a lo establecido en el
Título II del presente Reglamento.
|
| Decreto 24, SALUD
Art. 1 Nº 4
D.O. 24.11.2011 |
|
Artículo 490.- ELIMINADO
|
| Decreto 24, SALUD
Art. 1 Nº 5
D.O. 24.11.2011 |
|
Artículo 491.- ELIMINADO.
|
| Decreto 24, SALUD
Art. 1 Nº 5
D.O. 24.11.2011 |
|
Artículo 492.- ELIMINADO.
|
| Decreto 24, SALUD
Art. 1 Nº 5
D.O. 24.11.2011 |
|
Párrafo II
De las fórmulas para lactantes
|
|
Artículo 493.- Las fórmulas para lactantes
son aquellos productos que satisfacen los
requerimientos nutricionales de los lactantes, cuando la
alimentación con leche materna no es posible o es
insuficiente.
Se entiende por lactantes a los niños que tengan hasta
12 meses de edad.
La información y rotulación nutricional de estas
fórmulas deberán expresarse por cada 100g o 100ml, según
corresponda, y por cada 100 kilocalorías (kcal) utilizables
del producto, así como por 100 ml del producto listo para
el consumo, de acuerdo a las instrucciones indicadas por el
fabricante. Además, deberá declararse la cantidad total de
cada vitamina, mineral y cuando corresponda los
"ingredientes opcionales" referidos en el artículo 495.
|
| Decreto 13, SALUD
Art. 1 N° 1
D.O. 03.07.2019 |
|
Artículo 494.- Las fórmulas para lactantes se
clasifican en:
a) fórmula de inicio: es el producto líquido o
en polvo para reconstituir, especialmente fabricados para
satisfacer por sí solo las necesidades nutricionales de los
lactantes durante al menos los primeros seis meses de vida
en reemplazo de la leche materna, cuando no sea posible o
sea insuficiente la alimentación con ésta. Debe estar
fabricada a base de leche de vaca o de otros animales, o de
mezclas de la leche de éstos, o de otros ingredientes
autorizados por este reglamento.
b) fórmula de continuación: es aquella que forma parte
de un esquema de alimentación mixta destinada al consumo de
los lactantes de más de seis meses hasta los 12 meses de
edad.
c) fórmulas para lactantes con necesidades nutricionales
especiales, tales como, intolerancia a la lactosa, intolerancia al gluten,
fenilcetonuria u otros problemas metabólicos. Éstas
deberán indicar en el rótulo en forma clara y destacada la
necesidad especial para la que debe emplearse, las
propiedades específicas en que se basa y recomendaciones
concretas y advertencias en relación a su consumo, si fuese
necesario.
|
| Decreto 13, SALUD
Art. 1 N° 2
D.O. 03.07.2019 |
| Decreto 106,
SALUD
Art. 1 Nº 33
D.O. 23.04.2009 |
|
Artículo 495.- El producto debe haber sido
elaborado exclusivamente por medios físicos y
envasado de manera que se evite su alteración y
contaminación en cualquier condición normal de
manipulación, almacenamiento, distribución y venta.
Asimismo, deberá estar fabricada a base de leche de
vaca o de otros animales o de mezclas de leches de distintos
animales o de otros ingredientes sobre los cuales se haya
demostrado que son idóneos para la alimentación de los
lactantes. Deberá estar científicamente demostrada la
inocuidad, así como la idoneidad nutricional, para
favorecer el crecimiento y el desarrollo de los lactantes.
Estas fórmulas deberán ser libres de gluten.
La fórmula de inicio reconstituida deberá presentar
la siguiente composición:
a)
Energía mínimo máximo
60 kcal/100 ml 70 kcal/100
ml
b)
Proteínas mínimo máximo
1,8 g/100 kcal 3,0 g/100
kcal
Cuando las fórmulas a base de proteínas de la leche
no hidrolizadas, contengan menos de 2 g de proteínas/100
kcal y, cuando las fórmulas para lactantes a base de
proteínas hidrolizadas contengan menos de 2,25 g de
proteínas/100 kcal, deberán mantener los antecedentes de
las evaluaciones clínicas realizadas, disponibles para
cuando la autoridad sanitaria los requiera.
El valor mínimo de proteínas de 1,8 g/100kcal se
aplica a las proteínas de la leche de vaca o de otros
animales o mezcla de la leche de éstos. En las fórmulas a
base de aislados de proteínas de soya, en cambio, se aplica
un valor mínimo de 2,25 g/100 kcal.
El cálculo del contenido de proteínas de la fórmula
final preparada y lista para el consumo deberá basarse en N
x 6,25, salvo que se proporcione una justificación
científica para el uso de un factor de conversión
diferente aplicable a un determinado producto.
La fórmula debe contener una cantidad disponible de
cada aminoácido esencial y semiesencial igual, al menos, a
la que contiene la proteína de referencia, según se define
en la Tabla Nº 1 del presente artículo. No obstante, a
efectos de cálculo, las concentraciones de tirosina y
fenilalanina pueden sumarse. Las concentraciones de
metionina y cisteína pueden sumarse si la proporción es
inferior a 2:1; si la proporción se sitúa entre 2:1 y 3:1,
la idoneidad de la fórmula debe demostrarse por medio de
ensayos clínicos.
Podrán añadirse al preparado para lactantes
aminoácidos aislados únicamente a fin de mejorar su valor
nutritivo para los lactantes. Para mejorar la calidad de las
proteínas, podrán añadirse aminoácidos esenciales y
semiesenciales, pero sólo en las cantidades necesarias a
tal efecto. Sólo podrán utilizarse las formas L de los
aminoácidos.
Tabla Nº 1: Contenido de aminoácidos de la proteína
de referencia de la leche humana*
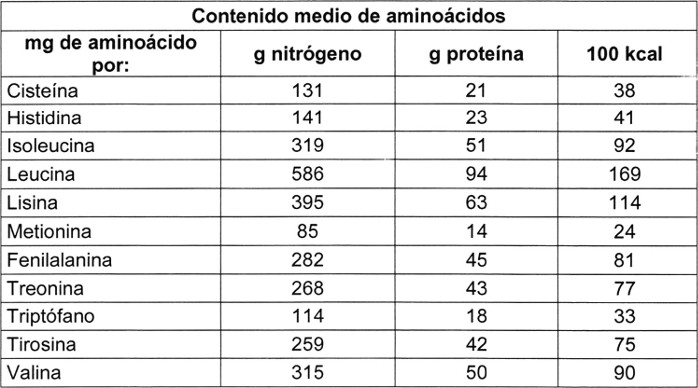
|
.
* Adaptado del Codex Stan 72, revisado en 2016.
c)
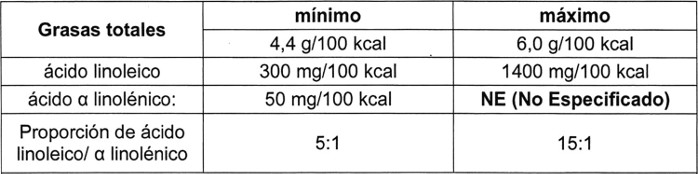
|
.
Se prohíbe la utilización de aceite de sésamo y
aceite de algodón.
Los ácidos láurico y mirístico en conjunto no
deberán superar el 20% del contenido total de ácidos
grasos.
Los ácidos grasos trans solamente serán de origen
lácteo. El contenido de ácidos grasos trans no deberá ser
superior al 3% del contenido total de ácidos grasos.
El contenido de ácido erúcico no deberá superar el
1% del contenido total de ácidos grasos.
El contenido total de fosfolípidos no deberá superar
los 300mg/100kcal.
No se podrán utilizar aceites o grasas hidrogenadas
comercialmente.
d)
mínimo
máximo
Carbohidratos disponibles 9 g/100 kcal 14 g/100
kcal
La lactosa y los polímeros de glucosa deberán ser los
carbohidratos preferentes para las fórmulas a base de
proteínas de la leche de vaca y de proteínas hidrolizadas.
Solo podrán añadirse almidones exentos de gluten
precocidos o gelatinizados hasta un máximo de 30% del
contenido total de carbohidratos y hasta un máximo de 2
g/100 ml de la fórmula reconstituida.
Deberá evitarse el uso de sacarosa y fructosa: La
sacarosa sólo se puede añadir a fórmulas para lactantes
con base en proteínas hidrolizadas. Si se añade, el
contenido de sacarosa no deberá exceder el 20% del
contenido total de hidratos de carbono. Este agregado
deberá señalarse en forma destacada en la cara principal
del envase.
e)
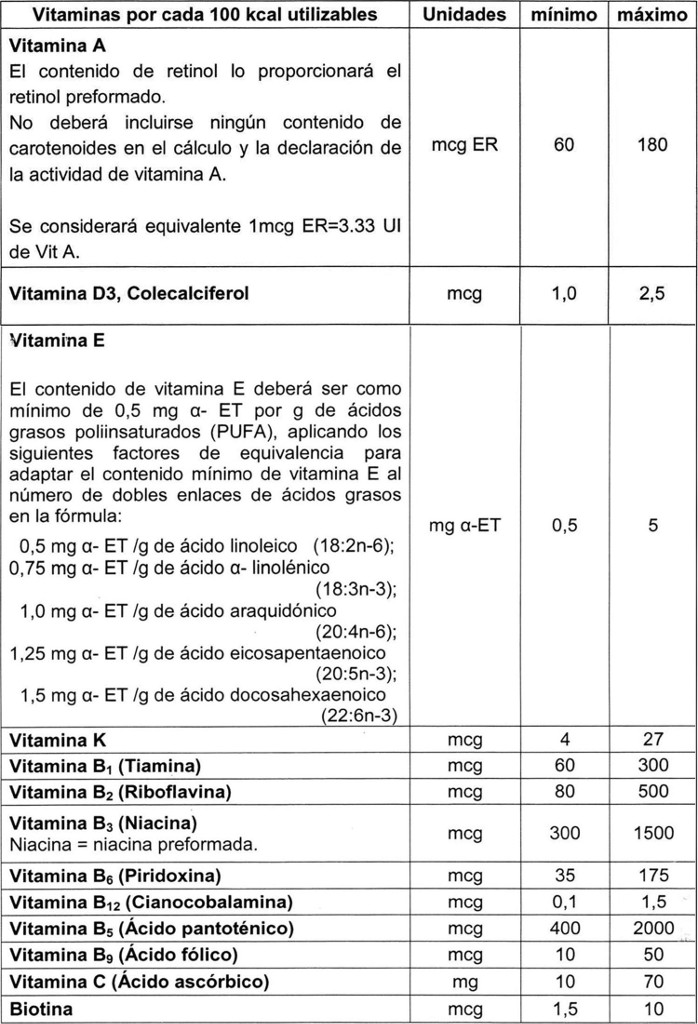
|
.
f)
.
.
g) Otras sustancias:
Deberán añadirse las sustancias que se indican a
continuación, en cuyo caso su contenido por 100 kcal en la
fórmula lista para el consumo deberá estar entre los
límites siguientes:
.
h) Ingredientes opcionales
Se podrán adicionar los siguientes ingredientes
opcionales de acuerdo a los límites de la siguiente tabla:
.
Podrán añadirse otras sustancias que normalmente
están presentes en la leche humana, para mejorar la calidad
nutricional de las fórmulas. La idoneidad e inocuidad de
estas sustancias deberán estar demostradas
científicamente. La fórmula deberá contener las
cantidades sobre la base de su presencia en la leche humana.
Podrán emplearse únicamente cultivos que produzcan
ácido láctico L (+).
i) Aditivos
Sólo se podrán usar los siguientes aditivos en las
cantidades señaladas:
.
.
.
|
| Decreto 13, SALUD
Art. 1 N° 3
D.O. 03.07.2019 |
|
Artículo 496.- La fórmula de
continuación reconstituida deberá presentar la
siguiente composición básica:
a) energía: mínimo 60 kcal/100 ml
máximo 85 kcal/100 ml
b) proteínas: mínimo 3 g/100 kcal
máximo 5,5 g/100 kcal
c) lípidos: mínimo 3,0 g/100 kcal
máximo 6,0 g/100 kcal
-ácido linoleico:
mínimo : 300 mg/100 kcal
máximo : 1400 mg/100Kcal.
- ácido α-linolénico
mínimo : 50 mg/100 kcal
máximo : N.E. (No Especificado)
Proporción de ácido linoleico/ α-linolénico
mínimo 5:1
máximo 15:1
Se prohíbe la utilización de aceite de sésamo y
aceite de algodón
Los ácidos láurico y mirístico en conjunto no
deberán superar el 20% del contenido total de ácidos
grasos.
El contenido de ácidos grasos trans no deberá ser
superior al 3% del contenido total de ácidos grasos.
El contenido de ácido erúcico no deberá superar el
1% del contenido total de ácidos grasos.
El contenido total de fosfolípidos no deberá superar
los 300 mg/100 kcal.
En los preparados para lactantes no se utilizarán
aceites y grasas hidrogenadas comercialmente
d) carbohidratos: mínimo 7 g/100 kcal.
máximo 14 g/100 kcal.
-Lactosa: mínimo 1,8 g/100 kcal.
-Sacarosa,
glucosa, fructosa,
miel: máximo 20% del contenido total
de carbohidratos por separado o
en conjunto.
e) sales minerales por cada 100 kcal
utilizables:
Mín. Máx.
Hierro (mg) 0,45 3
Sodio (mg) 20 60
Potasio (mg) 60 180
Cloro (mg) 50 160
Calcio (mg) 50 140
Fósforo (mg) 25 100
Magnesio (mg) 5 15
Zinc (mg) 0,5 1,5
Cobre (mcg) 35 120
Yodo (mcg) 10 60
Manganeso (mcg) 1 100
Selenio (mcg) 1 9
Mín. Máx.
Relación
calcio/fósforo 1:1 2:1
f) vitaminas por cada 100 kcal utilizables.
Mín. Máx.
Vitamina A
(mcg retinol) 75 225
Vitamina D
(mcg colecalciferol) 1 3
Tiamina (mcg) 40 300
Riboflavina (mcg) 60 500
Nicotinamida
(mcg niacina) 250 1500
Ácido pantoténico
(mcg) 300 2000
Vitamina B6 (mcg) 45 175
los preparados
deberán contener un
mínimo de 15 mcg de
vitamina B6/g de
proteína
Biotina (mcg) 1,5 10
Ácido fólico (mcg) 4 50
Vitamina B12 (mcg) 0,2 1,5
Vitamina C (mg) 8 70
Vitamina K (mcg) 4 27
Vitamina E
(mg-tocoferol) 0,5 5 mg/g de ácidos grasos
poliinsaturados
expresados como
ácido linoleico.
En ningún caso será
inferior a 0,5
mg/100 kcal
disponibles.
g) Otras sustancias: por cada 100 kcal.
Mín. Máx.
Mioinositol (mg) 4 40
L- carnitina (mg) 1,2 NE
h) Ingredientes facultativos
Min.
Máx.
h.1) Taurina (mg) por cada 100 kcal - 12
h.2) Ac. Docosahexaenoico (% total de lípidos) - 0,5
Cuando se use ácido Docosahexaenoico (DHA) (22:6-3) en
los preparados para lactantes, el contenido de ácido
araquidónico (20:4n-6) deberá alcanzar, por lo menos, la
misma concentración que el DHA.
Mín.
Máx.
h.3) Nucleótidos: mg/100 Kcal - 16
i) aditivos.
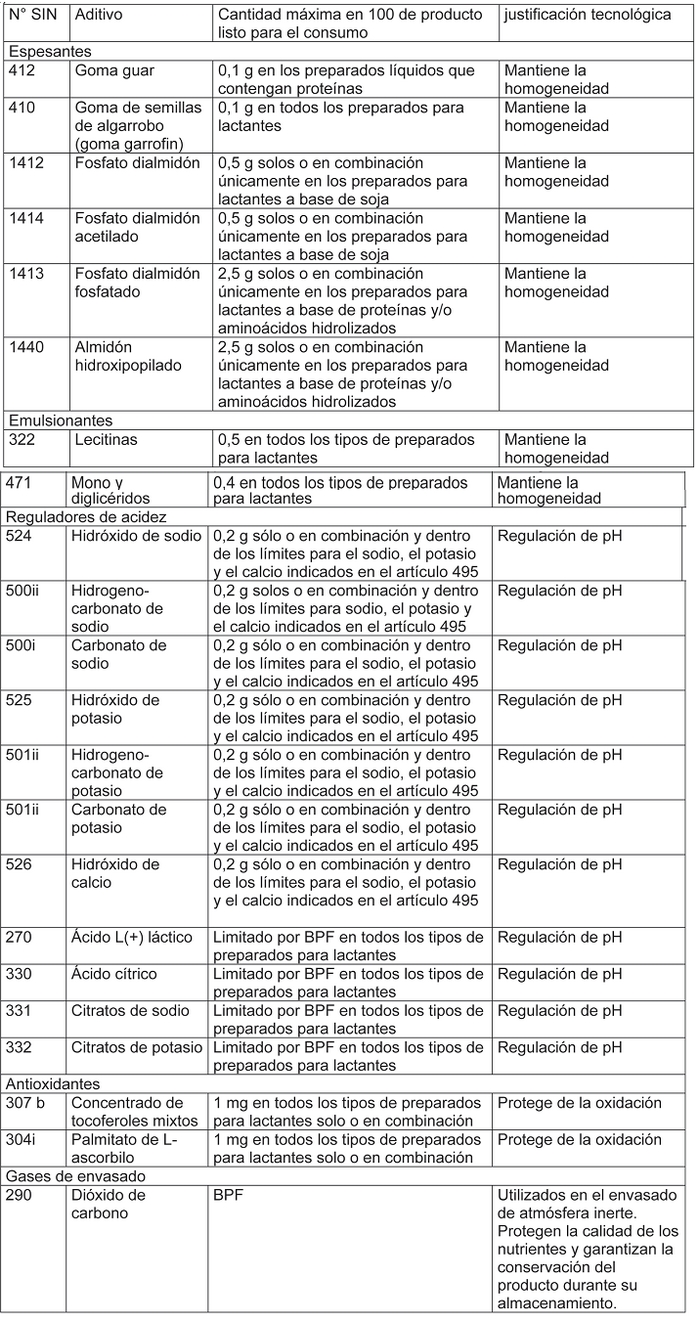
|
|
| Decreto 106, SALUD
Art. 1 Nº 35
D.O. 23.04.2009 |
| Decreto 117, SALUD
Art. 1 N° 1
D.O. 17.09.2014 |
| Decreto 24, SALUD
Art. 1 Nº 8
D.O. 24.11.2011 |
|
Artículo 497.- Además de lo dispuesto en el
presente reglamento para etiquetado general y
para regímenes especiales, en la rotulación y/o publicidad
de cualquier tipo de las fórmulas para lactantes sólo
podrá proveerse la siguiente información, la que, además,
tiene el carácter de obligatoria:
a) origen de las proteínas que contiene el producto. Si
el 90% de las proteínas como mínimo, procede de leche
deberá denominarse "Fórmula para lactantes a base de
leche"; si el producto no contiene leche ni ninguno de sus
derivados deberá indicarse "no contiene leche ni productos
lácteos".
b) rotulación del valor energético disponible (expresado
en kcal), contenido de proteínas, lípidos y carbohidratos
disponibles (expresados en gramos), los que deberán
expresarse según Artículo 491 del presente Reglamento.
c) rotulación de otros nutrientes opcionales, los que
deberán rotularse de acuerdo al Artículo 491 del presente
reglamento
d) los productos que contengan un mínimo de 1 mg de
hierro por 100 kcal utilizables deberán tener la
denominación "Fórmula con hierro para lactantes".
e) deberá indicarse en caracteres destacados que la
fórmula "NO SUSTITUYE A LA LECHE MATERNA".
f) En la rotulación y publicidad de las fórmulas para
lactantes queda totalmente prohibido el uso de los términos
"humanizada", "maternalizada" u otros similares y de
imágenes que puedan inducir a la indebida comparación con
la lactancia materna o a desalentar su práctica, como por
ejemplo, lactantes, mujeres, biberones, entre otros.
g) Asimismo la etiqueta de cada envase deberá contener un
mensaje claro, visible y fácilmente legible que incluya las
palabras "AVISO IMPORTANTE: LA LECHE MATERNA ES EL MEJOR
ALIMENTO PARA SU NIÑO/A" o una declaración equivalente que
exprese inequívocamente la superioridad de la leche materna
por sobre las fórmulas para lactantes.
h) Deberá advertirse la necesidad de combinar el alimento
para lactantes con alimentación complementaria adecuada al
desarrollo del menor, a partir de los 6 meses de edad.
i) el producto destinado a lactantes con necesidades
especiales de nutrición, deberá indicar la necesidad
especial para la que va a emplearse la fórmula y la
propiedad o las propiedades dietéticas en que se basa.
j) Deberá informarse que el producto debe ser usado
únicamente bajo indicación de un profesional de la salud.
k) Deberá rotularse, además, la fecha de elaboración y
la fecha de vencimiento e instrucciones sobre su correcta
preparación y uso, así como su almacenamiento y
conservación antes y después de abrir el envase.
|
| Decreto 106, SALUD
Art. 1 Nº 36
D.O. 23.04.2009 |
|
Artículo 497 bis.- Se prohíbe toda acción de
publicidad de fórmulas de inicio y fórmulas de
continuación hasta los 12 meses de edad, de las que trata
el presente párrafo, tales como:
- El ofrecimiento o entrega a título gratuito de
productos o muestras de éstos.
- La distribución de regalos o elementos publicitarios
con el producto o asociado a la venta del mismo.
- La realización de exhibiciones promocionales o
degustaciones.
- La realización de publicidad en medios de
comunicación u otros soportes.
- La utilización en el envase de imágenes o palabras
que correspondan a publicidad.
- La publicación de avisos, carteles o señaléticas
que destaquen ofertas como promociones o reducciones en el
precio, cupones de descuento, descuento en el precio según
la cantidad de productos adquiridos u otras estrategias
publicitarias similares.
El profesional que requiera indicar estas fórmulas
deberá garantizar que el usuario cuente con la información
necesaria para seleccionar adecuadamente la fórmula
respectiva, señalando en la prescripción solamente la
expresión "Fórmula de inicio" o "Fórmula de
continuación", sin indicar marcas comerciales específicas,
y la edad del niño o niña que la recibirá.
|
| Decreto 24
Art. 1 N° 2
D.O. 28.11.2017 |
|
Párrafo III
De las preparaciones comerciales de alimentos infantiles
|
|
Artículo 498.- Preparaciones comerciales de
alimentos infantiles son aquellas utilizadas
durante el período de destete y adaptación de los niños a
la alimentación sólida. Se preparan para ser administrados
directamente, o bien, deshidratados para ser reconstituidos.
|
| Decreto 13, SALUD
Art. 1 N° 4
D.O. 03.07.2019 |
|
Artículo 499.- Las preparaciones comerciales de
alimentos infantiles para administrarse directamente según
el tamaño de partículas se clasifican en:
a) colados : aquellas preparaciones de textura fina y
homogénea, que contiene partículas pequeñas, de tamaño
uniforme y que no requieren ni incitan a la masticación
antes de la deglución;
b) picados : aquellas preparaciones de partículas más
grandes y textura más gruesa, incluyendo trocitos de
alimentos que incitan a la masticación.
|
|
Artículo 500.- Los alimentos infantiles deshidratados,
una vez reconstituidos serán parecidos en cuanto a
consistencia y tamaño de sus partículas a los descritos en
a) y b) del artículo anterior.
|
|
Artículo 501.- Estos alimentos infantiles
deben contener sustancias inocuas y
adecuadas para la alimentación de los lactantes y niños
pequeños hasta los 36 meses de edad.
El producto y sus componentes no deberán haber sido
tratados con radiaciones ionizantes.
|
| Decreto 13, SALUD
Art. 1 N° 5
D.O. 03.07.2019 |
|
Artículo 502.- Estos alimentos deberán presentar
la siguiente composición:
a) Proteínas
El contenido de proteínas de los colados o picados
deberá ser el correspondiente a la declaración de
ingredientes en su rotulación, según las siguientes
condiciones:
a.1) Al menos 7g/100 kcal, cuando la carne, el pollo,
el pescado u otra fuente de proteínas de origen animal,
individualmente o en combinación, sean los únicos
ingredientes mencionados en la denominación del producto.
En estos productos, la carne, el pollo, el pescado u otra
fuente de proteínas de origen animal deberán constituir en
total, como mínimo tanto el 40% del peso total del
producto, como el 25% del peso total de las fuentes de
proteínas mencionadas.
a.2) Al menos 4g/100 kcal, cuando la carne, el pollo,
el pescado u otra fuente de proteínas de origen animal,
individualmente o en combinación, sean nombrados en primer
lugar en la denominación del producto. En estos productos,
la carne, el pollo, el pescado o la otra fuente de
proteínas deberán constituir en total, como mínimo tanto
el 10% del peso total del producto, como el 25% del peso
total de las fuentes de proteínas mencionadas.
a.3) Al menos 3g/100 kcal, cuando la carne, el pollo,
el pescado u otra fuente de proteínas de origen animal,
individualmente o en combinación, aparecen declarados,
aunque no en primer lugar, en la denominación del producto.
En estos productos, la carne, el pollo, el pescado o la otra
fuente de proteínas de origen animal deberán constituir en
total, como mínimo tanto el 8% del peso total del producto,
como el 25% del peso total de las fuentes de proteínas
mencionadas.
a.4) Al menos 3g/100 kcal, cuando no menciona la carne,
el pollo, el pescado u otra fuente de proteínas de origen
animal en la denominación del producto.
En los casos en que los productos contengan menos
proteínas que 3g/100 kcal, se considerarán bajos en
proteínas, y deberá rotular de manera destacada, en la
cara frontal del producto, una frase como se indica en la
letra c) del artículo 505 de este reglamento.
b) Materia grasa:
No deben utilizarse grasas y aceites parcialmente
hidrogenados.
c) Sodio: máximo 200 mg/100 g.
No se permitirá la adición de sal (NaCl) a los
productos de postre a base de frutas.
d) Vitaminas y minerales: podrán agregarse vitaminas y
minerales hasta los límites máximos establecidos en el
artículo 495 del presente reglamento.
e) Fibra dietética total: deberá ser la propia de los
alimentos naturales utilizados como ingredientes del
producto, y no deberá adicionarse fibra dietética con
ingredientes artificiales.
f) Carbohidratos disponibles: No deberán añadirse
mono o disacáridos.
|
| Decreto 13, SALUD
Art. 1 N° 6
D.O. 03.07.2019 |
|
Artículo 503.- Sólo se permitirá el uso de
los siguientes aditivos, en la cantidad
que se indica por 100 g o 100 ml del producto listo para el
consumo:
.
.
|
| Decreto 13, SALUD
Art. 1 N° 7
D.O. 03.07.2019 |
|
Artículo 504.- El producto deberá prepararse
con especial cuidado, mediante buenas
prácticas de fabricación, a fin de eliminar totalmente los
residuos de los plaguicidas que pueden necesitarse para la
producción, el almacenamiento o la elaboración de las
materias primas o del ingrediente alimentario acabado o, si
ello es técnicamente inevitable, reducirlos en la mayor
medida posible.
El producto no deberá contener residuos de hormonas ni
de antibióticos determinados mediante métodos convenidos
de análisis, y estará prácticamente exento de otros
contaminantes y otras sustancias dañinas para la salud,
especialmente, de sustancias farmacológicamente activas.
|
| Decreto 13, SALUD
Art. 1 N° 8
D.O. 03.07.2019 |
|
Artículo 505.- Además de lo dispuesto para
etiquetado general y para regímenes especiales,
las preparaciones comerciales de alimentos infantiles
deberán indicar en su etiqueta lo siguiente:
a) Su denominación de colado o picado, según las
definiciones de este reglamento.
b) Se debe indicar la edad a partir de la cual podrá
consumirse el producto, teniendo en cuenta su composición,
textura y otras propiedades particulares. La edad indicada
será, como mínimo, de seis meses para cualquier producto.
c) En los casos en que los productos contengan menos
proteínas que 3g/100 kcal deberá indicar claramente y
destacado en la cara frontal del envase la siguiente frase:
"NO REEMPLAZA UNA COMIDA COMPLETA PARA UN NIÑO".
d) En este tipo de productos, no deberán incorporarse
en los rótulos ni publicidad de los mismos, declaraciones
de propiedades saludables.
|
| Decreto 13, SALUD
Art. 1 N° 9
D.O. 03.07.2019 |
|
Artículo 505 bis.- La información y
rotulación nutricional de los alimentos
comprendidos en este párrafo deberán expresarse por cada
100 g o 100 ml, según corresponda, y por cada porción del
producto listo para el consumo. Además, opcionalmente,
podrá expresarse por cada 100 kilocalorías (kcal)
utilizables del producto
|
| Decreto 13, SALUD
Art. 1 N° 10
D.O. 03.07.2019 |
|
Párrafo IV
De los alimentos para uso infantil procesados a base de
cereales
|
|
Artículo 506.- Los alimentos para uso
infantil procesados a base de cereales son
aquellos destinados a completar el régimen alimentario
normal de niños desde los 6 meses hasta los 36 meses de
edad.
|
| Decreto 106, SALUD
Art. 1 Nº 40
D.O. 23.04.2009 |
|
Artículo 507.- Los alimentos elaborados a base
de cereales están preparados
principalmente con uno o más cereales molidos que se
procesan para lograr un escaso contenido de humedad y se
fragmentan para ser consumidos diluidos con agua, leche u
otro líquido conveniente o sin dilución como galletas,
bizcochos o pastas y se consumen de acuerdo a las
instrucciones que el fabricante debe indicar en el rótulo
del producto.
El contenido de cereales en el producto deberá
alcanzar por lo menos el 25 por ciento de la mezcla final en
relación con el peso en seco. De acuerdo a su preparación
se distinguen las siguientes categorías:
a) Productos que consisten en cereales que se preparan
para el consumo añadiendo leche u otros líquidos
nutritivos idóneos.
b) Cereales con adición de alimentos de alto valor
proteínico, que se preparan para el consumo con agua u
otros líquidos apropiados exentos de proteínas.
|
| Decreto 106, SALUD
Art. 1 Nº 41
D.O. 23.04.2009 |
|
Artículo 508.- Las categorías descritas en
artículo 507 se preparan principalmente con
uno o más productos molidos de cereales, como trigo, arroz,
cebada, avena, centeno, maíz o sorgo. También podrán
contener leguminosas previamente tratadas para eliminar
factores antinutricionales (según las buenas prácticas de
fabricación), raíces amiláceas como arroz o mandioca,
tallos amiláceos y semillas oleaginosas en menor
proporción.
|
| Decreto 106, SALUD
Art. 1 Nº 42
D.O. 23.04.2009 |
|
Artículo 509.- Los requisitos relativos al
contenido energético y de nutrientes se
refieren al producto listo para el consumo tal como se
vende, o preparado de conformidad con las instrucciones del
fabricante, a menos que se especifique otra cosa y deberán
ajustarse a lo siguiente:
Contenido energético
El contenido energético de los alimentos elaborados a base
de cereales no deberá ser inferior a 0,8 kcal/g.
Proteínas
En aquellos que se consumen de acuerdo a lo descrito en el
punto b) del art. 507, el índice químico de la proteína
añadida deberá ser equivalente por lo menos al 80 por
ciento de la calidad de la caseína. El contenido de
proteína no deberá ser inferior a 2 g/100 kcal ni superior
a 5,5 g/100 kcal.
Se permite la adición de aminoácidos sólo con el fin de
mejorar el valor nutricional de la mezcla proteínica y en
las proporciones necesarias para tal fin. Podrán emplearse
únicamente formas naturales de L-aminoácidos.
Lípidos
Para los productos mencionados en punto b) del artículo
507, el contenido de lípidos no deberá ser superior a 4,5
g/100 kcal. Sin embargo, si el contenido de lípidos es
superior a 3,3 g/100 kcal:
- la cantidad de ácido linoleico (en forma de
triglicéridos = linoleatos) no deberá ser inferior a 300
mg/100 kcal. ni superior a 1200 mg/100 kcal.
- la cantidad de ácido láurico no deberá exceder del 15%
del contenido lipídico total;
- la cantidad de ácido mirístico no deberá exceder del
15% del contenido lipídico total.
Las categorías de productos a que se refiere la letra a)
del artículo 507 no deberán exceder de un contenido
máximo de lípidos de 3,3 g/100 kcal.
Hidratos de Carbono
Si a los productos mencionados en el punto a) artículo 507
se añade sacarosa, fructosa, glucosa, jarabe de glucosa o
miel:
- la cantidad de carbohidratos añadidos procedentes de
estas fuentes no deberá ser superior a 7,5 g/100 kcal
- la cantidad de fructosa añadida no deberá ser superior a
3,75 g/100 kcal.
Si a los productos mencionados en el punto b) del artículo
507 se añade sacarosa, fructosa, glucosa, jarabe de glucosa
o miel:
- la cantidad de carbohidratos añadidos procedentes de
estas fuentes no deberá ser superior a 5 g/100 kcal.
- la cantidad de fructosa añadida no deberá ser superior a
2,5 g/100 kcal.
Minerales
- El contenido de calcio de los productos mencionados en el
punto b) del artículo 507 no deberá ser inferior a 80
mg/100 kcal.
- El contenido de sodio de los productos descritos en el
artículo 507 podrá ser como máximo de 100 mg/100 Kcal del
producto listo para el consumo.
Vitaminas
La cantidad de vitamina B1 (tiamina) no deberá ser inferior
a 50 mcg/100 kcal.
En lo que respecta a los productos mencionados en punto
b) del artículo 507 la cantidad de vitamina A y de vitamina
D deberá mantenerse dentro de los límites siguientes:
Vitamina
mcg/100 kcl
Vitamina A (en mcg de 60 - 180
retinol equivalente)
Vitamina D 1 - 3
Los productos señalados en el punto a) del artículo 507 a
los que se adicione vitamina A o vitamina D deberán cumplir
con los límites de esas vitaminas descritos para los
productos mencionados en la letra f) del artículo 496.
Las vitaminas y minerales no mencionados en el presente
artículo podrán ser agregadas de acuerdo a los límites
establecidos en el artículo 496 del presente reglamento.
Humedad
El contenido de humedad de los productos deberá ser
conforme a las buenas prácticas de fabricación para cada
una de las categorías de productos, y su cuantía deberá
ser tal que se reduzca al mínimo la pérdida de valor
nutritivo y no pueda haber multiplicación de
microorganismos.
|
| Decreto 106, SALUD
Art. 1 Nº 43
D.O. 23.04.2009 |
|
Artículo 510.- Tanto el producto como sus
componentes no deberán haberse tratado con
radiaciones ionizantes.
Queda prohibido el uso de grasas hidrogenadas y
parcialmente hidrogenadas en estos productos.
El contenido máximo de fibra dietaria total será de
2g/100g de producto listo para el consumo conforme a las
instrucciones sugeridas por el fabricante.
|
| Decreto 106, SALUD
Art. 1 Nº 44
D.O. 23.04.2009 |
|
Artículo 511.- Todos los ingredientes, incluso
los facultativos, deberán estar limpios
y ser inocuos, apropiados y de buena calidad.
Todos los procedimientos de elaboración y desecación
deberán llevarse a cabo de forma que sean mínimas las
pérdidas del valor nutritivo, especialmente en la calidad
de sus proteínas.
Los productos que contengan miel o jarabe de arce
deberán tratarse de manera que se destruyan las esporas de
Clostridium botulinum, si las hubiere.
Sólo podrán utilizarse cultivos productores de ácido
láctico.
|
| Decreto 106, SALUD
Art. 1 Nº 45
D.O. 23.04.2009 |
|
Artículo 512.- Sólo se permitirá el uso de
los siguientes aditivos y en las
cantidades indicadas por cada 100 g de producto listo para
el consumo, preparado conforme a las instrucciones del
fabricante, salvo indicación contraria de su médico.
|
| Decreto 106, SALUD
Art. 1 Nº 46
D.O. 23.04.2009 |
|
Artículo 513.- Además de lo dispuesto para
etiquetado general y para regímenes especiales
en el artículo 491 en la etiqueta de estos alimentos se
indicará lo siguiente:
- la frase "para niños mayores de seis meses";
- Instrucci�nes sobre su preparación y uso, así como de su
almacenamiento y conservación;
- Cuando el producto no haya sido fabricado para ser
preparado acorde a lo descrito en el punto b) del artículo
507, deberá indicar el uso de leche para diluirlo o
mezclarlo.
- Si el producto contiene cacao se indicará "Para niños
mayores de 12 meses de edad".
Los productos contenidos en este párrafo no son
sustitutos de la leche materna y no deberán presentarse
como tales ni podrán declarar propiedades saludables.
|
| Decreto 106, SALUD
Art. 1 Nº 47
D.O. 23.04.2009 |
|
Párrafo V
De los alimentos para uso médico o medicinal
|
| Decreto 24, SALUD
Art. 1 Nº 10
D.O. 24.11.2011 |
|
Artículo 514.- Un alimento de uso médico o
medicinal es una categoría de alimentos para
regímenes especiales, formulados, elaborados y presentados
especialmente para el tratamiento dietético exclusivo o
parcial de pacientes, y que deberán utilizarse bajo la
supervisión de un profesional de la salud.
Estos alimentos deberán rotular:
- que el producto debe utilizarse bajo supervisión
médica o de un profesional de la salud,
- si el producto es o no adecuado para ser consumido como
única fuente de alimento,
- si el producto va destinado a un grupo de edad
específico, y
- si el producto puede perjudicar la salud de las
personas que lo consuman sin estar afectados por alguna de
las enfermedades, trastornos o afecciones, para los que vaya
destinado.
|
| Decreto 24, SALUD
Art. 1 Nº 10
D.O. 24.11.2011 |
|
Artículo 515.- Estos alimentos se clasificarán
de acuerdo a las instrucciones del
fabricante en:
a) Alimentos completos con una formulación de nutrientes
específica adaptada para determinadas enfermedades,
trastornos o situaciones fisiológicas. Pueden constituir la
única fuente de alimentos para las personas a las que van
destinados. Estos alimentos también pueden utilizarse como
sustitutos de una parte del régimen alimentario.
b) Alimentos incompletos con una formulación de
nutrientes específica adaptada para determinadas
enfermedades, trastornos o afecciones. No son adecuados como
única fuente de alimentos, por lo que sólo pueden
utilizarse como sustitutos de una parte del régimen
alimentario.
Esta información deberá quedar, claramente, indicada
en el rótulo para contribuir al uso adecuado del producto.
|
| Decreto 24, SALUD
Art. 1 Nº 10
D.O. 24.11.2011 |
|
Párrafo VI
De los alimentos para regímenes exentos de gluten
|
|
Artículo 516.- Un alimento libre de gluten es
aquel que está preparado únicamente con
ingredientes que por su origen natural y por la aplicación
de buenas prácticas de fabricación - que impidan la
contaminación cruzada - no contiene prolaminas procedentes
de trigo, de todas las especies de triticum como la escaña
común (Triticum spelta L.), el kamut (Triticum polonicum
L.), trigo duro, centeno, cebada, ni sus variedades
cruzadas, así como también de la avena.
Para efectos de la inclusión en el rótulo de la
leyenda "Libre de Gluten", los elaboradores de alimentos
libres de gluten deberán cumplir con las exigencias
establecidas en el presente Reglamento, así como contar con
un programa de buenas prácticas de fabricación, con el fin
de asegurar la no contaminación con los derivados de trigo,
centeno, cebada y avena en los procesos, desde la recepción
de las materias primas hasta la comercialización del
producto final.
|
| Decreto 106, SALUD
Art. 1 Nº 48
D.O. 23.04.2009 |
|
Artículo 517.- Las harinas libres de gluten
destinadas a la panificación, así como el pan
libre de gluten, deberán contener las vitaminas y minerales
establecidas en el artículo 350 de este Reglamento. Todos
los alimentos libres de gluten deberán etiquetarse
nutricionalmente de acuerdo a lo establecido en el
etiquetado general y en el artículo correspondiente de este
Reglamento.
|
| Decreto 106, SALUD
Art. 1 Nº 49
D.O. 23.04.2009 |
|
Artículo 518.- El término "Libre de gluten" y el
logo o símbolo de la espiga tachada,
sólo podrán utilizarse cuando el resultado del análisis
de laboratorio del producto alimenticio no sobrepase los 5
miligramos de gluten, de los cereales establecidos en el
artículo 516, por kilogramo del producto listo para su
entrega al consumidor final, de acuerdo a las técnicas
analíticas que, para estos efectos, determine el Instituto
de Salud Pública de Chile. La expresión "Libre de gluten"
se rotulará en las proximidades del nombre del producto,
con caracteres de buen realce, tamaño y visibilidad.
|
| Decreto 10, SALUD
Art. 1 N° 1
D.O. 24.07.2018 |
|
Párrafo VII
De los alimentos para regímenes de control de peso
|
|
Artículo 519.- Se entiende por alimentos para regímenes de control de peso,
aquellos que según las instrucciones correspondientes
sustituyen la totalidad de la dieta o una parte de la misma.
En el rótulo junto al nombre principal del
alimento, formando parte del mismo o junto a la
información nutricional deberá señalarse, con caracteres
fáciles de leer en circunstancias normales de compra
y uso la frase "alimento para
control de peso".
| NOTA:
El artículo transitorio del DTO 115, Salud, publicado el
25.11.2003, dispone que la modificaciones a este artículo,
regirán 180 días después de su publicación.
|
|
| DTO
475, SALUD
Art. Unico, N° 151
D.O. 13.01.2000 |
| DTO 115, SALUD
Art. primero Nº 25
D.O. 25.11.2003 |
|
Artículo 520.- Un producto que se presente
como sustituto de todas las comidas de la
dieta diaria deberá aportar como mínimo 800 kcal. y como
máximo 1.200 kcal.
Cuando el producto total se presente dividido en
porciones, 3 o 4 diarias, según los hábitos alimenticios
de la persona, estas porciones deberán suministrar
aproximadamente una tercera o una cuarta parte del aporte
energético total del producto, respectivamente.
|
| DTO 475, SALUD
Art. Unico, N° 1
D.O. 13.01.2000 |
|
Artículo 521.- Si el producto se presenta
como sustituto de una o más comidas de la
dieta diaria deberá aportar como mínimo 200 kcal y como
máximo 400 kcal. por comida, esto referido al producto tal
como se comercializa.
|
| DTO 475, SALUD
Art. Unico, N° 1
D.O. 13.01.2000 |
| Decreto 24, SALUD
Art. 1 Nº 11
D.O. 24.11.2011 |
|
Artículo 522.- Los sustitutos de comidas para
regímenes de control de peso se prepararán con elementos
constituyentes de proteínas de origen animal y vegetal que
se hayan demostrado aptos para el consumo humano, y con
otros ingredientes apropiados para obtener la composición
esencial del producto.
|
|
Artículo 523.- El contenido de proteínas de estos
productos será de un 25% como mínimo y un 50% como máximo
de la energía disponible del alimento listo para su
consumo.
La ingesta total diaria de proteínas no será superior
a 125 g. La calidad biológica de las proteínas no será
menor a un 80% de las proteínas del huevo o de la leche.
Para mejorar la calidad de las proteínas podrán añadirse
aminoácidos esenciales pero sólo en las cantidades
necesarias para tal efecto. Los aminoácidos utilizados
deberán presentarse en su forma levógira, pero se podrá
utilizar DL-metionina.
|
|
Artículo 524.- Estos alimentos deberán cumplir con
el descriptor bajo en grasa y no
deberán aportar, en forma de grasa total, más del 30% de
la energía disponible en el alimento. No menos del 3% de la
energía disponible deberá ser aportada como ácido
linoleico.
|
| Decreto 24, SALUD
Art. 1 Nº 12
D.O. 24.11.2011 |
|
Artículo 525.- Cuando un alimento se presente
como sustitutivo de todas las comidas de
un día, deberá contener, al menos, el 100% de las
cantidades de vitaminas y minerales especificadas a
continuación, en el producto tal como se comercializa:
Vitamina A 600 mcg EAR
Vitamina D 2,5 mcg D 3
Vitamina E 10 mg ET
Vitamina C 60 mg
Tiamina 0,8 mg
Riboflavina 1,2 mg
Niacina 11 mg
Vitamina B 6 2 mg
Vitamina B 12 1 mcg
Folato 200 mcg EFA
Calcio 500 mg
Fósforo 500 mg
Hierro 14 mg
Yodo 140 mcg
Magnesio 300 mg
Cobre 1,5 mg
Zinc 6 mg
Potasio 1,6 g
Sodio 0,6 g
Estos alimentos que se presenten como sustitutivo de
todas las comidas de un día deberán contener un mínimo de
13 g de fibra dietética total. Las cantidades por cada
tiempo de comida, deberán ajustarse a una cantidad que
corresponda al 33% o 25% del total señalado, según si el
número de porciones recomendadas por día es de 3 o 4,
respectivamente, lo que corresponde a 4,3 g o 3,3 g de fibra
dietética/porción, según si son 3 o 4 porciones por día.
Se podrán incluir otros nutrientes esenciales no
especificados en esta lista para los que exista Dosis Diaria
Remendada o Valores de Referencia Diaria, la sumatoria o
concentración final de ellos en el producto, no deberá ser
superior al 100% de la Dosis Diaria de Referencia
establecida para el nutriente en particular.
|
| Decreto 24, SALUD
Art. 1 Nº 13
D.O. 24.11.2011 |
|
Artículo 526.- Cuando un producto se presente
como sustituto de una sola comida de la
dieta diaria, es decir como reemplazo de una de las
principales comidas del día, desayuno, almuerzo, once o
cena, las cantidades de vitaminas y minerales deberán
ajustarse a una cifra que corresponda al 33% ó
|
| Decreto 106, SALUD
Art. 1 Nº 51
D.O. 23.04.2009 |
|
Artículo 527.- Estos productos se etiquetarán
conforme las disposiciones relativas a
etiquetado general y según lo dispuesto en el artículo
491. Si en las instrucciones para el uso se indica que el
producto debe combinarse con otros ingredientes, en la
etiqueta deberá agregarse la declaración del valor
nutritivo por porción de consumo habitual del resultado
final de la combinación.
En lo particular, en la etiqueta o etiquetado no se
deberá hacer referencia al ritmo ni a la magnitud de la
pérdida de peso resultante del consumo del alimento, como
tampoco a la disminución de la sensación de hambre ni al
aumento de la sensación de saciedad.
|
| DTO 475, SALUD
Art. Unico, N° 154
D.O. 13.01.2000 |
|
Artículo 528.- En la etiqueta o en el etiquetado
deberá hacerse referencia a la necesidad de mantener una
ingesta adecuada de líquido cuando se utilizan preparados
para el control de peso. Si el consumo de alimentos
proporciona una ingesta diaria de alcoholes de azúcar
superior a los 20 g diarios, la etiqueta deberá llevar una
declaración de que el alimento podría tener un efecto
laxante. La etiqueta deberá llevar una declaración de que
el alimento puede ser útil para el control de peso
únicamente como parte de una dieta con un contenido
energético controlado. La etiqueta de los productos que se
presentan como sustitutos de la dieta total para utilizar
durante más de seis semanas, deberá contener una
recomendación de que transcurrido ese período deberá
solicitarse asesoría médica.
|
| DTO 475, SALUD
Art. Unico, N° 155
D.O. 13.01.2000 |
|
Párrafo VIII De los alimentos con bajo contenido
de grasas y/o calorías.- DEROGADO
|
| Decreto 24, SALUD
Art. 1 Nº 14
D.O. 24.11.2011 |
|
Art�culo 529°.- DEROGADO
|
| Decreto 24, SALUD
Art. 1 Nº 14
D.O. 24.11.2011 |
|
Art�culo 530°.- DEROGADO
|
| Decreto 24, SALUD
Art. 1 Nº 14
D.O. 24.11.2011 |
|
Art�culo 531°.- DEROGADO
|
| Decreto 24, SALUD
Art. 1 Nº 14
D.O. 24.11.2011 |
|
Art�culo 532°.- DEROGADO
|
| Decreto 24, SALUD
Art. 1 Nº 14
D.O. 24.11.2011 |
|
Art�culo 533°.- DEROGADO
|
| Decreto 24, SALUD
Art. 1 Nº 14
D.O. 24.11.2011 |
|
TÍTULO XXIX
DE LOS SUPLEMENTOS ALIMENTARIOS Y DE LOS ALIMENTOS
PARA DEPORTISTAS
|
| DTO 253, SALUD
Nº 1 A) y B)
D.O. 20.01.2003 |
|
Párrafo I
De los Suplementos Alimentarios
|
| DTO 253, SALUD
Nº 1 A) y B)
D.O. 20.01.2003 |
|
Artículo 534.- Suplementos alimentarios son aquellos
productos elaborados o preparados especialmente para
suplementar la dieta con fines saludables y contribuir a
mantener o proteger estados fisiológicos característicos
tales como adolescencia, adultez o vejez.
Su composición podrá corresponder a un nutriente,
mezcla de nutrientes y otros componentes presentes
naturalmente en los alimentos, incluyendo compuestos tales
como vitaminas, minerales, aminoácidos, lípidos, fibra
dietética o sus fracciones.
Se podrán expender en diferentes formas de liberación
convencional, tales como polvos, líquidos, granulados,
grageas, comprimidos, tabletas, cápsulas u otras propias de
los medicamentos.
| NOTA:
El Art. transitorio del DTO 253, Salud, publicado el
20.01.2003, dispuso que la presente modificación entrará
en vigencia 30 días después de su publicación en el
Diario Oficial.
|
|
|
Artículo 535.- Los ingredientes dietarios
para suplementos alimentarios, que son las
substancias utilizadas intencionalmente para suplementar la
dieta humana, incrementando la ingesta diaria total de
vitaminas, minerales, aminoácidos, lípidos, fibra
dietética u otros elementos naturalmente presentes en los
alimentos, deberán cumplir con la identidad y pureza
indicada en las especificaciones de calidad e inocuidad.
|
| DTO 287, SALUD
Art. 2º
D.O. 18.02.2002 |
|
Artículo 536.- La declaración de propiedades saludables y nutricionales, y la
información nutricional complementaria que se describa en
los envases de estos productos, deberá ceñirse a las
normas establecidas para estos fines en este reglamento,
siendo prohibido promocionar su consumo para fines de
diagnóstico, prevención o tratamiento de las
enfermedades.
| NOTA:
El artículo transitorio del DTO 57, Salud, publicado el
06.05.2005, dispone que las modificaciones a la presente
norma entrarán en vigencia dieciocho meses después de su
publicación.
|
|
| DTO
287, SALUD
Art. 2º
D.O. 18.02.2002 |
| DTO 57, SALUD
Art. único Nº 13
D.O. 06.05.2005 |
|
Artículo 537.- La publicidad, a través de
cualquier medio, así como la rotulación de
los suplementos alimentarios, deberá adecuarse a las normas
que sobre el particular se contemplan en este reglamento;
adicionalmente, estos productos deberán señalar en su
etiquetado, en forma destacada en la cara principal del
envase y a continuación del nombre del producto, su
clasificación de "suplemento alimentario".
Todos los suplementos alimentarios deberán incluir,
inmediatamente por debajo de la rotulación como "Suplemento
Alimentario", una leyenda que señale: "Su uso no es
recomendable para consumo por menores de 8 años,
embarazadas y nodrizas, salvo indicación profesional
competente y no reemplaza a una alimentación balanceada".
|
| DTO 287, SALUD
Art. 2º
D.O. 18.02.2002 |
|
Artículo 538.- Los niveles, máximo y mínimo,
de vitaminas, minerales y demás
componentes a que alude el artículo 534, serán
establecidos por resolución del Ministerio de Salud,
dictada en uso de sus atribuciones legales técnico
normativas.
|
| DTO 287, SALUD
Art. 2º
D.O. 18.02.2002 |
|
Párrafo II, De los Alimentos para Deportistas
|
| DTO 253, SALUD
Nº 1 D)
D.O. 20.01.2003 |
|
Artículo 539.- Alimentos para deportistas son
aquellos productos alimentarios
formulados para satisfacer requerimientos de individuos
sanos, en especial de aquellos que realicen ejercicios
físicos pesados y prolongados.
Estos alimentos estarán compuestos por un ingrediente
alimentario o mezcla de éstos. Se les podrá adicionar uno
o más nutrientes, como hidratos de carbono, proteínas,
vitaminas, minerales y otros componentes presentes
naturalmente en los alimentos, tales como cafeína o
aquellos expresamente autorizados en el presente Reglamento.
En su elaboración se deberán cumplir las normas de las
buenas prácticas de manufactura.
En ellos no se podrá incorporar, solos ni en
asociación, hormonas o compuestos con efecto anabolizante.
Tampoco se les podrá incorporar sustancias con acción
estimulante sobre el sistema nervioso, salvo aquellas que
estén expresamente autorizadas y dentro de los límites
permitidos para este tipo de alimentos en este
Reglamento.
| NOTA: El
Art. transitorio del DTO 253, Salud, publicado el
20.01.2003, dispuso que la presente modificación entrará
en vigencia 30 días después de su publicación en el
Diario Oficial.
|
|
|
Artículo 540.- Sólo podrán considerarse alimentos
para deportistas aquellos que cumplan con los requisitos de
alguna de las propiedades nutricionales que se indican a
continuación. Ellos deberán colocar en la etiqueta, en el panel principal del
envase, con letras fácilmente legibles en color
contrastante con el fondo de la etiqueta: "ALIMENTO PARA
DEPORTISTAS ......." con el
descriptor que se indica entre comillas, según corresponda:
a) "Alto en energía". Aquellos alimentos que tienen por
porción de consumo habitual un 30%, o más, de la dosis
diaria de referencia (DDR) de energía (DDR =
2000 Kcal/día).
b) "Buena fuente de energía". Alimentos que tienen por
porción de consumo habitual entre un 20% y un 29% de la
dosis diaria de referencia de energía.
c) "Alto en hidratos de carbono disponibles".
Alimentos que tienen por porción de consumo habitual
un 30%, o más, de la dosis diaria de referencia de
carbohidratos disponibles (DDR = 350 g de carbohidratos
disponibles/día).
d) "Buena fuente de hidratos de carbono disponibles".
Alimentos que tienen por porción de consumo habitual
entre un 20% y un 29% de la dosis diaria de referencia de
carbohidratos disponibles.
e) "Alto en proteínas". Alimentos que tienen por porción
de consumo habitual de referencia un 40%, o más, de la
dosis diaria de referencia de proteínas equivalente a una
óptima calidad y digestibilidad (DDR = 50 g de proteínas).
f) "Buena fuente de proteínas". Alimentos que tienen por
porción de consumo habitual entre un 20% y un 39% de la DDR
de proteínas equivalente a una óptima calidad y
digestibilidad.
g) "Con adición de aminoácidos". A estos alimentos se
les podrá adicionar los aminoácidos que a continuación se
indican, hasta las cantidades máximas por día que se
señalan. En la recomendación de consumo de la etiqueta no
se podrá sobrepasar las cantidades máximas por día que se
indican en cada caso.
Aminoácido Cantidad máxima por día
mg
Alanina 4800
Arginina 4400
Acido aspártico 2400
Cisteína 1800
Glutamina 5600
Acido glutámico 6400
Glicina 6000
Histidina 1700
Isoleucina 1400
Leucina 1900
Lisina 1700
Metionina 720
Ornitina 1400
Fenilalanina 1900
Prolina 4400
Serina 5600
Taurina 1500
Treonina 1000
Tirosina 1600
Triptofano 100
Valina 1400
Los alimentos que tengan fenilalanina deberán incluir
en la etiqueta el siguiente mensaje:
"Fenilcetonúricos: contiene fenilalanina". Los alimentos
cuyo contenido de taurina sea igual o superior a 500 mg por
porción de consumo deberán incluir en la etiqueta el
siguiente mensaje: "No recomendable para diabéticos".
h) "Con adición de electrolitos". Los alimentos que se presentan como bebidas
no alcohólicas o preparaciones a reconstituir podrán
contener electrolitos como sodio y/o potasio.
El contenido de sodio deberá
ser igual o mayor a 10 mmol/l (230 mg Na+/l), el contenido
de potasio deberá ser igual o mayor a 2 mmol/l (78 mg
K+/l). Estas bebidas podrán ser isotónicas o hipotónicas
y deberán ser formuladas para tener una osmolalidad mínima
de 200 mosm/kg de agua y máxima de 340 mosm/kg de agua. Las
bebidas que presenten una osmolalidad entre 200 y 250
mosm/kg de agua podrán denominarse: "hipotónicas" y
aquellas que presenten una osmolalidad entre 250 y 340
mosm/kg de agua, podrán denominarse: "isotónicas".
La recomendación de consumo de los "Alimentos para
Deportistas" que se rotule, adjunte o relacione con el
producto no podrá sobrepasar, por día, las cantidades de
sodio y potasio, que se indican a continuación:
Electrolito Cantidad máxima por día
mmol mg
Sodio 70 1610
Potasio 95 3715
i) "Con adición de vitaminas y/o minerales". Si se
adicionan vitaminas y/o minerales, estos productos
alimenticios deberán clasificarse según corresponda como
"Alimento Fortificado" o "Suplemento Alimentario",
respetando los límites establecidos para cada nutriente en
cada categoría.
Cuando un "Alimento para Deportistas" califique además
como "Suplemento Alimentario" deberá dar cumplimiento a los
artículos correspondientes de este Reglamento,
especialmente, pero no sólo, a lo establecido en el
Párrafo I del Título XXIX.
j) Con cafeína. La cafeína podrá ser incorporada en
forma pura o por adición de uno o más ingredientes
alimentarios que la contengan. De los cuales sólo se
podrán utilizar los siguientes ingredientes:
café (Coffea spp.), té verde o té negro (Camellia
sinensis o Thea sinensis), cacao (Theobroma cacao), yerba
mate (Ilex brasillensis e Ilex paraguariensis), nuez de cola
(Kola spp.) y guaraná (Paullinia cupana), como tales o en
forma de extractos. La recomendación de consumo en la
etiqueta y/o publicidad no podrá sobrepasar los 500 mg. de
cafeína por día.
k) Con adición de otros compuestos. A los alimentos para
deportistas se les podrá incorporar los ingredientes
alimentarios que a continuación se indican pudiendo
contener las cantidades máximas por porción de consumo
habitual que se establecen.
La recomendación de consumo que se rotule, adjunte o
relacione con el producto no podrá sobrepasar, por día,
las cantidades máximas que se indican en cada caso. En
estos alimentos se deberá usar el descritpor: "Con
................", indicando el nombre del ingrediente,
según corresponda, así por ejemplo si tiene adición de
L-carnitina y colina, se deberá utilizar el descriptor:
"Con L-carnitina y colina"
Ingrediente alimentario Cantidad máxima
por día
L - carnitina 2 g
Inosina 10 mg
Ubiquinona 15 mg
Creatina 5 g
Delta-gluconolactona o 600 mg
Glucono-delta-lactona
l) Con hierbas: Se podrá incorporar como ingredientes
alimentarios las hierbas, y/o extractos de las hierbas que a
continuación se indican, en las cantidades máximas por
porción de consumo habitual que se establecen. La
recomendación de consumo de los "Alimentos para
Deportistas" que se rotule, adjunte o relacione con el
producto no podrá sobrepasar las cantidades máximas por
día que se indican en cada caso.
Ingrediente alimentario Cantidad máxima
por día
Raíz de Panax Ginseng C.A. Meyer
(Ginseng Coreano, Ginseng
Asiático o Ginseng Oriental)
1,0 g de raíz
Fruto de Schizandra Chinesis
(Turcz.)
Baill. (Chisandra) 1,5 g de fruto
Raíz y risoma de Eleuterococcus
Senticosus Rupr. et Maxim.
(Ginseng Siberiano) 2,0 g de raíz y
rizoma
Si estos ingredientes se incorporan en forma de
extractos, éstos deberán ser apropiados para uso en
alimentos y su concentración máxima deberá ser calculada
considerando la equivalencia del contenido especificado en
cada una de las formas incluidas en esta tabla.
En los alimentos que contengan una o más de estas
hierbas, el contenido máximo de cafeína en el producto
listo para el consumo será de 54 mg. por porción de
consumo habitual y no más de 180 mg. de cafeína/litro en
los alimentos que se consumen líquidos y de 90 mg/100 g. en
los que se consumen sólidos.
| NOTA: El Art.
transitorio del DTO 253, Salud, publicado el 20.01.2003,
dispuso que la presente modificación entrará en vigencia
30 días después de su publicación en el Diario Oficial.
|
| NOTA 1: El
Art. segundo del DTO 68, Salud, publicado el 23.01.2006,
dispuso que la modificación introducida al presente
artículo rige a contar de 180 días después de su
publicación.
|
|
| DTO 253,
SALUD
Nº 1 D)
D.O. 20.01.2003 |
| Decreto 24, SALUD
Art. 1 Nº 15
D.O. 24.11.2011 |
| DTO 68,
SALUD
Art. primero Nº 34
D.O. 23.01.2006 |
|
Artículo 541.- Los alimentos para deportistas
se etiquetarán conforme a las
disposiciones relativas a etiquetado general y según lo
dispuesto en los artículos 110 y 540 de este
Reglamento.
Los que tengan adición de: aminoácidos, L- carnitina,
colina, inosina, ubiquinona, creatina, hierbas o extractos
de Panax ginseng C.A. Meyer, Schizandra chinesis (Turcz.)
Baill., Eleuterococcus senticosus Rupr. et Maxim, o que su
contenido de cafeína sea mayor a 180 mg/l. en los alimentos
líquidos y en los sólidos mayor a 90 mg/100 g., deberán
incluir una leyenda que diga: "NO RECOMENDABLE PARA MENORES
DE 15 AÑOS, EN EMBARAZO NI LACTANCIA" en letras mayúsculas
y negrita (destacado).
INCISO DEROGADO
| NOTA: El
Art. transitorio del DTO 253, Salud, publicado el
20.01.2003, dispuso que la presente modificación entrará
en vigencia 30 días después de su publicación en el
Diario Oficial.
|
| NOTA 1: El
artículo transitorio del DTO 57, Salud, publicado el
06.05.2005, dispone que las modificaciones a la presente
norma entrarán en vigencia dieciocho meses después de su
publicación.
|
|
| DTO 253, SALUD
Nº 1 D)
D.O. 20.01.2003 |
| DTO 57, SALUD
Art. único Nº 14
D.O. 06.05.2005 |
|
TITULO XXX De las Sanciones
|
| DTO 287,SALUD
Art. 2º
D.O. 18.02.2002 |
|
Artículo 542.- Las infracciones a las
disposiciones del presente reglamento serán
sancionadas por los Servicios de Salud en cuyo territorio se
hayan cometido, previa instrucción del respectivo sumario,
en conformidad con lo
establecido en el Libro X del Código
Sanitario.
| NOTA: El Art.
transitorio del DTO 253, Salud, publicado el 20.01.2003,
dispuso que la modificación introducida al presente
artículo entrará en vigencia 30 días después de su
publicación en el Diario Oficial.
|
|
| DTO 253, SALUD
Nº 1 C)
D.O. 20.01.2003 |
|
TITULO FINAL.
|
|
Artículo 543.- El presente reglamento entrará
en vigencia ciento ochenta días
después de su publicación en el Diario Oficial, fecha en
que se entenderán derogados el decreto supremo N° 60, del
5 de abril de 1982, del
Ministerio de Salud y sus modificaciones, así como
cualquier otra norma, resolución o disposición que fuera
contraria o incompatible con las contenidas en este decreto
supremo.
| NOTA: El Art.
transitorio del DTO 253, Salud, publicado el 20.01.2003,
dispuso que la modificación introducida al presente
artículo entrará en vigencia 30 días después de su
publicación en el Diario Oficial.
|
|
| DTO 253, SALUD
Nº 1 C)
D.O. 20.01.2003 |
|
Artículo Transitorio.- Sin perjuicio de lo dispuesto
en el artículo anterior, la autoridad sanitaria podrá, por
resolución fundada, autorizar la comercialización de
productos alimenticios que no cumplan con las disposiciones
de este reglamento, por un plazo máximo de un año, contado
desde la fecha de su publicación.
|
|
Anótese, tómese razón, publíquese en el Diario
Oficial e insértese en la Recopilación de Reglamentos de
la Contraloría General de República.- EDUARDO FREI
RUIZ-TAGLE, Presidente de la República.- Carlos Massad A.,
Ministro de Salud.
Lo que transcribo a Ud., para su conocimiento.- Saluda
atentamente a Ud., Fernando Muñoz Porras, Subsecretario de
Salud.
|
|

